হিমোগ্লোবিন
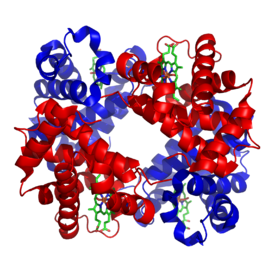
হিমোগ্লোবিন, মানব, পূর্ণবয়স্ক (heterotetramer, (αβ)2)
| ||
| ||
| Structure of human hemoglobin. The proteins' α and β subunits are in red and blue, and the iron-containing heme groups in green. From পিডিবি: 1GZX প্রটিওপিডিয়া Hemoglobin | ||
| − | ||
| প্রোটিনের ধরণ | metalloprotein, globulin | |
| ক্রিয়া | oxygen-transport | |
| সহউত্পাদক | heme (4) | |
| − | ||
| উপএককের নাম |
জিন | ক্রোমোজমাল লোকাস |
| Hb-α1 | HBA1 | Chr. 16 p13.3 |
| Hb-α2 | HBA2 | Chr. 16 p13.3 |
| Hb-β | HBB | Chr. 11 p15.5 |
হিমোগ্লোবিন একটি অক্সিজেনবাহী লৌহসমৃদ্ধ মেটালোপ্রোটিন যা মেরুদণ্ডী প্রাণিদের লোহিত কণিকা এবং কিছু অমেরুদণ্ডী প্রাণির কলায় পাওয়া যায়।
স্তন্যপায়ী প্রাণিদের ক্ষেত্রে লোহিত রক্তকণিকার শুষ্ক ওজনের ৯৬-৯৭%ই হয় হিমোগ্লোবিনের প্রোটিন অংশ, এবং জলসহ মোট ওজনের তা ৩৫%। হিমোগ্লোবিন ফুসফুস হতে অক্সিজেন দেহের বাকি অংশে নিয়ে যায় এবং কোষীয় ব্যবহারের জন্য অবমুক্ত করে। এটি অন্যান্য গ্যাস পরিবহনেও অবদান রাখে, যেমন এটি কোষকলা হতে CO2 পরিবহন করে ফুসফুসে নিয়ে যায়।
প্রতি গ্রাম হিমোগ্লোবিন ১.৩৬ হতে ১.৩৭ মিলিলিটার অক্সিজেন ধারণ করতে পারে, যা রক্তের অক্সিজেন পরিবহন ক্ষমতা ৭০গুণ বাড়িয়ে দেয়।
বংশাণুবিজ্ঞান
[সম্পাদনা]হিমোগ্লোবিন প্রোটিন সাবইউনিট (গ্লোবিন অণু) নিয়ে গঠিত এবং এই প্রোটিনগুলি পালাক্রমে পলিপেপটাইড নামক ভিন্ন অ্যামিনো অ্যাসিডের চেনে ভাঁজ এর মধ্যে থাকে। কোষের মাধ্যমে সৃষ্ট যেকনো পলিপেপটাইডের অ্যামিনো অ্যাসিডের পালাক্রমটি জিন নামক ডিএনএ প্রসারণের দ্বারা নির্ধারিত হয়। সমস্ত রকম প্রোটিনের মধ্যে কেবল অ্যামিনো অ্যাসিডের ক্রমটি প্রোটিনের রাসায়নিক বৈশিষ্ট্য এবং কার্যকারিতা নির্ধারণ করে।
মানবশরীরে একধিক হিমোগ্লোবিন জিন রয়েছে। হিমোগ্লোবিন A(প্রাপ্তবয়স্কদের মধ্যে উপস্থিত প্রধান হিমোগ্লোবিন) জিন, HBA1, HBA2 এবং HBB দ্বারা কোড করা হয়। হিমোগ্লোবিন সাবইউনিট আলফা-1 এবং আলফা-2 যথাক্রমে HBA1 এবং HBA2 জিন দ্বারা কোড করা হয়, যা উভয়ই ক্রোমোজোম 16-এর অন্তর্গত এবং একে অপরের নিকটে অবস্থান করে। হিমোগ্লোবিন সাবইউনিট বিটা সাধারণত HBB জিনের দ্বারা কোড করা, যেটি ক্রোমোজোম-11 এ অবস্থিত। হিমোগ্লোবিনের মধ্যে অবস্থিত গ্লোবিন প্রোটিনগুলির অ্যামিনো অ্যাসিড ক্রম সাধারণত প্রজাতির মধ্যে ভিন্ন হয়। এই পার্থক্যগুলি প্রজাতির মধ্যে বিবর্তনীয় দূরত্বের সাথে বৃদ্ধি পায়। উদাহরণস্বরূপ বলা যায়, মানুষের মধ্যে সবচেয়ে সাধারণ হিমোগ্লোবিন ক্রমগুলি, বোনোবো এবং শিম্পাঞ্জি প্রাণী গুলির মধ্যে সম্পূর্ণ অভিন্নরূপে লক্ষণীয়। এমনকি আলফা বা বিটা গ্লোবিন প্রোটিন চেনে একটি অ্যামিনো অ্যাসিডেরও পার্থক্য নেই।
অপর পক্ষে মানুষ এবং গরিলার হিমোগ্লোবিনে আলফা এবং বিটা উভয় চেনে একটি অ্যামিনো অ্যাসিডে ভিন্ন, এই পার্থক্যগুলি লক্ষ্য করা যায় কম ঘনিষ্ঠ সম্পর্কিত প্রজাতির মধ্যে।
এছাড়া ভিন্ন প্রজাতির মধ্যে হিমোগ্লোবিনের ভিন্ন রূপ বিদ্যমান, যদিও প্রতিটি প্রজাতির মধ্যে একটি ক্রম সাধারণত একই হয়। জিন পরিব্যক্তির ফলে একটি প্রজাতির হিমোগ্লোবিন প্রোটিনের জন্য হিমোগ্লোবিন রূপান্তর ঘটে। যদিও হিমোগ্লোবিনের এই মিউট্যান্ট ফর্ম গুলির জন্য বিশেষ কোন রোগ লক্ষ্য করা যায় না। হিমোগ্লোবিনের কিছু মিউট্যান্ট ফর্ম গুলির কারণে হিমোগ্লোবিনপ্যাথি নামক এক বংশগত রোগ লক্ষ্য করা যায়। সবচেয়ে পরিচিত হিমোগ্লোবিনপ্যাথি একটি রোগ হলো সিকেল-সেল ডিজিজ। যেটি মানবশরীরের আণবিক স্তরে লক্ষণীয় প্রথম রোগ।
থ্যালাসেমিয়া নামক রোগটি সাধারণত মানবশরীরে গ্লোবিন জিন নিয়ন্ত্রণজনিত কারণে অস্বাভাবিক হিমোগ্লোবিন উৎপাদনের প্রভাবে ঘটে। এই সমস্ত রোগ প্রধানত রক্তশূন্যতা তৈরি করে।
হিমোগ্লোবিন অ্যামিনো অ্যাসিডের ক্রমগুলির প্রকারভেদ অন্যান্য প্রোটিনের মতো অভিযোজিত হতে পারে। উদাহরণস্বরূপ , লক্ষ্য করা গেছে যে, হিমোগ্লোবিন উচ্চ উচ্চতায় বিভিন্ন উপায়ে মানিয়ে নিতে পারে । সমুদ্রপৃষ্ঠ থেকে উচ্চ উচ্চতায় বসবাসকারী প্রাণীরা তুলনামূলক কম অক্সিজেনের আংশিক চাপ অনুভব করে থাকে। এটি এই ধরনের পরিবেশে বসবাসকারী জীবদের জন্য একটি চ্যালেঞ্জ উপস্থাপন করে। কারণ হিমোগ্লোবিন, যা সাধারণত অক্সিজেনের উচ্চ আংশিক চাপে অক্সিজেনকে আবদ্ধ করে, তা অক্সিজেনকে বাঁধতে সক্ষম হয় যখন এটি আংশিক নিম্ন চাপে থাকে। ক্রমে বিভিন্ন জীব এই ধরনের চ্যালেঞ্জের সাথে অভিযোজিত হয়েছে।
উদাহরণস্বরূপ, সাম্প্রতিক গবেষণায় হরিণ ইঁদুরের জিনগত বৈচিত্রের ওপর ভিত্তি করে ব্যাখ্যা করা হয়েছে যে কীভাবে পাহাড়ে একসাথে বসবাসকারী হরিণ ও ইঁদুর উচ্চ উচ্চতায় থাকা পাতলা বাতাসে বেঁচে থাকতে সক্ষম হয়। নেব্রাস্কা-লিংকন বিশ্ববিদ্যালয়ের একজন গবেষক চারটি ভিন্ন জিনে মিউটেশন খুঁজে পেয়েছেন যা পাহাড়ের বিপরীতে নিম্নভূমিতে বসবাসকারী হরিণ ইঁদুর বনাম পাহাড়ে বসবাসকরি প্রাণীর মধ্যে পার্থক্য প্রমান করে। উচ্চভূমি এবং নিম্নভূমি উভয় থেকে ধরা বন্য ইঁদুরের পরীক্ষা করার পরে, এটি পাওয়া গেছে যে: দুটি প্রজাতির জিন কার্যত অভিন্ন। কেবল তাদের হিমোগ্লোবিনের অক্সিজেন বহন ক্ষমতা নিয়ন্ত্রণকারীরা ছাড়া। জিনগত এই বৈষম্য উচ্চভূমির ইঁদুরকে তাদের অক্সিজেনের দক্ষভাবে ব্যবহার করতে সক্ষম করে, যেহেতু পাহাড়ের মতো উচ্চ উচ্চতায় সংখ্যায় এমন প্রাণী কম পাওয়া যায়। ম্যামথ হিমোগ্লোবিন বৈশিষ্ট্যযুক্ত মিউটেশন যা নিম্ন তাপমাত্রায় অক্সিজেন সরবরাহে সক্ষম হয়, এইভাবে ম্যামথ বিশেষ প্রাণী গুলিকে প্লাইস্টোসিনের সময় উচ্চ অক্ষাংশে স্থানান্তরিত করতে সক্ষম করে। এটি আন্দিজে বসবাসকারী হামিংবার্ডগুলিতেও পাওয়া গেছে। হামিংবার্ড সাধারণত প্রচুর শক্তি ব্যয় করে এবং এই কারণে অক্সিজেনের চাহিদাও বেশি থাকে তাদের এবং তবুও আন্দিয়ান হামিংবার্ডগুলি উচ্চ উচ্চতায় সফল ভাবে অভিযোজিত হতে দেখা গেছে। উচ্চ উচ্চতায় বসবাসকারী একাধিক প্রজাতির হিমোগ্লোবিন জিনের অ-সমার্থক মিউটেশন ( Oreotrochilus, A. castelnaudii, C. violifer, P. gigas, এবং A. viridicuada ) প্রোটিনের ইনোসিটল হেক্সাফসফেট (IHP) এর সাথে কম বংশগত সাদৃশ্য লক্ষ্য করা গেছে । পাখিদের মধ্যে পাওয়া একটি অণু যা মানুষের মধ্যে 2,3-BPG এর মতো একই ভূমিকা রাখে; এর ফলে নিম্ন আংশিক চাপে অক্সিজেন বাঁধার ক্ষমতা হয়।
পাখিদের অনন্য সংবহনকারী ফুসফুসও অক্সিজেনের কম আংশিক চাপে অক্সিজেনকে দক্ষ ভাবে ব্যবহার করতে সক্ষম হয়েছে। এই দুটি অভিযোজন একে অপরকে শক্তিশালী করে এবং পাখিদের উচ্চ-উচ্চতার কর্মক্ষমতার জন্য দায়ী।
হিমোগ্লোবিন অভিযোজন মানুষের মধ্যেও সুস্থায়ী। 4,000 মিটার উচ্চতায় বসবাসকারী তিব্বতি মহিলাদের সন্তানসন্ততির উচ্চ অক্সিজেন সম্পৃক্তি জিনোটাইপ সহ বেঁচে থাকার হার বেশি। প্রাকৃতিক ভাবে নির্বাচন এই জিনের উপর কাজ করার প্রধান শক্তি বলে মনে হয় কারণ কম হিমোগ্লোবিন-অক্সিজেন সম্বন্ধযুক্ত মহিলাদের সন্তানের থেকে উচ্চ হিমোগ্লোবিন-অক্সিজেন সম্বন্ধযুক্ত মহিলাদের সন্তানের মৃত্যুর হার উল্লেখযোগ্যভাবে কম।যদিও সঠিক জিনোটাইপ এবং প্রক্রিয়া যা দ্বারা এটি ঘটে তা এখনও স্পষ্ট নয়, নির্বাচন এই মহিলাদের কম আংশিক চাপে অক্সিজেন বাঁধার ক্ষমতার উপর কর্মক্ষমতা প্রকাশ করে। যা সামগ্রিকভাবে তাদের গুরুত্বপূর্ণ বিপাকীয় প্রক্রিয়াগুলিকে আরও ভালভাবে বজায় রাখে।
গঠন
[সম্পাদনা]আণবিক সংকেতঃ(C712H1130 O245N214S2Fe)4 হিমোগ্লোবিন টারশিয়ারী এবং কোয়াটার্নারী উভয় ধরনের প্রোটিন গঠনের বৈশিষ্ট্য দেখায়। হিমোগ্লোবিনের অধিকাংশ অ্যামিনো অ্যাসিড আলফা হেলিক্স গঠন করে যেগুলো সংক্ষিপ্ত নন-হেলিক্যাল অংশ দ্বারা সংযুক্ত। হেলিক্যাল অংশগুলো হাইড্রোজেন বন্ধন দ্বারা যুক্ত থাকে যা প্রোটিন অণুটিকে স্থায়িত্ব প্রদান করে।
অধিকাংশ মানুষের হিমোগ্লোবিন অণু চারটি বর্তুলাকার প্রোটিন অংশ নিয়ে গঠিত যার প্রতিটি আবার একটি প্রোটিন শিকলের সাথে একটি নন-প্রোটিন হিম অণুর শক্ত বন্ধনে সৃষ্ট।
সংশ্লেষণ
[সম্পাদনা]হিমোগ্লোবিন সংশ্লেষিত হয় পরপর কিছু জটিল সারির ধাপের মধ্য দিয়ে। এখানে হিম অংশটি সংশ্লেষিত হয় মাইটোকন্ড্রিয়া এবং অপরিণত লোহিত রক্তকণিকার সাইটোসলের কয়েকটি ক্রমের মাধ্যমে, অন্যদিকে গ্লোবিন প্রোটিন অংশগুলি সংশ্লেষিত হয় সাইটোসোলের রাইবোজোম দ্বারা। হিমোগ্লোবিনের উৎপাদন চলতে থাকে কোষের মধ্যে প্রোয়েরিথ্রোব্লাস্ট থেকে শুরু করে অস্থি মজ্জার রেটিকিউলোসাইট পর্যন্ত।এই মুহুর্তে, স্তন্যপায়ী প্রাণীদের লাল রক্ত কোষে নিউক্লিয়াসটি হারিয়ে যায়, তবে পাখি সহ অন্যান্য অনেক প্রজাতির মধ্যে এই বিষয়ে বৈসাদৃশ্য লক্ষ্য করা যায়। এমনকি স্তন্যপায়ী প্রাণীদের মধ্যে নিউক্লিয়াসটি হারানোর পরেও,অবশিষ্ট রাইবোজোমাল আরএনএ হিমোগ্লোবিনকে পুনরায় সংশ্লেষণের অনুমতি দেয় ততক্ষণ পর্যন্ত, যতক্ষণ না রেটিকিউলোসাইট ভাস্কুলেচারে প্রবেশ করে তার আরএনএ হারাচ্ছে। (এই হিমোগ্লোবিন-সাংশ্লেষিক আরএনএ প্রকৃতপক্ষে রেটিকিউলোসাইটকে তার জালিকার চেহারা এবং নাম প্রদান করে)।
মেরুদন্ডী প্রাণীর হিমোগ্লোবিনের বিবর্তন
[সম্পাদনা]বিজ্ঞানীরা একত্রিত ভাবে মত পোষণ করেন যে মায়োগ্লোবিনকে হিমোগ্লোবিন থেকে আলাদা করার ঘটনাটি ঘটেছে মেরুদণ্ডী প্রাণীর চোয়ালের ল্যাম্প্রে বিচ্ছিন্ন হওয়ার পরে। মায়োগ্লোবিন এবং হিমোগ্লোবিনের এই বিচ্ছেদ দুটি অণুর বিভিন্ন কাজের জন্য উত্থান এবং বিকাশের পরিচিতি দেয়: মায়োগ্লোবিন সাধারণত অক্সিজেন সঞ্চয়ের ভূমিকা পালন করে অন্যদিকে হিমোগ্লোবিন অক্সিজেন পরিবহনের ভূমিকা পালন করে। α এবং β এর মতো গ্লোবিন জিনগুলি প্রোটিনের পৃথক সাবইউনিটগুলিকে এনকোড করে। এই জিনগুলির পূর্বসূরীরা একটি অন্য ঘটনার মাধ্যমে উদ্ভূত হয়েছিল। প্রায় 450 থেকে 500 মিলিয়ন বছর আগে চোয়ালবিহীন মাছ থোসোম (Gnathosome) নামক পূর্বপুরুষের থেকে প্রাপ্ত । পূর্বপুরুষের পুনর্গঠন বিষয়ক অধ্যয়ন থেকে জানা যায় যে α এবং β জিন বা বংশানুর পূর্ববর্তী পূর্বসুরি ছিল অভিন্ন গ্লোবিন সাবইউনিট দ্বারা গঠিত একটি ডাইমার, যেটি নকলের পরে একটি টেট্রামেরিক আর্কিটেকচারে একত্রিত হতে বিবর্তিত হয়। α এবং β জিনের বিকাশ হিমোগ্লোবিনের একাধিক স্বতন্ত্র সাবইউনিটের সমন্বয়ে গঠিত হওয়ার সম্ভাবনা তৈরী করে, যা অক্সিজেন পরিবহনে হিমোগ্লোবিনের ক্ষমতার কেন্দ্রবিন্দু।একাধিক সাবইউনিট থাকার ফলে হিমোগ্লোবিনের অক্সিজেনকে সহযোগিতামূলকভাবে আবদ্ধ করার পাশাপাশি রূপক হিসেবে নিয়ন্ত্রন করার ক্ষমতাতে অবদান রাখে। পরবর্তীকালে, α জিনটিও HBA1 এবং HBA2 জিন গঠনের জন্য একটি সদৃশ ঘটনা ঘটিয়েছিল। এই পুনরায় সদৃশতা এবং ভিন্নতাগুলি α- এবং β-এর মতো গ্লোবিন জিনের একটি বৈচিত্র্যময় পরিসর তৈরি করেছে যা নিয়ন্ত্রিত হয় যাতে কিছু নির্দিষ্ট রূপ বিকাশের বিভিন্ন পর্যায়ে ঘটে।
Channichthyidae পরিবারের বেশিরভাগ বরফ জলের মাছ ঠান্ডা জলে অভিযোজিত হতে গিয়ে তাদের হিমোগ্লোবিন জিন হারিয়েছে।
অক্সিহিমোগ্লোবিনে লোহার জারণ অবস্থা
[সম্পাদনা]অক্সিজেনযুক্ত হিমোগ্লোবিনের জারণ অবস্থা নির্ধারণ করা কঠিন কারণ অক্সিহিমোগ্লোবিন (Hb-O2), পরীক্ষামূলক পরিমাপের মাধ্যমে, ডাইম্যাগনেটিক। তবুও অক্সিজেন এবং লোহা উভয়েরই সর্বনিম্ন-শক্তি (ভূমি-স্থিতি) ইলেক্ট্রন বিন্যাস টি প্যারাম্যাগনেটিক। অক্সিজেনের সর্বনিম্ন-শক্তি রূপ , এবং লোহার জারণ সম্পর্কিত সর্বনিম্ন শক্তি রূপগুলি হল:
● অক্সিজেন ত্রয়ী, সর্বনিম্ন-শক্তির আণবিক অক্সিজেন প্রজাতি, যার অ্যান্টিবন্ডিং π* আণবিক কক্ষপথে অযুগ্ম ইলেকট্রন রয়েছে।
● আয়রন(II) একটি উচ্চ-স্পিন 3d6 বিন্যাসে চারটি অযুগ্ম ইলেকট্রন বিদ্যমান।
● আয়রন(III) (3d5) এর একটি অযুগ্ম ইলেকট্রন আছে, এবং এভাবে এক বা একাধিক অযুগ্ম ইলেকট্রন থাকতে হবে।
এখানে সমস্ত কাঠামোই প্যারাম্যাগনেটিক (অযুগ্ম ইলেকট্রন আছে), ডাইম্যাগনেটিক নয়। এইভাবে, লোহা এবং অক্সিজেনের সংমিশ্রণে একটি অ-স্বজ্ঞাত ( অন্তত একটি প্রজাতির জন্য একটি উচ্চ-শক্তি) ইলেকট্রনের বণ্টন বিদ্যমান থাকা আবশ্যক, যাতে পর্যবেক্ষণ করা ডাইম্যাগনেটিজম ব্যাখ্যা করা যায় এবং যেখানে কোনো অযুগ্ম ইলেকট্রন নেই।
ডাইম্যাগনেটিক Hb-O2 তৈরি করার দুটি যৌক্তিক সম্ভাবনা হল:
1 নিম্ন-স্পিন যুক্ত Fe 2+ একক অক্সিজেনের সাথে আবদ্ধ হয়। লো-স্পিন আয়রন এবং একক অক্সিজেন উভয়ই ডাইম্যাগনেটিক হয়। যেখানে, অক্সিজেনের একক রূপ হল অণুর উচ্চ-শক্তির রূপ।
2 নিম্ন-স্পিন যুক্ত Fe 3+ , O2 •− ( সুপারঅক্সাইড আয়ন) এবং দুটি অযুগ্ম ইলেকট্রনকে অ্যান্টিফেরোম্যাগনেটিকভাবে জোড়া দেয়, যা পর্যবেক্ষণ করা ডাইম্যাগনেটিক বৈশিষ্ট্য প্রদান করে। ফলে লোহা জারিত হয়েছে (একটি ইলেকট্রন হারিয়ে), এবং অক্সিজেন হ্রাস পেয়েছে (একটি ইলেকট্রন লাভ করে)।
আরেকটি সম্ভাব্য মডেল যাতে লো-স্পিন Fe4+ পারক্সাইডের সাথে আবদ্ধ হয়, O22−, নিজে থেকেই বাতিল হয়ে যায়, কারণ লোহা প্যারাম্যাগনেটিক (যদিও পারক্সাইড আয়ন ডাইম্যাগনেটিক)। এখানে, লোহা, দুটি ইলেকট্রন দ্বারা জারিত হয়েছে, এবং অক্সিজেনের দুটি ইলেকট্রন হ্রাস পেয়েছে।
প্রত্যক্ষ পরীক্ষামূলক তথ্য:
●এক্স-রে ফটোইলেক্ট্রন স্পেকট্রোস্কোপি প্রমান করে লোহার প্রায় 3.2 জারণ অবস্থা রয়েছে।
●O-O বন্ডের. অবলোহিত কম্পন তরঙ্গগুলি (Infrared Vibrational Frequency) সুপারঅক্সাইডের সাথে একটি মানানসই দৈর্ঘ্যের বন্ড প্রস্তুত করে (একটি বন্ড অর্ডার প্রায় 1.6, সুপার অক্সাইড 1.5 সহ)।
●প্রান্তের এক্স-রে শোষণ ঘটে লোহার K-প্রান্ত । ডিঅক্সিহিমোগ্লোবিন এবং অক্সিহিমোগ্লোবিনের মধ্যে 5 ইলেক্ট্র ভোল্ট শক্তি স্থানান্তর, সমস্ত মেথেমোগ্লোবিন প্রজাতির জন্য, দৃঢ়ভাবে Fe 2+ এর তুলনায় Fe 3+ এর কাছাকাছি একটি প্রকৃত স্থানীয় চার্জের পরামর্শ দেয়।
এইভাবে, Hb-O2 -এ লোহার নিকটতম সাধারণ অবস্থা হল +3 অবস্থা এবং অক্সিজেন −1 অবস্থা (সুপারঅক্সাইড হিসাবে O2− )। এই রূপরেখা ডাইম্যাগনেটিজম উৎপন্ন হয় সুপারঅক্সাইডের একক অযুগ্ম ইলেক্ট্রন থেকে অ্যান্টিফেরোম্যাগনেটিকভাবে ও লোহার উপর একক অযুগ্ম ইলেক্ট্রনের সাথে সারিবদ্ধ করে (একটি কম-স্পিন d5 অবস্থায়),এই রূপরেখা নেট স্পিন দেয় না যা ডাইম্যাগনেটিক অক্সিহিমোগ্লোবিনের সাথে সামঞ্জস্য পরীক্ষা থেকে লক্ষ্য করা যায়।
ডাইম্যাগনেটিক অক্সিহেমোগ্লোবিনের জন্য উপরের যৌক্তিক সম্ভাবনার দ্বিতীয়টি পরীক্ষার মাধ্যমে সঠিক হিসেবে গণ্য হয়, এটি আশ্চর্যজনক নয়: একক অক্সিজেন (সম্ভাবনা #1) একটি অবাস্তবিক উচ্চ শক্তির অবস্থা। মডেল 3 চার্জের প্রতিকূল পৃথকীকরণের দিকে নির্দেশ করে (চৌম্বকীয় ডেটার সাথে একমত নয়), যদিও এটি একটি অনুরণন ফর্ম হিসাবে ছোট অবদান রাখে। Hb-O2 তে আয়রনের উচ্চতর জারণ অবস্থায় স্থানান্তরিত হলে পরমাণুর আকার কমে যায় এবং এটিকে পোরফাইরিন বলয়ের সমতলে প্রবেশ করতে দেয়, সমন্বিত হিস্টিডিন অবশিষ্টাংশকে টেনে নেয় এবং গ্লোবিউলিনে অ্যালোস্টেরিক পরিবর্তনগুলি শুরু করে।
জৈব-অজৈব রসায়নবিদদের প্রাথমিক অনুমানগুলি দাবি করেছে যে সম্ভাবনা #1 (উপরে) সঠিক ছিল এবং লোহা দ্বিতীয় জারণ অবস্থায় থাকা উচিত। এই মন্তব্যটি সম্ভব বলে মনে হয়েছিল, যেহেতু লোহার তৃতীয় জারণ অবস্থায় মেথেমোগ্লোবিন হিসাবে হয়, যখন সুপারঅক্সাইডের সাথে অনুষঙ্গীক নয়। O2− অক্সিডেশন ইলেক্ট্রনকে ধরে রাখার জন্য, হিমোগ্লোবিনকে স্বাভাবিক অক্সিজেন ত্রয়ীতে বাঁধতে অক্ষম হিসেবে পরিচিত ছিল কারণ এটি বাতাসে ঘটে।এইভাবে অনুমান করা হয়েছিল যে ফুসফুসে অক্সিজেন গ্যাস আবদ্ধ হলে লোহা Fe(II) হিসাবে থেকে যায়। এই পূর্ববর্তী সর্বোত্তম মডেলের লোহার রসায়ন সুরুচিপূর্ণ ছিল, কিন্তু ডাইম্যাগনেটিক, উচ্চ-শক্তি, একক অক্সিজেন অণুর প্রয়োজনীয় উপস্থিতি কখনই ব্যাখ্যা করা হয়নি। এটি সর্বোত্কৃষ্ট যুক্তি দেওয়া হয়েছিল যে একটি অক্সিজেন অণুর বাঁধাই উচ্চ-স্পিন আয়রন (II) শক্তিশালী-ক্ষেত্র লিগ্যান্ডগুলির একটি অষ্টতলকীয় ক্ষেত্রে স্থাপন করে; ক্ষেত্রের এই পরিবর্তন স্ফটিক ক্ষেত্রের বিভাজন শক্তিকে বাড়িয়ে তুলবে, যার ফলে লো-স্পিন রূপরেখায় লোহার ইলেকট্রন যুক্ত হবে, যা Fe(II) তে ডাইম্যাগনেটিক হবে। এই জোরপূর্বক লো-স্পিন পেয়ারিং প্রকৃতপক্ষে লোহাতে ঘটবে বলে মনে করা হয় যখন অক্সিজেন আবদ্ধ হয়, কিন্তু আয়রনের আকার পরিবর্তন ব্যাখ্যা করার জন্য যথেষ্ট নয়। অক্সিজেন দ্বারা লোহা থেকে একটি অতিরিক্ত ইলেকট্রন নিষ্কাশনের জন্য লোহার ছোট আকার এবং বর্ধিত জারণ অবস্থা এবং অক্সিজেনের দুর্বল বন্ধন উভয়ই ব্যাখ্যা করা প্রয়োজন।
একটি পূর্ণ-সংখ্যা জারণ অবস্থার নিয়োগ একটি প্রথানুগত্য মাত্র, কারণ সমযোজী বন্ধনগুলির সম্পূর্ণ ইলেক্ট্রন স্থানান্তর নিখুঁত বন্ড অর্ডারের প্রয়োজন নেই। এইভাবে, প্যারাম্যাগনেটিক Hb-O2 -এর তিনটি মডেলই Hb-O2 -এর প্রকৃত ইলেকট্রন বিন্যাস কিছুটা ছোট মাত্রায় (অনুনাদন দ্বারা) অবদান রাখতে পারে।অবশেষে বলা যায়, Hb-O2 -এ লোহার মডেল Fe(III) হচ্ছে সর্বোত্কৃষ্ট ধারণার চেয়ে বেশি সঠিক যে এটি Fe(II) থেকে যায়।
সহযোগিতা
[সম্পাদনা]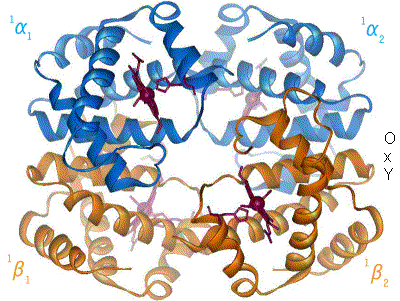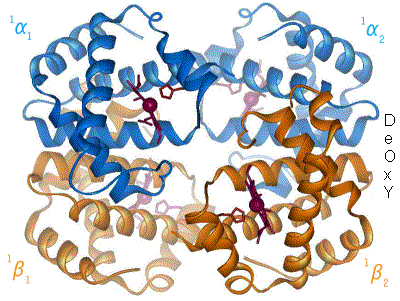
যখন অক্সিজেন আয়রন কমপ্লেক্সের সাথে আবদ্ধ হয়, তখন এটি লোহার পরমাণুকে পোরফাইরিন রিংয়ের সমতলের কেন্দ্রের দিকে ফিরিয়ে দেয় (চলমান চিত্র দেখুন)। একই সময়ে, লোহার অন্য মেরুতে মিথস্ক্রিয়াকারী হিস্টিডিনের অবশিষ্টাংশের ইমিডাজল সাইড-চেইনটি পোরফাইরিন বলয়ের প্রস্থান করে। এই মিথস্ক্রিয়া বল টেট্রামারের বাইরের দিকে রিং এর সমতলে বল প্রয়োগ করে, এবং লোহার পরমাণুর কাছাকাছি চলে যাওয়ার সাথে সাথে হিস্টিডিন ধারণকারী প্রোটিন হেলিক্সে একটি চাপ সৃষ্টি করে। এই স্ট্রেনটি টেট্রামারের অবশিষ্ট তিনটি মনোমারে স্থানান্তরিত হয়, যেখানে এটি অন্যান্য হিম গুলিতে অনুরূপ গঠনগত পরিবর্তনে বাধ্য করে যাতে এই সাইটগুলিতে অক্সিজেন সহজে আবদ্ধ হয়।
যেহেতু অক্সিজেন হিমোগ্লোবিনের একটি মনোমারের সাথে আবদ্ধ হয়, তাই টেট্রামারের রূপটি T (টান) অবস্থা থেকে R (স্বচ্ছন্দ) অবস্থায় স্থানান্তরিত হয়। এই স্থানান্তরটি বাকি তিনটি মনোমারের হিম গ্রুপের সাথে অক্সিজেনকে আবদ্ধ করে, এইভাবে এটি অক্সিজেনের সাথে হিমোগ্লোবিন অণুকে পরিপূর্ণ করে।
স্বাভাবিক প্রাপ্তবয়স্ক হিমোগ্লোবিনের টেট্রামেরিক বিভাগে, অক্সিজেন বন্ধন একটি সমবায় প্রক্রিয়া আকারে থাকে। অক্সিজেনের দ্বারা হিমোগ্লোবিনে আবদ্ধ অণুর অক্সিজেন সম্পৃক্ততা বৃদ্ধি পায়, অক্সিজেন বন্ডের প্রথম অণুগুলি পরবর্তী অণুগুলিকে একই আকৃতিকে আবদ্ধ হতে প্রভাবিত করে। এই ইতিবাচক সহযোগিতামূলক বন্ধনটি উপরে আলোচিত হিমোগ্লোবিন প্রোটিন কমপ্লেক্সের স্টেরিক গঠনগত পরিবর্তনের মাধ্যমে তৈরী হয়। উদাহরনস্বরূপ, যখন হিমগ্লোবিনে একটি সাবইউনিট প্রোটিন অক্সিজেনযুক্ত হয়ে যায়, তখন পুরো কমপ্লেক্সে একটি গঠনমূলক বা কাঠামোগত পরিবর্তন শুরু হয়, যার ফলে অন্যান্য সাবইউনিটগুলি অক্সিজেনের প্রতি বর্ধিত সম্বন্ধ তৈরী করে।
ফলস্বরূপ, হিমোগ্লোবিনের অক্সিজেন বাইন্ডিং সিগময়েডাল বা S- আকৃতির গঠন তৈরি করে যা হাইপারবোলিক বক্ররেখার বিপরীতে অসহযোগি বন্ধনের সাথে যুক্ত হয়।
হিমোগ্লোবিনে সহযোগি গতিশীল প্রক্রিয়া এবং নিম্ন-তরঙ্গ রেজোন্যান্সের সাথে এর সম্পর্ক নিয়ে ইতোমধ্যে বর্ণনা করা হয়েছে।
হিমোগ্লোবিন সম্পর্কিত রোগ
[সম্পাদনা]থ্যালাসেমিয়া
[সম্পাদনা]থ্যালাসেমিয়া হলে একটি মারাত্মক জিনঘটিত রোগ যাতে হিমোগ্লোবিনের α ও β চেন গঠিত হয় না বা আংশিক গঠিত হয়, ফলে লোহিত রক্তকণিকার অক্সিজেন পরিবহণ ক্ষমতা কমে।
অক্সিজেন ব্যতীত অন্যান্য লিগ্যান্ডের বন্ধন
[সম্পাদনা]অক্সিজেন লিগ্যান্ডের পাশাপাশি হিমোগ্লোবিনকে সহযোগিতামূলক পদ্ধতিতে আবদ্ধ করে। হিমোগ্লোবিন লিগ্যান্ডগুলি কার্বন মনোক্সাইড (CO) এবং অ্যালোস্টেরিক লিগ্যান্ড যেমন কার্বন ডাই অক্সাইড (CO 2 ) এবং নাইট্রিক অক্সাইড (NO) এর মতো প্রতিরোধকও অন্তর্ভুক্ত করে। কার্বন ডাই অক্সাইড গ্লোবিন প্রোটিনে অ্যামিনো গ্রুপের সাথে আবদ্ধ হয়ে কার্ব-অ্যামিনোহিমোগ্লোবিন গঠন করে; এটি গ্লোবিন প্রোটিনের নির্দিষ্ট থিওল গ্রুপের সাথে আবদ্ধ হয়ে একটি S-nitrosothiol রূপ গঠন করে। এই প্রক্রিয়াটি স্তন্যপায়ী প্রাণীদের কার্বন ডাই অক্সাইড পরিবহন প্রক্রিয়ায় প্রায় 10 শতাংশ দায়ী। হিমোগ্লোবিন দ্বারা নাইট্রিক অক্সাইডও পরিবাহিত হতে পারে; যা মুক্ত নাইট্রিক অক্সাইড এবং থিওল গ্রূপে আবার বিচ্ছিন্ন হয়ে যায়, কারণ হিমোগ্লোবিন তার হিম অংশ থেকে অক্সিজেন মুক্ত করে। পেরিফেরাল কোষে এই নাইট্রিক অক্সাইড পরিবহন, কোষের মধ্যে অক্সিজেন পরিবহনের ভূমিকা পালন করে বলে অনুমান করা হয়, এই প্রক্রিয়াটি সম্ভব হয় যখন কম অক্সিজেন মাত্রা যুক্ত কোষের মধ্যে ভ্যাসোডাইলেটর নাইট্রিক অক্সাইড মুক্ত করে।
প্রতিযোগিতামূলক:
কার্বন মনোক্সাইডের মতো অণু দ্বারা অক্সিজেন বন্ধন প্রভাবিত হয় (যেমন: তামাক পাতার ধোঁয়া, নিষ্কাশীত গ্যাস এবং চুল্লিতে অসম্পূর্ণ জ্বলন)। কার্বন মনোক্সাইড অক্সিজেনের সাথে প্রতিদ্বন্দ্বীতায় লিপ্ত হয় হিম অংশে। কার্বন মনোক্সাইডে হিমোগ্লোবিন বন্ধনের প্রবণতা অক্সিজেনের প্রতি তার প্রবণতার থেকে 250 গুণ বেশি হয়, অর্থাৎ অল্প পরিমাণে কার্বন মনোক্সাইড নির্দিষ্ট কোষে অক্সিজেন সরবরাহ প্রক্রিয়াটিতে হিমোগ্লোবিনের কার্য-ক্ষমতা কে হ্রাস করে। যেহেতু কার্বন মনোক্সাইড একটি স্বাদহীন, বর্ণহীন এবং গন্ধহীন গ্যাস। তাছাড়া এটি একটি মরণাত্মক গ্যাস, তাই বাসস্থানে এর বিপজ্জনক মাত্রা সম্পর্কে সতর্ক হওয়ার জন্য কার্বন মনোক্সাইড ডিটেক্টর বাণিজ্যিকভাবে সহজলভ্য করা হয়েছে। যখন হিমোগ্লোবিন কার্বন মনোক্সাইডের সাথে মিলিত হয়, তখন উজ্জ্বল লাল বর্ণের কার্বক্সিহিমোগ্লোবিন নামক একটি যৌগ তৈরি করে, যা কার্বন মনোক্সাইড বিষক্রিয়ায় আক্রান্তদের ত্বকে সাদা বা নীল রঙের পরিবর্তে গোলাপী রঙ লক্ষ্য করা যায়।যখন বাতাসে কার্বন মনোক্সাইডের মাত্রা 0.02% এর কম থাকে, তখন মাথাব্যথা এবং বমি বমি ভাব অনুভব হয়; যদি কার্বন মনোক্সাইডের ঘনত্ব 0.1% বৃদ্ধি পায়, তখন জ্ঞান হারিয়ে ফেলার প্রবণতা লক্ষ্য করা যায়।অতিরিক্ত ধূমপায়ীদের, অক্সিজেন-সক্রিয় স্থানগুলির 20% পর্যন্ত ব্লক হয়ে যায় এই কার্বন মনোক্সাইড দ্বারা।
অনুরূপ ভাবে, হিমোগ্লোবিনেরও প্রতিযোগিতামূলক বন্ধনের প্রবণতা রয়েছে, সায়ানাইড (CN − ), সালফার মনোক্সাইড (SO), সালফাইড (S 2− ), হাইড্রোজেন সালফাইড (H 2 S) গ্যাসগুলির সাথে ।এইসব গ্যাসগুলি হিম অংশে লোহার সাথে তার অপরিবর্তিত জারণ অবস্থা আবদ্ধ করে, কিন্তু তবুও গ্যাসগুলি অক্সিজেন-বাইন্ডিংকে বাধা দেয়, যা মারাত্মক বিষাক্ততা সৃষ্টি করে।
অক্সিজেন সহ অন্যান্য গ্যাসের বাইন্ডিং এবং পরিবহনকে সমর্থন করার জন্য হিম গ্রুপের লোহার পরমাণুকে অবশ্যই লৌহঘটিত (Fe 2+ ) জারণ অবস্থায় থাকতে হবে (পূর্বে ব্যাখ্যা করা হয়েছে)। অক্সিজেন ছাড়া ফেরিক (Fe 3+ ) অবস্থায় প্রাথমিক জারণ হিমোগ্লোবিনকে হিমোগ্লোবিন বা মেথেমোগ্লোবিনে রূপান্তরিত করে, যা অক্সিজেন বাইন্ডিং এ অক্ষম। যাতে এটি না ঘটতে পারে তাই স্বাভাবিক লোহিত রক্ত কণিকার হিমোগ্লোবিন একটি রূপান্তরকরণ দ্বারা সুরক্ষিত থাকে। নাইট্রিক অক্সাইড লোহিত রক্তকণিকায় হিমোগ্লোবিনের একটি ছোট ভগ্নাংশকে মেথেমোগ্লোবিনে রূপান্তর করতে সক্ষম হয়। পরের প্রতিক্রিয়া হল গ্লোবিনের আরও প্রাচীন নাইট্রিক অক্সাইড ডাইঅক্সিজেনেস ফাংশনের একটি অবশিষ্ট কার্যকলাপ।
অ্যালোস্টেরিক:
কার্বন ডাই অক্সাইড হিমোগ্লোবিনের একটি আলাদা বাইন্ডিং স্থান দখল করে। কোষে, যেখানে কার্বন ডাই অক্সাইডের ঘনত্ব বেশি, সেখানে কার্বন ডাই অক্সাইড হিমোগ্লোবিনের অ্যালোস্টেরিক অংশের সাথে আবদ্ধ হয়, হিমোগ্লোবিন থেকে অক্সিজেন শূন্য করার সুবিধা দেয় এবং শেষ পর্যন্ত বিপাক প্রক্রিয়ার মধ্য দিয়ে কোষে অক্সিজেন প্রদানের পরে শরীর থেকে এটি অপসারণ হয়। শিরায় অবস্থিত রক্ত দ্বারা কার্বন ডাই অক্সাইডের প্রতি এই প্রবণতার বৃদ্ধি বোর প্রভাব নামে পরিচিত। কার্বনিক অ্যানহাইড্রেজ উৎসেচক এর মাধ্যমে, কার্বন ডাই অক্সাইড জলের সাথে বিক্রিয়া করে কার্বনিক অ্যাসিড প্রস্তুত করে যা বাইকার্বোনেট এবং প্রোটনে পরিণত হয়: CO 2 + H 2 O → H 2 CO 3 → HCO 3− + H+

উচ্চ কার্বন ডাই অক্সাইডে যুক্ত রক্তে পি.এইচ এর মাত্রা কম থাকে (অম্ল প্রকৃতির)। হিমোগ্লোবিন প্রোটন এবং কার্বন ডাই অক্সাইডকে আবদ্ধ করতে পারে, যা প্রোটিনের গঠনগত পরিবর্তন ঘটানোর সাথে সাথে অক্সিজেন মুক্তিকে সহজ করে। যখন কার্বন ডাই অক্সাইড α-অ্যামিনো গ্রুপে আবদ্ধ থাকে তখন প্রোটিনের বিভিন্ন জায়গায় প্রোটন আবদ্ধ হয়। কার্বন ডাই অক্সাইড হিমোগ্লোবিনের সাথে আবদ্ধ হয়ে কার্বামিনোহেমোগ্লোবিন (carbaminohemoglobin) গঠন করে। কার্বন ডাই অক্সাইড এবং অ্যাসিডের আবদ্ধতার কারণে অক্সিজেনের প্রতি হিমোগ্লোবিনের প্রবণতার এইরুপ হ্রাসকে বোর প্রভাব বলা হয়। বোর প্রভাব R অংশের পরিবর্তে T অংশে বেশি প্রভাবশালী। (O2 -স্যাচুরেশন গ্রাফ তুলনামূলক ডানদিকে স্থানান্তরিত করে)। বিপরীতভাবে, যখন রক্তে কার্বন ডাই অক্সাইডের মাত্রা হ্রাস পায় (অর্থাৎ, ফুসফুসের ক্যাপিলারিতে), তখন কার্বন ডাই অক্সাইড এবং প্রোটন হিমোগ্লোবিন থেকে নিঃসৃত হয়, ফলে প্রোটিনে অক্সিজেনের প্রবণতা বাড়ায়। পি.এইচ হ্রাসের কারণে হিমোগ্লোবিনে অক্সিজেন বাইন্ডিং ক্ষমতা হ্রাস পায় (অর্থাৎ গ্রাফটি নিচে সরে, কেবল ডানদিকে নয়)। এটি রুট এফেক্ট নামে পরিচিত। এটি অস্থি বিশেষ মাছে দেখা যায়।
এখানে বন্ধন সৃষ্টি করার জন্য হিমোগ্লোবিনের অক্সিজেন মুক্ত করা অত্যন্ত প্রয়োজনীয়; যদি তা না হয়, তাহলে বন্ধন সৃষ্টি করার কোনো ভূমিকাই থাকে না। হিমোগ্লোবিনের সিগময়েডাল বক্ররেখা এটিকে বাঁধাই করতে দক্ষ করে তোলে (ফুসফুস O2 গ্রহণ করে), এবং খালি করতে (কোষ O2 খালি করে) কার্যকর করে।
উচ্চ উচ্চতায় অবস্থিত ব্যক্তিদের মধ্যে, রক্তে 2,3 -বিসফসফোগ্লিসারেট (2,3-BPG) এর ঘনত্ব বৃদ্ধি পায়, যা এই ব্যক্তিদের নিম্ন অক্সিজেন প্রবণতা পরিস্থিতিতে কোষে প্রচুর পরিমাণে অক্সিজেন সরবরাহ করতে সাহায্য করে। এই ঘটনাটি, যেখানে Y অনু একটি পরিবহন অণু Z এর সাথে X অনুর বন্ধনকে প্রভাবিত করে, যাকে হেটেরোট্রপিক অ্যালোস্টেরিক প্রভাব বলা হয়। উচ্চ উচ্চতায় জীবের হিমোগ্লোবিনও এমনভাবে অভিযোজিত হয়েছে যে এটি 2,3-BPG-এর সাথে কম প্রবণতায় থাকে এবং এই কারণে প্রোটিনটি তার R অবস্থার দিকে আরও স্থানান্তরিত হয়। R অবস্থায়, হিমোগ্লোবিন অক্সিজেনকে আরও সহজে আবদ্ধ করে, এইভাবে জীবগুলিকে প্রয়োজনীয় বিপাক প্রক্রিয়াগুলি সম্পাদন করতে সাহায্য করে, যখন অক্সিজেন কম আংশিক চাপে অবস্থান করে।
মানুষ ব্যতীত অন্যান্য প্রাণীরা হিমোগ্লোবিনের সাথে আবদ্ধ হওয়ার জন্য বিভিন্ন অণু ব্যবহার করে এবং প্রতিকূল পরিস্থিতিতে এর অক্সিজেন প্রবণতা পরিবর্তন করে। মাছ ATP এবং GTP উভয়ই ব্যবহার করে। এগুলি মাছের হিমোগ্লোবিন অণুর উপর একটি ফসফেট "পকেট" এর সাথে আবদ্ধ হয়। যা উত্তেজনাপূর্ণ অবস্থাকে স্থিতিশীল করে এবং অক্সিজেন প্রবণতা হ্রাস করে। GTP হিমোগ্লোবিনের অক্সিজেন প্রবণতা ATP-এর তুলনায় অনেক বেশি কমিয়ে দেয়, যা একটি অতিরিক্ত হাইড্রোজেন বন্ধনের কারণে ঘটে বলে মনে করা হয় এবং এটি উত্তেজিত অবস্থাকে স্থিতিশীল করে। হাইপোক্সিক অবস্থার অধীনে, অক্সিজেনের প্রবণতা বাড়াতে মাছের লোহিত রক্তকণিকায় ATP এবং GTP উভয়ের ঘনত্ব হ্রাস পায়।
ভ্রূণের হিমোগ্লোবিন (HbF, α 2 γ 2 ) নামক একটি বিকল্প হিমোগ্লোবিন ভ্রূণে পাওয়া যায় এবং এটি প্রাপ্তবয়স্ক হিমোগ্লোবিনের তুলনায় অক্সিজেনকে বেশি আবদ্ধ করে। ভ্রূণের হিমোগ্লোবিনে অক্সিজেন বাইন্ডিং বক্ররেখা বাম দিকে স্থানান্তরিত হয় প্রাপ্তবয়স্ক দের হিমোগ্লোবিনের তুলনায় । ফলস্বরূপ, প্লাসেন্টায় ভ্রূণের রক্ত মাতৃ রক্ত থেকে অক্সিজেন নিতে সক্ষম হয়।
হিমোগ্লোবিন অণুর গ্লোবিন অংশেও নাইট্রিক অক্সাইড (NO) বহন করতে সক্ষম।এটি পরিধিতে অক্সিজেন সরবরাহের উন্নতি করে এবং শ্বাস-প্রশ্বাস নিয়ন্ত্রণে অবদান রাখে। নাইট্রিক অক্সাইড গ্লোবিনের একটি নির্দিষ্ট সিস্টেইনের সাথে বিপরীতভাবে আবদ্ধ হয়; এই বন্ধনটি হিমোগ্লোবিনের অবস্থার (R বা T) উপর নির্ভর করে। ফলস্বরূপ এস-নাইট্রোসাইলেটেড হিমোগ্লোবিন বিভিন্ন নাইট্রিক অক্সাইড সম্পর্কিত ক্রিয়াকলাপ, যেমন ভাস্কুলার প্রতিরোধক নিয়ন্ত্রণ, রক্তচাপ এবং শ্বাস-প্রশ্বাসকে প্রভাবিত করে। নাইট্রিক অক্সাইড লোহিত রক্ত কণিকার সাইটোপ্লাজম থেকে নিঃসৃত হয় না, কিন্তু AE1 নামক একটি অ্যানিয়ন এক্সচেঞ্জার দ্বারা সেগুলো থেকে পরিবাহিত হয়।
গবেষণার ইতিহাস
[সম্পাদনা]
1825 সালে, জোহান ফ্রেডরিখ এঙ্গেলহার্ট আবিষ্কার করেন যে বিভিন্ন প্রজাতির হিমোগ্লোবিনে লোহা থেকে প্রোটিনের অনুপাত ভিন্ন। লোহার পরিচিত পারমাণবিক ভর থেকে তিনি হিমোগ্লোবিনের আণবিক ভর গণনা করেন n × 16000 ( n = হিমোগ্লোবিন প্রতি লোহার পরমাণুর সংখ্যা, এখন 4 হিসাবে পরিচিত), প্রথমবার একটি প্রোটিনের আণবিক ভর নির্নয়।এই "দ্রুত উপসংহার" সেই সময়ে বিজ্ঞানীদের কাছ থেকে প্রচুর উপহাস কুড়িয়ে ছিল, যারা বিশ্বাস করতে পারেনি যে কোনও অণু এত বড় হতে পারে। গিলবার্ট স্মিথসন অ্যাডায়ার 1925 সালে হিমোগ্লোবিন দ্রবণের অসমোটিক চাপ পরিমাপ করে এঙ্গেলহার্টের ফলাফল নিশ্চিত করেছিলেন।
যদিও 1794 সাল থেকে রক্ত অক্সিজেন বহন করে বলে জানা গিয়েছিল, হিমোগ্লোবিনের অক্সিজেন বহনকারী বৈশিষ্ট্য 1840 সালে হুয়েনফেল্ড বর্ণনা করেছিলেন। 1851 সালে, জার্মান ফিজিওলজিস্ট অটো ফাঙ্কে একটি ধারাবাহিক নিবন্ধ প্রকাশ করেন যাতে তিনি ক্রমাগতভাবে দ্রাবক যেমন বিশুদ্ধ জল, অ্যালকোহল বা ইথার দিয়ে লোহিত রক্তকণিকাকে পাতলা করে, ফলস্বরূপ প্রোটিন দ্রবণ থেকে দ্রাবকের ধীরগতিতে বাষ্পীভবনের মাধ্যমে হিমোগ্লোবিন ধীরেধীরে স্ফটিকে পরিণত হয়। তার কয়েক বছর পর ফেলিক্স হোপ-সেলার বর্ণনা করেছিলেন হিমোগ্লোবিনের বিপরীত অক্সিজেনেশন ধর্ম।
1959 সালে, হিমোগ্লোবিনের আণবিক গঠন নির্ধারণ করেন ম্যাক্স পেরুৎজ একটি এক্স-রে ক্রিস্টালোগ্রাফির দ্বারা। এই কাজের ফলে জন কেন্ড্রিও'র সাথে গ্লোবিউলার প্রোটিনের গঠন নিয়ে গবেষণার জন্য 1962 সালে রসায়নে নোবেল পুরস্কার তাঁদের যৌথভাবে পুরস্কৃত করা হয়।
রক্তে হিমোগ্লোবিনের ভূমিকা ফরাসি ফিজিওলজিস্ট ক্লদ বার্নার্ড ব্যাখ্যা করেছিলেন। হিমোগ্লোবিন নামটি হিম এবং গ্লোবিন শব্দগুলি থেকে উদ্ভূত হয়েছে, এটি প্রতিফলিত করে যে হিমোগ্লোবিনের প্রতিটি সাবইউনিট একটি স্থাপিত হেম গ্রুপ সহ একটি গ্লোবুলার প্রোটিন ।প্রতিটি হিম গ্রুপে একটি লোহার পরমাণু থাকে, যা আয়ন-প্ররোচিত ডাইপোল বলের মাধ্যমে একটি অক্সিজেন অণুকে আবদ্ধ করতে পারে।সমস্ত স্তন্যপায়ী প্রাণীদের মধ্যে একটি সাধারণ ব্যাপার হলো এদের হিমোগ্লোবিনে এই ধরনের চারটি সাবইউনিটই থাকে।
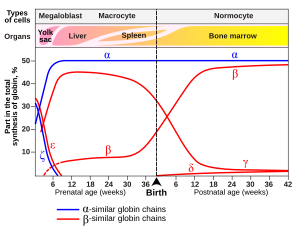
মানবশরীরে হিমোগ্লোবিনের প্রকার
[সম্পাদনা]হিমোগ্লোবিনের রূপগুলি স্বাভাবিক ভ্রূণ এবং ভ্রূণের বিকাশের একটি অংশ। প্রজননের তারতম্যের কারণে, এই প্রকার গুলি জনসংখ্যার মধ্যে হিমোগ্লোবিনের প্যাথলজিক মিউট্যান্ট ফর্মও হতে পারে। কিছু সুপরিচিত হিমোগ্লোবিন রূপ, যেমন সিকেল-সেল অ্যানিমিয়া, হিমোগ্লোবিনোপ্যাথি রোগের জন্য দায়ী। অন্যান্য প্রকার গুলি কোন সনাক্তকরণযোগ্য প্যাথলজি সৃষ্টি করে না, এবং এইভাবে নন-প্যাথলজিকাল প্রকার গুলি বিবেচিত হয়। [১][২]
ভ্রূণে ( ৮ সপ্তাহ পর্যন্ত ):
- গাওয়ার 1 (ζ 2 ε 2 )
- গাওয়ার 2 (α 2 ε 2 ) ( পিডিবি: 1A9W)
- হিমোগ্লোবিন পোর্টল্যান্ড I (ζ 2 γ 2 )
- হিমোগ্লোবিন পোর্টল্যান্ড II (ζ 2 β 2 )।
ভ্রূণে (৯ সপ্তাহ থেকে প্রসব পর্যন্ত):
জন্মের পর:
- হিমোগ্লোবিন A (প্রাপ্তবয়স্ক হিমোগ্লোবিন) (α2β2 ) ( পিডিবি: 1BZ0) - 95% এর বেশি স্বাভাবিক পরিমাণের সবচেয়ে সাধারণ হিমোগ্লোবিন।
- হিমোগ্লোবিন A (α2δ2 ) – δ চেন সংশ্লেষণ তৃতীয় ত্রৈমাসিকের পরেই শুরু হয় এবং প্রাপ্তবয়স্কদের মধ্যে এটির স্বাভাবিক পরিসীমা 1.5 - 3.5% হয়ে থাকে।
- হিমোগ্লোবিন F (ভ্রূণের হিমোগ্লোবিন) (α2γ2) – খুব সীমিত সংখ্যার প্রাপ্তবয়স্কদের মধ্যে এই হিমোগ্লোবিন-F, এফ-সেল নামক লাল কোষের মধ্যে সীমাবদ্ধ থাকে। যদিও সিকেল-সেল এবং বিটা-থ্যালাসেমিয়ায় আক্রান্ত ব্যক্তিদের মধ্যে হিমোগ্লোবিন F-এর মাত্রা বাড়ানো সম্ভব।
যে প্রকার গুলি রোগ সৃষ্টি করে:
- হিমোগ্লোবিন ডি-পাঞ্জাব - (α2βD2) - হিমোগ্লোবিনের একটি ভিন্ন রূপ।
- হিমোগ্লোবিন এইচ (β4) - β চেনের একটি টেট্রামার দ্বারা গঠিত হিমোগ্লোবিনের একটি প্রকার, যা α থ্যালাসেমিয়ার মধ্যেও থাকতে পারে।
- হিমোগ্লোবিন বার্টস (γ4) - γ চেনের একটি টেট্রামার দ্বারা গঠিত, হিমোগ্লোবিনের একটি প্রকার, যা α থ্যালাসেমিয়ার রূপগুলিতেও বিদ্যমান।
- হিমোগ্লোবিন এস (α2 βS2 ) - হিমোগ্লোবিনের একটি ভিন্ন প্রকার যা সিকেল সেল রোগে আক্রান্ত ব্যক্তিদের মধ্যে পাওয়া যায়। β-চেন জিনে একটি ভিন্নতা রয়েছে, যা হিমোগ্লোবিনের বৈশিষ্ট্যে পরিবর্তন ঘটায়, যার ফলে লোহিত রক্তকণিকা সিকেল রোগে আক্রান্ত হয়ে পড়ে।
- হিমোগ্লোবিন সি (α2βC2) - β-চেন জিনের ভিন্নতার কারণে সৃষ্ট হিমোগ্লোবিনের আরেকটি রূপ। এই রূপটি একটি হালকা দীর্ঘস্থায়ী হেমোলাইটিক অ্যানিমিয়া রোগের সৃষ্টি করে।
- হিমোগ্লোবিন ই (α2βE2 ) - β-চেন জিনের ভিন্নতার কারণে সৃষ্ট আরেকটি রূপ। এই রূপটিও একটি হালকা দীর্ঘস্থায়ী হেমোলাইটিক অ্যানিমিয়া সৃষ্টি করতে সক্ষম হয়।
- হিমোগ্লোবিন AS - একটি ভিন্নধর্মী রূপ যা একটি প্রাপ্তবয়স্ক জিন এবং একটি সিকেল সেল ডিজিজ জিনের সাথে সিকেল সেল বৈশিষ্ট্য সৃষ্টি করে।
- হিমোগ্লোবিন SC ডিজিজ - একটি সিকেল জিন এবং আরেকটি এনকোডিং হিমোগ্লোবিন সি সহ একটি যৌগিক ভিন্নধর্মী প্রকার।
- হিমোগ্লোবিন হপকিন্স-২ – হিমোগ্লোবিনের একটি ভিন্ন রূপ যা কখনও কখনও হিমোগ্লোবিন এস এর সাথে সিকেল সেল রোগ তৈরি করতে দেখা যায়।
মেরুদণ্ডী প্রাণীদের মধ্যে অবনতি
[সম্পাদনা]লোহিত রক্ত কণিকা যখন বার্ধক্য বা কোনো ত্রুটির কারণে তাদের জীবনচক্রর শেষ দশায় পৌঁছায়, তখন প্লীহা বা লিভার বা রক্ত সঞ্চালনের মধ্যে হেমোলাইজ দশা থেকে ম্যাক্রোফেজের ফ্যাগোসাইটিক কার্যকলাপ দ্বারা তারা নিষ্কাশিত হয়। তারপরেই মুক্ত হিমোগ্লোবিন, রক্ত সঞ্চালন থেকে নিষ্কাশন হয় হিমোগ্লোবিন ট্রান্সপোর্টার CD163 এর মাধ্যমে, যা কেবলমাত্র মনোসাইট বা ম্যাক্রোফেজে প্রকাশ পায়। এই কোষগুলির মধ্যে হিমোগ্লোবিন অণু ভেঙে যায় এবং লোহা পুনর্ব্যবহৃত হয়ে থাকে। এই প্রক্রিয়াটি ক্ষয়ে যাওয়া হিমের প্রতিটি অণুর জন্য কার্বন মনোক্সাইডের একটি অণু তৈরি করে। [৩] মানবদেহে কার্বন মনোক্সাইডের একমাত্র প্রাকৃতিক উৎস হল হিমের অবক্ষয়, এবং স্বাভাবিক বাতাসে শ্বাস নেওয়া মানুষের রক্তে কার্বন মনোক্সাইডের স্বাভাবিক মাত্রা বজায় রাখার ভূমিকাও পালন করে। [৪] হিম অবক্ষয়ে উৎপন্ন অন্য আরেকটি অবশিষ্ট যৌগ হল বিলিরুবিন। যদি লোহিত রক্তকণিকা স্বাভাবিকের তুলনায় দ্রুতহারে ধ্বংস হয়ে যায় তখন রক্তে এই বিলিরুবিন এর মাত্রা নির্ণয় করা হয়। অনুচিতভাবে হিমোগ্লোবিন প্রোটিন বা হিমোগ্লোবিন যা রক্তের কোষ থেকে খুব দ্রুত নিঃসৃত হচ্ছে তা ছোট রক্তনালী গুলিতে জমাট সৃষ্টি করতে পারে, বিশেষ করে কিডনির সূক্ষ্ম রক্তনালীতে যা কিডনির ক্ষতি করতে পারে। লোহা হিম থেকে বিচ্ছিন্ন হয়ে পরবর্তীতে ব্যবহারের জন্য সঞ্চয় হয়, যা কোষে হিমোসিডারিন বা ফেরিটিন হিসাবে সংরক্ষণ করা হয় এবং ট্রান্সফারিন হিসাবে বিটা গ্লোবিউলিন দ্বারা প্লাজমাতে পরিবাহিত হয়।যখন পোরফাইরিন রিংটি ভেঙে যায়, তখন টুকরোগুলি সাধারণত বিলিরুবিন নামে একটি হলুদ রঁজক পদার্থ নিঃসৃত করে, যা পিত্ত রস নামে অন্ত্রে নিঃসৃত হয়। অন্ত্রগুলি বিলিরুবিনকে ইউরোবিলিনোজেনে বিপাক করে। ইউরোবিলিনোজেন স্টেরকোবিলিন নামক রঞ্জক পদার্থে মিশে মল-মূত্রের মাধ্যমে শরীর থেকে নির্গত হয়। গ্লোবিউলিন অ্যামিনো অ্যাসিডে বিপাকিত হয় এবং পরে এই সঞ্চালনে মুক্ত হয়।
তথ্যসূত্র
[সম্পাদনা]- ↑ Huisman THJ (১৯৯৬)। "A Syllabus of Human Hemoglobin Variants"। Globin Gene Server। Pennsylvania State University। ২০০৮-১২-১১ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০০৮-১০-১২।
- ↑ "Hemoglobin Variants"। Lab Tests Online। American Association for Clinical Chemistry। ২০০৭-১১-১০। ২০০৮-০৯-২০ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০০৮-১০-১২।
- ↑ Kikuchi, G.; Yoshida, T. (২০০৫)। "Heme oxygenase and heme degradation": 558–67। ডিওআই:10.1016/j.bbrc.2005.08.020। পিএমআইডি 16115609।
- ↑ Coomes, Marguerite W. (২০১১)। "Amino Acid and Heme Metabolism"। Textbook of Biochemistry: With Clinical Correlations (7th সংস্করণ)। John Wiley & Sons। পৃষ্ঠা 797। আইএসবিএন 978-0-470-28173-4।
