হাইড্রোজেন বন্ধন

হাইড্রোজেন বন্ধন হল একধরনের তড়িদাকর্ষণ বল যাতে হাইড্রোজেন পরমাণু ও অধিক তড়িৎ ঋণাত্মকতা বিশিষ্ট ছোট আকারের পরমাণু অংশ নেয় (যেমন – N, F, O)। ফলে H পরমাণুর ইলেকট্রন মেঘের ঘনত্ব অধিক হ্রাস পায়। এরুপ পোলার অণুসমূহের মধ্যে ধনাত্মক ও ঋণাত্মক তড়িদাকর্ষণ বল সৃষ্টি হয়, তাকেই হাইড্রোজেন বন্ধন বলে।অর্থাৎ, এক বা ততোধিক পোলার যৌগের অণুতে পোলারত্বের কারণে সৃষ্ট বন্ধন হল হাইড্রোজেন বন্ধন।[১] এটি DNA এ N2 বেসের মধ্যেও থাকে। পানিও এই বন্ধন এ যুক্ত। এই বন্ধনই পানির উচ্চ স্ফুটনাংক এর জন্য দায়ী।
২০১১ সালে IUPAC এই বন্ধন এর সংজ্ঞা দেয়- হাইড্রোজেন বন্ধন হল হাইড্রোজেন এর সাথে অন্য মৌলের বন্ধন যখন সেখানে হাইড্রোজেনের চেয়ে বেশি তড়িৎ ঋনাত্মক মৌল থাকে।
ইতিহাস
[সম্পাদনা]The Nature of Chemical Bond বইটিতে প্রথম লিনাস পলিংগ এবং মুর ও ওইনমিল ১৯১২ সালে প্রথম এর সম্পর্কে ধারণা দেন। তারা দেখেন ট্রাইমিথাইলঅ্যামোনিয়াম হাইড্রোক্সাইড এর গঠন টেট্রামিথাইলঅ্যামোনিয়াম হাইড্রোক্সাইড এর চেয়ে দুর্বল। এটাই H-bond এর প্রকৃত উদাহরণ। লাটিমার এবং রডেবাশ এর সম্বন্ধে সম্পূর্ণ ধারণা দেন।
প্রকারভেদ
[সম্পাদনা]দুই প্রকারের হাইড্রোজেন বন্ধন দেখা যায়:
- আন্তঃআণবিক হাইড্রোজেন বন্ধন
- অন্তঃআণবিক হাইড্রোজেন বন্ধন
আন্তঃআণবিক হাইড্রোজেন বন্ধন
[সম্পাদনা]আন্তঃআণবিক হাইড্রোজেন বন্ধন (Intermolecular H-bond) হল একই বা ভিন্ন পদার্থের ভিন্ন অণুর মধ্যে গঠিত হাইড্রোজেন বন্ধন। যেমন – জল (H2O), অ্যামোনিয়া (NH3), হাইড্রোজেন ফ্লোরাইড (HF) ইত্যাদি। এগুলি খুব বড় বড় চেইন তৈরীর মাধ্যমে বৃহদাকৃতি অণুসমষ্টি সৃষ্টি করে।
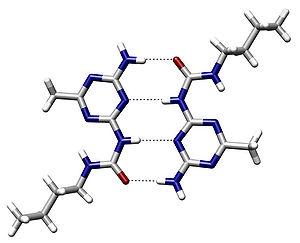
অন্তঃআণবিক হাইড্রোজেন বন্ধন
[সম্পাদনা]অন্তঃআণবিক হাইড্রোজেন বন্ধন (Intramolecular H-bond) হল একই অণুর ভিন্ন দুটি পরমাণুর মধ্যে গঠিত হাইড্রোজেন বন্ধন। যেমন – অর্থো-নাইট্রোফেনল, অর্থো-ক্লোরোফেনল ইত্যাদি। মূলত একটি বেঞ্জিন যৌগের দুটি সন্নিহিত কার্বন সংলগ্ন হাইড্রোজেন অপসারণ করার পর যুক্ত গ্রুপগুলি এই বন্ধন সৃষ্টি করে।

পানিতে হাইড্রোজেন বন্ধন
[সম্পাদনা]হাইড্রোজেন উচ্চ তড়িৎ ঋনাত্মক মৌল অক্সিজেন এর সাথে যুক্ত হয়ে পানি তৈরি করে এবং এদের মধ্যে পোলারিটি তৈরি হয়। এভাবে সৃষ্টি পোলার অণু সমূহ যখন পরস্পরের কাছে আসে তখন একটির ধনাত্মক প্রান্ত অপরটির ঋনাত্মক প্রান্তের সাথে দুর্বল বন্ধন গঠন করে। একে (----) দ্বারা বোঝানো হয়। অন্যান্য মৌলরাও এইভাবে হাইড্রোজেন বন্ধন গঠন করে।
বরফের ক্ষেত্রে অক্সিজেন পরমাণুর চারপাশে হাইড্রোজেন চতুস্তলকীয় আকারে সজ্জিত থাকে ও প্রচুর ফাঁকা স্থান পরে থাকে। তাই জলের চেয়ে বরফের ঘনত্ব কম।
ডিএনএ তে হাইড্রোজেন বন্ধন
[সম্পাদনা]

ডি এন এ তে একটি N2 base অন্য একটি base এর সাথে হাইড্রোজেন বন্ধন গঠন করে।যেমন Adenin-thimin Guanin-cytosin
তথ্যসূত্র
[সম্পাদনা]- ↑ Weinhold, Frank; Klein, Roger A. (২০১৪)। "What is a hydrogen bond? Resonance covalency in the supramolecular domain"। Chemistry Education Research and Practice। 15: 276–285। ডিওআই:10.1039/c4rp00030g।
- ↑ Beijer, Felix H.; Kooijman, Huub; Spek, Anthony L.; Sijbesma, Rint P.; Meijer, E. W. (১৯৯৮)। "Self-Complementarity Achieved through Quadruple Hydrogen Bonding"। Angew. Chem. Int. Ed.। 37 (1–2): 75–78। ডিওআই:10.1002/(SICI)1521-3773(19980202)37:1/2<75::AID-ANIE75>3.0.CO;2-R।
আরও পড়ুন
[সম্পাদনা]- George A. Jeffrey. An Introduction to Hydrogen Bonding (Topics in Physical Chemistry). Oxford University Press, USA (March 13, 1997). আইএসবিএন ০-১৯-৫০৯৫৪৯-৯
বহিঃসংযোগ
[সম্পাদনা]- The Bubble Wall (Audio slideshow from the National High Magnetic Field Laboratory explaining cohesion, surface tension and hydrogen bonds)
- isotopic effect on bond dynamics
