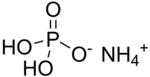
অ্যামোনিয়াম ডাইহাইড্রোজেন ফসফেট

| |
| |

| |
| নামসমূহ | |
|---|---|
| ইউপ্যাক নাম
অ্যামোনিয়াম ডাইহাইড্রোজেন ফসফেট
| |
| অন্যান্য নাম
মনোঅ্যামোনিয়াম ফসফেট
| |
| শনাক্তকারী | |
ত্রিমাত্রিক মডেল (জেমল)
|
|
| সিএইচইবিআই | |
| কেমস্পাইডার | |
| ইসিএইচএ ইনফোকার্ড | ১০০.০২৮.৮৭৭ |
| ইসি-নম্বর |
|
| ই নম্বর | E৩৪২(i) (অ্যান্টিঅক্সিডেন্ট, ...) |
পাবকেম CID
|
|
| ইউএনআইআই | |
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|
| |
| |
| বৈশিষ্ট্য | |
| H6NO4P | |
| আণবিক ভর | ১১৫.০২ g·mol−১ |
| বর্ণ | সাদা স্ফটিকস্বরূপ |
| গন্ধ | নেই |
| ঘনত্ব | ১.৮ গ্রা/সেমি৩ |
| গলনাঙ্ক | ১৯০ °সে (৩৭৪ °ফা; ৪৬৩ K) |
| (গ্রা/ডিএল) ২৮ (১০ °সে) ৩৬ (২০ °সে) ৪৪ (৩০ °সে) 56 (৪০ °সে) ৬৬ (৫০ °সে) ৮১ (৬০ °সে) ৯৯ (৭০ °সে) ১১৮ (৮০ °সে) ১৭৩ (১০০ °সে)[২][৩] | |
| দ্রাব্যতা | ইথানলে অদ্রবণীয়[২] অ্যাসিটোনে অদ্রবণীয় |
| প্রতিসরাঙ্ক (nD) | ১.৫২৫ |
| গঠন | |
| স্ফটিক গঠন | টেট্রাগোনাল |
| তাপ রসায়নবিদ্যা | |
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
−১৪৪৫.০৭ কিলোজুল/মোল[৪] |
| ঝুঁকি প্রবণতা | |
| জিএইচএস চিত্রলিপি | 
|
| জিএইচএস সাংকেতিক শব্দ | সতর্কতা |
| জিএইচএস বিপত্তি বিবৃতি | H319 |
| জিএইচএস সতর্কতামূলক বিবৃতি | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405 |
| এনএফপিএ ৭০৪ | |
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |
LD৫০ (মধ্যমা ডোজ)
|
৫৭৫০ মিগ্রা/কেজি (rat, oral) |
| সম্পর্কিত যৌগ | |
অন্যান্য অ্যানায়নসমূহ
|
অ্যামোনিয়াম ফসফেট ডাইঅ্যামোনিয়াম ফসফেট |
অন্যান্য ক্যাটায়নসমূহ
|
মনোসোডিয়াম ফসফেট পটাশিয়াম ডাইহাইড্রোজেন ফসফেট |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |
অ্যামোনিয়াম ডাইহাইড্রোজেন ফসফেট (এডিপি) একটি রাসায়নিক যৌগ। এটি মনোঅ্যামোনিয়াম ফসফেট ( এমএপি ) নামেও পরিচিত।[৫] এটির রাসায়নিক সংকেত (NH4)(H2PO4)। এটি কৃষি সার[৬] এবং শুষ্ক রাসায়নিক অগ্নি নির্বাপক যন্ত্রের একটি প্রধান উপাদান। আলোকবিদ্যা [৭] এবং ইলেকট্রনিক্সেও এর উল্লেখযোগ্য ব্যবহার রয়েছে। [৮]
রাসায়নিক বৈশিষ্ট্য[সম্পাদনা]
মনোঅ্যামোনিয়াম ফসফেট পানিতে দ্রবণীয় এবং এটি থেকে টেট্রাগোনাল পদ্ধতিতে অ্যানহাইড্রাস লবণ হিসাবে দীর্ঘায়িত প্রিজম বা সূঁচ হিসাবে স্ফটিক করে।[৭] এটি ইথানলে কার্যত অদ্রবণীয়।[২]
কঠিন মনোঅ্যামোনিয়াম ফসফেটকে পরীক্ষণে ২০০ ডিগ্রি সেলসিয়াস তাপমাত্রা পর্যন্ত স্থিতিশীল হিসাবে বিবেচনা করা যেতে পারে। এটি বিয়োজিত হয়ে অ্যামোনিয়া NH
3 এবং গলিত ফসফরিক এসিড H
3PO
4 উৎপন্ন হয়।
[৯] ১২৫ °সে এ অ্যামোনিয়ার আংশিক চাপ ০.০৫ মিমি পারদ হয়।[১০]
স্টকিয়মেট্রিক মনোঅ্যামোনিয়াম ফসফেটের দ্রবণ হল অম্লীয় (পিএইচ ৪.৭, ০.১% ঘনত্বে, ৪.২ এ ৫%)।[১১]
প্রস্তুতি[সম্পাদনা]
মনোঅ্যামোনিয়াম ফসফেট সঠিক অনুপাতে ফসফরিক অ্যাসিড এবং অ্যামোনিয়ার তাপোৎপাদী বিক্রিয়া দ্বারা শিল্পে প্রস্তুত করা হয়: [১২]
NH
3 + H
3PO
4 → NH
4H
2PO
4
অবস্থান[সম্পাদনা]
যৌগটি প্রকৃতিতে বিরল খনিজ বাইফসফামাইট হিসাবে উপস্থিত রয়েছে।
ব্যবহার[সম্পাদনা]
কৃষি[সম্পাদনা]
মনোঅ্যামোনিয়াম ফসফেটের সবচেয়ে বেশি ব্যবহার কৃষিতে, সারের উপাদান হিসাবে। এটি হতে উদ্ভিদ ব্যবহারযোগ্য আকারে নাইট্রোজেন এবং ফসফরাস মাটি হতে শোষণ করে। এর এনপিকে লেবেল হলো ১২-৬১-০ (১২-২৭-০), যার অর্থ এটিতে মৌলিক নাইট্রোজেন ১২% এবং ফসফরাস পেন্টক্সাইড P
2O
5 ৬১% বা মৌলিক ফসফরাস ২৭% বিদ্যমান।
অগ্নি নির্বাপক[সম্পাদনা]
যৌগটি কিছু শুকনো রাসায়নিক অগ্নি নির্বাপক যন্ত্রে এবিসি পাউডারের একটি উপাদান।
আলোকবিজ্ঞান[সম্পাদনা]
মনোঅ্যামোনিয়াম ফসফেট তার বায়ারফ্রিঞ্জেন্স বৈশিষ্ট্যের কারণে অপটিক্সের ক্ষেত্রে একটি বহুল ব্যবহৃত স্ফটিক। এর টেট্রাগোনাল স্ফটিক গঠনের ফলে, এই উপাদানটির নেতিবাচক অক্ষীয় অপটিক্যাল প্রতিসাম্য রয়েছে। এটির সাধারণত অপটিক্যাল তরঙ্গদৈর্ঘ্যে no = 1.522 এবং ne = 1.478 প্রতিসরাঙ্ক রয়েছে। [৭]
ইলেকট্রনিক্স[সম্পাদনা]
মনোঅ্যামোনিয়াম ফসফেট স্ফটিকগুলি পাইজোইলেক্ট্রিক, কিছু সক্রিয় সোনার (SONAR) ট্রান্সডুসারের জন্য প্রয়োজনীয় একটি বৈশিষ্ট্য। ১৯৫০-এর দশকে এডিপি স্ফটিকগুলি মূলত ট্রান্সডিউসারগুলিতে কোয়ার্টজ এবং রোচেল সল্ট স্ফটিকগুলির পরিবর্তে ব্যবহার শুরু হয়েছিল। [৮]
খেলনা[সম্পাদনা]
তুলনামূলকভাবে বিষাক্ত নয় বলে এমএপি বিনোদন মূলক ব্যবহারের ক্ষেত্রে জনপ্রিয় পদার্থ। এটি বিভিন্ন রঙের রঞ্জক মিশ্রিত খেলনা কিট হিসাবে বিক্রি করা হয়।
তথ্যসূত্র[সম্পাদনা]
- ↑ Lide, David R. (১৯৯৮)। Handbook of Chemistry and Physics (87 সংস্করণ)। Boca Raton, Florida: CRC Press। পৃষ্ঠা 4–40। আইএসবিএন 0-8493-0594-2।
- ↑ ক খ গ Dejun Xu, Xing Xiong, Lin Yang, Zhiye Zhang, and Xinlong Wang (2016): "Determination of the Solubility of Ammonium Dihydrogen Phosphate in Water-Ethanol System at Different Temperatures from 283.2 to 343.2 K".
- ↑ Chemical Book: "Ammonium dihydrogen phosphate". Accessed on 2018-08-14.
- ↑ National Bureau of Standards. Selected Values of Chemical Thermodynamic Properties. Technical note 270-3. 1968 [১]
- ↑ "Monoammonium Phosphate (MAP)" (পিডিএফ)। www.mosaicco.com। ১৭ নভেম্বর ২০১৫ তারিখে মূল (পিডিএফ) থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০১৫-০৬-০৫।
- ↑ IPNI। "Monoammonium Phosphate (MAP)" (পিডিএফ)। www.ipni.net। International Plant Nutrition Institute। সংগ্রহের তারিখ ২১ জুলাই ২০১৪।
- ↑ ক খ গ Amnon Yariv, Pochi Yeh (১৯৮৪)। Optical Waves in Crystals। Wiley, Inc।
- ↑ ক খ Willem Hackmann (১৯৮৪)। Seek and Strike: Sonar, Anti-Submarine Warfare and the Royal Navy, 1914–1954। Her Majesty's Stationery Office। আইএসবিএন 0-11-290423-8।
- ↑ G. O. Guerrant and D. E. Brown (196): "Thermal Decomposition of High-Analysis Fertilizers Based on Ammonium Phosphate".
- ↑ John R Van Wazer (১৯৫৮)। Phosphorus And Its Compounds - Volume I: Chemistry। Interscience Publishers, Inc। পৃষ্ঠা 503।
- ↑ Haifa Chemicals Ltd.: "Mono-Ammonium Phosphate 12-61-0".
- ↑ Martin Bäckman, Martin Gunnarsson, Linnea Kollberg, Martin Müller, and Simon Tallvod (2016): "Production of Monoammonium Phosphate at Yara AB ওয়েব্যাক মেশিনে আর্কাইভকৃত ১৮ নভেম্বর ২০১৭ তারিখে".

