অ্যাসিটোন
| |||
| |||

| |||
| নামসমূহ | |||
|---|---|---|---|
| ইউপ্যাক নাম
Acetone[৬]
| |||
| পছন্দসই ইউপ্যাক নাম
Propan-2-one[৭] | |||
| অন্যান্য নাম | |||
| শনাক্তকারী | |||
ত্রিমাত্রিক মডেল (জেমল)
|
|||
| থ্রিডিমেট | |||
| বেইলস্টেইন রেফারেন্স | 635680 | ||
| সিএইচইবিআই | |||
| সিএইচইএমবিএল | |||
| কেমস্পাইডার | |||
| ইসিএইচএ ইনফোকার্ড | ১০০.০০০.৬০২ | ||
| ইসি-নম্বর |
| ||
| মেলিন রেফারেন্স | 1466 | ||
| কেইজিজি | |||
| এমইএসএইচ | Acetone | ||
পাবকেম CID
|
|||
| আরটিইসিএস নম্বর |
| ||
| ইউএনআইআই | |||
| ইউএন নম্বর | 1090 | ||
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|||
| |||
| |||
| বৈশিষ্ট্য | |||
| C3H6O | |||
| আণবিক ভর | ৫৮.০৮ g·mol−১ | ||
| বর্ণ | Colourless liquid | ||
| গন্ধ | Pungent, irritating, floral, cucumber like | ||
| ঘনত্ব | 0.7845 g/cm3 (25 °C) | ||
| গলনাঙ্ক | −৯৪.৭ °সে (−১৩৮.৫ °ফা; ১৭৮.৫ K)[১২] | ||
| স্ফুটনাঙ্ক | ৫৬.০৫ °সে (১৩২.৮৯ °ফা; ৩২৯.২০ K)[১২] | ||
| Miscible | |||
| দ্রাব্যতা | Miscible in benzene, diethyl ether, methanol, chloroform, ethanol[৮] | ||
| লগ পি | −0.16[৯] | ||
| বাষ্প চাপ |
| ||
| অম্লতা (pKa) | |||
| −33.78·10−6 cm3/mol | |||
| প্রতিসরাঙ্ক (nD) | 1.3588 (VD = 54.46) | ||
| সান্দ্রতা | 0.295 mPa·s (25 °C)[৮] | ||
| গঠন | |||
| Coordination geometry |
Trigonal planar at C2 | ||
| আণবিক আকৃতি | Dihedral at C2 | ||
| ডায়াপল মুহূর্ত | 2.91 D | ||
| তাপ রসায়নবিদ্যা | |||
| তাপ ধারকত্ব, C | 125.45 J/(mol·K) | ||
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
200.4 J/(mol·K) | ||
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
(−250.03) – (−248.77) kJ/mol | ||
| দহনে প্রমান এনথ্যাল্পির পরিবর্তন ΔcH |
−1.772 MJ/mol | ||
| ঝুঁকি প্রবণতা | |||
| জিএইচএস চিত্রলিপি |  
| ||
| জিএইচএস সাংকেতিক শব্দ | বিপদজনক | ||
| জিএইচএস বিপত্তি বিবৃতি | H225, H319, H336, H373 | ||
| জিএইচএস সতর্কতামূলক বিবৃতি | P210, P235, P260, P305+351+338 | ||
| এনএফপিএ ৭০৪ | |||
| ফ্ল্যাশ পয়েন্ট | −২০ °সে (−৪ °ফা; ২৫৩ K) | ||
| ৪৬৫ °সে (৮৬৯ °ফা; ৭৩৮ K) | |||
| বিস্ফোরক সীমা | 2.6–12.8%[১৩] | ||
| Threshold Limit Value | 1185 mg/m3 (TWA), 2375 mg/m3 (STEL) | ||
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |||
LD৫০ (মধ্যমা ডোজ)
|
| ||
LC৫০ (মধ্যমা একাগ্রতা)
|
20,702 ppm (rat, 8 h)[১৪] | ||
LCLo (সর্বনিম্ন প্রকাশিত)
|
45,455 ppm (mouse, 1 h)[১৪] | ||
| যুক্তরাষ্ট্রের স্বাস্থ্য অনাবৃতকরণ সীমা (NIOSH): | |||
PEL (অনুমোদনযোগ্য)
|
1000 ppm (2400 mg/m3)[৫] | ||
REL (সুপারিশকৃত)
|
TWA 250 ppm (590 mg/m3)[৫] | ||
IDLH (তাৎক্ষণিক বিপদ
|
2500 ppm[৫] | ||
| সম্পর্কিত যৌগ | |||
সম্পর্কিত যৌগ
|
|||
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |||
| তথ্যছক তথ্যসূত্র | |||
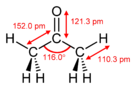
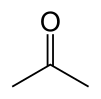
অ্যাসিটোন বা প্রোপানন একটি জৈব যৌগ, যার রাসায়নিক সংকেত (CH3)2CO।[১৫] এটি ক্ষুদ্রতম ও সরলতম কিটোন। এটি বর্ণহীন, অত্যন্ত উদ্বায়ী, দাহ্য এবং তীব্র গন্ধযুক্ত পদার্থ।
অ্যাসিটোন পানিতে সম্পূর্ণভাবে মিশে যায় এবং গুরুত্বপূর্ণ জৈব দ্রাবক বিবেচিত হয়। ২০১০ সালে ৬.৭ মিলিয়ন টন অ্যাসিটোন উৎপন্ন হয়েছিল। দ্রাবক হিসেবে ব্যবহার ছাড়াও মিথাইল মেথিক্রিলেট ও বিসফেনল এ তৈরিতেও অ্যাসিটোন ব্যবহার করা হয়। [১৬] নেইলপলিশ দূরীকারক এবং তুলি পাতলাকারকেও অ্যাসিটোনের ব্যবহার বিদ্যমান।
স্বাভাবিক বিপাকীয় প্রক্রিয়ায় মানবদেহেও অ্যাসিটোন উৎপন্ন হয়। রক্ত ও মূত্রে এটি অধিক পরিমাণে উপস্থিত। বহুমূত্র রোগীদের দেহ বিপুল পরিমাণে অ্যাসিটোন তৈরি করে থাকে। প্রজননসংক্রান্ত সমস্যার ক্ষেত্রে এটি খুব বেশি অসুবিধাজনক বিবেচিত হয় না। শিশুদের মৃগীরোগ প্রতিকারেও অ্যাসিটোন ব্যবহার করা হয়। [১৭]
ইতিহাস[সম্পাদনা]
১৬০৬ সালে সীসার(II) অ্যাসিটেট যৌগ হতে আন্দ্রিয়াস লিবাভিয়াস প্রথম অ্যাসিটোন উৎপাদন করেন। [১৮]
১৮৩২ সালে ফ্রেঞ্চ রসায়নবিদ জঁ ব্যাপটিস্ট ডুমা ও জার্মান রসায়নবিদ জুস্টুস ফন লিবিগ অ্যাাসিটোনের স্থূল সংকেত নির্ণয় করেন। [১৯] ১৮৩৩ সালে ফ্রেঞ্চ রসায়নবিদ আতোয়াঁ বুসি অ্যাসিটিক অ্যাসিডের অ্যাসিটোর সাথে ওন প্রত্যয় যুক্ত করে যৌগটির নাম দেন "অ্যাসিটোন।"[২০]১৮৫২ সালের দিকে ইংরেজ রসায়নবিদ আলেকজান্ডার উইলিয়াম উইলিয়ামসন উপলব্ধি করতে পারেন, অ্যাসিটোন প্রকৃতপক্ষে মিথাইল অ্যাসিটাইল। [২১]পরের বছর ফ্রেঞ্চ রসায়নবিদ শার্ল ফ্রেডরিক গের্দত তার সঙ্গে ঐকমত্য পোষণ করেন। ১৮৬৫ সালে জার্মান বিজ্ঞানী অগাস্ট কেকুলে অ্যাসিটোনের আধুনিক গাঠনিক সংকেত নির্ণয় করেন। [২২] ইয়োহান ইয়োসেফ লোশমিট ১৮৬১ সালে অ্যাসিটোনের গঠন নির্ণয় করেন। প্রথম বিশ্বযুদ্ধের সময় বিজ্ঞানী চাইম ওয়েজম্যান অ্যাসিটোনের বাণিজ্যিক উৎপাদনের পদ্ধতি নির্ণয় করেন। [২৩]
উৎপাদন[সম্পাদনা]
২০১০ সালে বিশ্বজুড়ে ৬.৭ মিলিয়ন অ্যাসিটোন উৎপন্ন হয়েছিল।[১৬] যুক্তরাষ্ট্রে পৃথিবীর সর্বোচ্চ পরিমাণ অ্যাসিটোন উৎপন্ন হয়েছিল, যার পরিমাণ ছিল ১.৫৬ মিলিয়ন টন।[২৪] তাইওয়ান ও চীন অ্যাসিটোন উৎপাদনে বিশ্বে যথাক্রমে দ্বিতীয় ও তৃতীয়। অ্যাসিটোন উৎপাদনকারী সর্ববৃহৎ প্রতিষ্ঠান আইএনইওএস ফেনল। বিশ্বের ১৭% অ্যাসিটোন-ই এ প্রতিষ্ঠান উৎপাদন করে থাকে। মিতসুই, সুনোকো ও শেল কোম্পানিও অ্যাসিটোন উৎপাদন করে। [১৬] বেলজিয়ামের বেভেরেন শহরে বিশ্বের সর্ববৃহৎ অ্যাসিটোন উৎপাদন কারখানা অবস্থিত। ২০১২ সালের গ্রীষ্মকালে যুক্তরাষ্ট্রে প্রতি টন অ্যাসিটোন ১১০০-১২৫০ ডলারে বিক্রি হয়।[২৫]
প্রোপিলিন থেকে প্রত্যক্ষ বা পরোক্ষভাবে অ্যাসিটোন উৎপাদন করা হয়। ক্যুমিন প্রক্রিয়ায় প্রায় ৮৩% অ্যাসিটোন প্রস্তুত করা হয়। [২৬] ফেনল-ও একই প্রক্রিয়ায় তৈরি করা হয়। ক্যুমিন প্রক্রিয়ায় বেনজিনকে প্রোপিলিনের সাথে ক্ষারকায়িত করা হয়। অতঃপর একে বায়ুতে জারিত করে ফেনল ও অ্যাসিটোন উৎপাদন করা হয়। একে বিক্রিয়ার সাহায্যে নিম্নরূপে দেখানো হলো:
ওয়েকার-হোয়েস্ট প্রক্রিয়ায় সরাসরি জারণ করেও অ্যাসিটোন উৎপাদন করা সম্ভব হয়। এছাড়াও প্রোপিলিনে পানি সংযোজন করে ২-প্রোপানল উৎপাদন করা যায়, যাকে জারিত করে অ্যাসিটোন প্রস্তুত করা সম্ভব হয়।
ইতোপূর্বে অ্যাসিটোনসমূহের শুষ্ক পরিস্রাবণ প্রক্রিয়ায় অ্যাসিটোন উৎপন্ন করা হতো। ক্যালসিয়াম অ্যাসিটেটের কিটোনিক ডিকার্বক্সিলেশন বিক্রিয়ায় পরিস্রাবণ এর অনন্য উদাহরণ:
Ca(CH3COO)2 → CaO(s) + CO2(g) + (CH3)2CO (v)
পরবর্তীতে Clostridium acetobutylicum থেকে অ্যাসিটোন-বিউটানল-ইথানল গাঁজন প্রক্রিয়ায় অ্যাসিটোন উৎপাদন করা হতো। চাইম ওয়াজম্যান (যিনি পরবর্তীতে ইসরায়েলের রাষ্ট্রপতি হন) ব্রিটিশদের যুদ্ধপ্রচেষ্টা বেগবান করার জন্য এ প্রক্রিয়া উদ্ভাবন করেন।
তথ্যসূত্র[সম্পাদনা]
- ↑ The Merck Index, 15th Ed. (2013), p. 13, Acetone Monograph 65, O'Neil: The Royal Society of Chemistry.টেমপ্লেট:Subscription needed
- ↑ ক খ গ ঘ Acetone in Linstrom, P.J.; Mallard, W.G. (eds.) NIST Chemistry WebBook, NIST Standard Reference Database Number 69. National Institute of Standards and Technology, Gaithersburg MD. http://webbook.nist.gov (retrieved 2014-05-11)
- ↑ Klamt, Andreas (২০০৫)। COSMO-RS: From Quantum Chemistry to Fluid Phase Thermodynamics and Drug Design। Elsevier। পৃষ্ঠা 92–94। আইএসবিএন 978-0-444-51994-8।
- ↑ Myers, Richard L. (২০০৭)। The 100 Most Important Chemical Compounds: A Reference Guide। Greenwood। পৃষ্ঠা 4–6। আইএসবিএন 978-0-313-08057-9।
- ↑ ক খ গ ঘ "NIOSH Pocket Guide to Chemical Hazards #0004" (ইংরেজি ভাষায়)। ন্যাশনাল ইনস্টিটিউট ফর অকুপেশনাল সেফটি অ্যান্ড হেলথ (NIOSH)।
- ↑ ChemSpider lists 'acetone' as a valid, expert-verified name for what would systematically be called 'propan-2-one'.
- ↑ Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book)। Cambridge: The Royal Society of Chemistry। ২০১৪। পৃষ্ঠা 723। আইএসবিএন 978-0-85404-182-4। ডিওআই:10.1039/9781849733069-FP001।
- ↑ ক খ Properties of substance: acetone. chemister.ru.
- ↑ "acetone"। ChemSrc। সংগ্রহের তারিখ ২০১৮-০৪-১৩।
- ↑ Chiang, Yvonne; Kresge, A. Jerry; Tang, Yui S.; Wirz, Jakob (১৯৮৪)। "The pKa and keto-enol equilibrium constant of acetone in aqueous solution"। Journal of the American Chemical Society। 106 (2): 460–462। ডিওআই:10.1021/ja00314a055।
- ↑ Bordwell, Frederick G. (১৯৮৮)। "Equilibrium acidities in dimethyl sulfoxide solution"। Accounts of Chemical Research। 21 (12): 456–463। ডিওআই:10.1021/ar00156a004।
- ↑ ক খ Lide, David R. (ed) (2003). CRC Handbook of Chemistry and Physics, 84th Edition. CRC Press. Boca Raton, Florida; Section 3, Physical Constants of Organic Compounds.
- ↑ "Working with modern hydrocarbon and oxygenated solvents: a guide to flammability"। American Chemistry Council Solvents Industry Group। জানুয়ারি ২০০৮। পৃষ্ঠা 7। ২০০৯-০৬-০১ তারিখে মূল থেকে আর্কাইভ করা।
- ↑ ক খ গ "Acetone"। স্বাস্থ্য এবং জীবনের জন্য সহসা ঝুঁকিপূর্ণ। National Institute for Occupational Safety and Health (NIOSH)।
- ↑ Allen, P.W.; Bowen, H.J.M.; Sutton, L.E.; Bastiansen, O. (১৯৫২)। "The molecular structure of acetone"। Transactions of the Faraday Society। 48: 991। ডিওআই:10.1039/TF9524800991।
- ↑ ক খ গ "Global Chemical Market Solutions | IHS Markit"। ihsmarkit.com।
- ↑ Freeman, John M.; Kossoff, Eric H.; Hartman, Adam L. (1 মার্চ, 2007)। "The Ketogenic Diet: One Decade Later"। Pediatrics। 119 (3): 535–543। ডিওআই:10.1542/peds.2006-2447। পিএমআইডি 17332207 – pediatrics.aappublications.org-এর মাধ্যমে। এখানে তারিখের মান পরীক্ষা করুন:
|তারিখ=(সাহায্য) - ↑ LIBAVIUS, Andreas (21 অক্টোবর, 1606)। "Alchymiae"। Francfort : J. Saurius – Internet Archive-এর মাধ্যমে। এখানে তারিখের মান পরীক্ষা করুন:
|তারিখ=(সাহায্য) - ↑ "Annales de chimie et de physique"। Crochard। 21 অক্টোবর, 1832 – Google Books-এর মাধ্যমে। এখানে তারিখের মান পরীক্ষা করুন:
|তারিখ=(সাহায্য) - ↑ "Annales de chimie et de physique. ser.2:t.53 (1833)."। HathiTrust।
- ↑ Britain), Chemical Society (Great (21 অক্টোবর, 1852)। "Journal - Chemical Society, London"। Chemical Society. – Google Books-এর মাধ্যমে। এখানে তারিখের মান পরীক্ষা করুন:
|তারিখ=(সাহায্য) - ↑ "Bulletin de la Société chimique de Paris. 1865v.1 1865."। HathiTrust।
- ↑ "Chaim Weizmann - Chemistry Encyclopedia"।
- ↑ https://web.archive.org/web/20090515133058/http://www.icis.com/v2/chemicals/9074858/acetone/uses.html
- ↑ "সংরক্ষণাগারভুক্ত অনুলিপি"। ১৬ মে ২০১৩ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২১ অক্টোবর ২০২০।
- ↑ fStylianos Sifniades, Alan B. Levy, "Acetone" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005