ইথানল: সংশোধিত সংস্করণের মধ্যে পার্থক্য
| ৬০ নং লাইন: | ৬০ নং লাইন: | ||
:2 CH<sub>3</sub>CH<sub>2</sub>OH {{Unicode|→}} CH<sub>3</sub>CH<sub>2</sub>OCH<sub>2</sub>CH<sub>3</sub> + H<sub>2</sub>O (120 °C তাপমাত্রায়) |
:2 CH<sub>3</sub>CH<sub>2</sub>OH {{Unicode|→}} CH<sub>3</sub>CH<sub>2</sub>OCH<sub>2</sub>CH<sub>3</sub> + H<sub>2</sub>O (120 °C তাপমাত্রায়) |
||
===দহন=== |
===দহন=== |
||
ইথানলের পূর্ণ দহনে কার্বন ডাই অক্সাইড এবং পানি উৎপন্ন হয়: |
|||
:C<sub>2</sub>H<sub>5</sub>OH (l) + 3 O<sub>2</sub> (g) {{Unicode|→}} 2 CO<sub>2</sub> (g) + 3 H<sub>2</sub>O (liq); −ΔH<sub>c</sub> = 1371 kJ/mol<ref>{{cite journal|title=Heats of Formation of Simple Organic Molecules|author=Rossini, Frederick D. |journal=Ind. Eng. Chem.|year=1937|vo</ref> |
|||
==বিভিন্ন রকমের ইথানল== |
==বিভিন্ন রকমের ইথানল== |
||
২২:২১, ১২ জুলাই ২০১৪ তারিখে সংশোধিত সংস্করণ
| |||
| |||
| নামসমূহ | |||
|---|---|---|---|
| ইউপ্যাক নাম
ইথানল
| |||
| অন্যান্য নাম
ইথাইল অ্যালকোহল; গ্রেইন অ্যালকোহল; বিশুদ্ধ অ্যালকোহল; হাইড্রক্সিইথেন; পানীয় অ্যালকোহল; ইথাইল হাইড্রেট; অ্যাবসোলুট অ্যালকোহল; নির্জল অ্যালকোহল
| |||
| শনাক্তকারী | |||
ত্রিমাত্রিক মডেল (জেমল)
|
|||
| কেমস্পাইডার | |||
| ইসিএইচএ ইনফোকার্ড | ১০০.০০০.৫২৬ | ||
| ইসি-নম্বর | |||
পাবকেম CID
|
|||
| আরটিইসিএস নম্বর |
| ||
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|||
| |||
| |||
| বৈশিষ্ট্য | |||
| C2H6O | |||
| আণবিক ভর | ৪৬.০৭ g·mol−১ | ||
| বর্ণ | colorless liquid | ||
| ঘনত্ব | 0.789 g/cm3 | ||
| গলনাঙ্ক | −১১৪.৩ °সে (−১৭৩.৭ °ফা; ১৫৮.৮ K) | ||
| স্ফুটনাঙ্ক | ৭৮.৪ °সে (১৭৩.১ °ফা; ৩৫১.৫ K) | ||
| miscible | |||
| অম্লতা (pKa) | 15.9 | ||
| প্রতিসরাঙ্ক (nD) | 1.36 (25 °C) | ||
| সান্দ্রতা | 1.200 cP (1.200 mPa·s) (20 °C) | ||
| ডায়াপল মুহূর্ত | 1.69 D (gas) | ||
| ঝুঁকি প্রবণতা | |||
ইইউ শ্রেণীবিভাগ (ডিএসডি)
|
Flammable (F) | ||
| আর-বাক্যাংশ | আর১১ | ||
| এস-বাক্যাংশ | (এস২) এস৭ এস১৬ | ||
| এনএফপিএ ৭০৪ | |||
| ফ্ল্যাশ পয়েন্ট | 13 °C (55.4 °F) | ||
| সম্পর্কিত যৌগ | |||
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |||
| তথ্যছক তথ্যসূত্র | |||
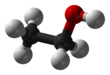
ইথানল, যা ইথাইল অ্যালকোহল নামেও পরিচিত, এক প্রকারের অ্যালকোহল। এটি দাহ্য, স্বাদবিহীন, বর্ণহীন, সামান্য বিষাক্ত ও বিশিষ্ট গন্ধযুক্ত, এবং অধিকাংশ মদ এর প্রধান উপাদান। এতে ৯৯% বিশুদ্ধ অ্যালকোহল থাকে। এটি জৈব সংশ্লেষণে ব্যবহৃত হয়। এর রাসায়নিক সংকেত হল CH3-CH2-OH, বা C2H6O, বা EtOH, C2H5OH বা C2H6O।
উৎস
প্রস্তুত প্রণালী
ইতিহাস
বিক্রিয়া
এলকোহলকে তিনভাগে ভাগ করা হয় । ইথানল প্রাইমারী এলকোহল। প্রাইমারী এলকোহল তাদের বলা হয় যাদের হাইড্রোক্সিল মূলক যুক্ত কার্বনের সাথে কমপক্ষে দুইটি হাইড্রোজেন যুক্ত থাকে। অধিকাংশ ইথানলের হাইড্রোক্সিল মূলক অংশে প্রধান বিক্রিয়া ঘটে।
এস্টার ফরমেশান
এসিড প্রভাবকের উপস্থিতিতে ইথানল কার্বক্সিলিক এসিডের সাথে বিক্রিয়া করে ইথাইল এস্টার এবং পানি তৈরী করে:
- RCOOH + HOCH2CH3 → RCOOCH2CH3 + H2O
শিল্প কারখানায় প্রস্তুত এস্টার থেকে পানি অপসারণ করা হয়। এস্টার এসিড অথবা ক্ষারের উপস্থিতিতে বিক্রিয়া করে পূণরায় এলকোহল ও লবন উৎপন্ন করে।এই বিক্রিয়াটি স্যাপোনিফিকেশান বা সাবানিকরণ বিক্রিয়া নামে পরিচিত। কারণ এই বিক্রিয়ার মাধ্যমে সাবান প্রস্তুত করা হয়। [১] অজৈব এসিডের সাথে ইথানল বিক্রিয়া করে এস্টার গঠন করে। সালফার ট্রাই অক্সাইড এবং ফসফরাস পেন্টাঅক্সাইডের সাথে ইথানলের বিক্রিয়ায় পর্যায়ক্রমে ডাই ইথাইল সালফেট এবং ট্রাই ইথাইল ফসফেট তৈরী হয়। অজৈব সংশ্লেষনে ডাই ইথাইল সালফেট উপকারী ইথাইলেটিং এজেন্ট হিসেবে কাজ করে। সোডিয়াম নাইট্রাইট এবং সালফিউরিক এসিডের সাথে ইথানলের বিক্রিয়ায় ইথাইল নাইট্রাইট উৎপন্ন হয় যা ডাই ইউরেটিক হিসেবে ব্যবহৃত হয়।
পানি বিয়োজন
শক্তিশালী এসিডের উপস্থিতিতে ইথানলের ডিহাইড্রেশান বা পানি বিয়োজন ঘটে। পানি বিয়োজিত হয়ে ইথানল ডাই ইথাইল ইথার এবং অন্যান্য উপজাত তৈরী করে। প্রতিবছর সালফিউরিক এসিড প্রভাবক হিসেবে ব্যবহার করে লক্ষ লক্ষ কেজি ডাই ইথাইল ইথার প্রস্তুত করা হয়:
- 2 CH3CH2OH → CH3CH2OCH2CH3 + H2O (120 °C তাপমাত্রায়)
দহন
ইথানলের পূর্ণ দহনে কার্বন ডাই অক্সাইড এবং পানি উৎপন্ন হয়:
- C2H5OH (l) + 3 O2 (g) → 2 CO2 (g) + 3 H2O (liq); −ΔHc = 1371 kJ/mol[২]
বিভিন্ন রকমের ইথানল
রেক্টিফায়েড স্পিরিট
৯৫.৪% ইথানল ও ৪.৬% পানির মিশ্রণ ।
মেথিলেটেড স্পিরিট
মদ, বিয়ার, হুইস্কি, ব্রান্ডি প্রভৃতি পানীয় ইথাইল এলকোহল হতে প্রস্তুত করা হয়। এ পানীয়সমহূল প্রকৃতপক্ষে ইথাইল এলকোহলের বিভিন্ন ঘনমাত্রার জলীয় দ্রবণ বিশেষ। এসকল পানীয়ের উপর প্রচুর আবগারী শুল্ক দিতে হয়। তাই এগুলো অত্যন্ত মহার্ঘ। অনেক সময় মাদকাসক্ত ব্যক্তিরা বাজার হতে সস্তা দামের ইথাইল এলকোহল কিনে এর সঙ্গে প্রয়োজন মত পানি মিশ্রিত করে দামী বাণিজ্যিক মদের বিকল্প হিসেবে পান করে। পানের কাজে এরূপ যথেচ্ছ ব্যবহারের ফলে ইথাইল এলকোহলের ঘাটতি পড়তে পারে। কারণ দ্রাবক এবং শিল্পজাত দ্রব্য উৎপাদনকাজে ইথাইল এলকোহল ব্যাপকভাবে ব্যবহৃত হয়। তাই পানীয় হিসেবে ইথাইলে এলকোহলের অনঅনুমোদিত ব্যবহার বন্ধে এর সাথে মিথানল, পিরিডিন, ন্যাপথা প্রভৃতি বিষাক্ত পদার্থ মিশিয়ে বাজারজাত করা হয়। বাণিজ্যিকভাবে এরূপ অ্যালকোহলকে মেথিলেটেড স্পিরিট, ডি ন্যাচারড অ্যালকোহল বা অসেবনীয় অ্যালকোহল নামে পরিচিত। এটি বিশেষভাবে রং-বার্ণিশের কাজে দ্রাবক হিসেবে ব্যবহার করা হয়।[৩]মেথিলেটেড স্পিরিটকে ইথানলের প্রকারভেদ হিসেবে গন্য করা হয়।
| রসায়ন বিষয়ক এই নিবন্ধটি অসম্পূর্ণ। আপনি চাইলে এটিকে সম্প্রসারিত করে উইকিপিডিয়াকে সাহায্য করতে পারেন। |
তথ্যসূত্র
- ↑ এস্টার ও ফ্যাটি এসিড সমূহের রসায়ন। উচ্চ মাধ্যমিক রসায়ন। দ্বিতীয় পত্র। সরোজ কান্তি সিংহ ও নাগ।
- ↑ {{cite journal|title=Heats of Formation of Simple Organic Molecules|author=Rossini, Frederick D. |journal=Ind. Eng. Chem.|year=1937|vo
- ↑ উচ্চ মাধ্যমিক রসায়ন, দ্বিতীয় পত্র। অধ্যায়ঃ২৪, এলকোহল, ফেনল ও ইথারসমহুহ। ৩০৭ পৃষ্ঠা। লেখকঃ ড. রবিউল ইসলাম, ড. গাজী মোঃ আহসানুল কবীর, ডঃ মনিমুল হক। ৬ষ্ঠ সংস্করণ, জুন ২০০৪ । প্রথম প্রকাশ মার্চ ১৯৯৯।