গ্লাইকোলিপিড
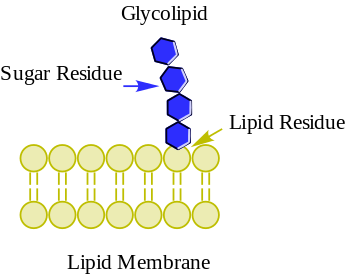
গ্লাইকোলিপিড হলো এক ধরণের লিপিড যার সাথে কার্বোহাইড্রেট যুক্ত থাকে। কার্বোহাইড্রেট লিপিডের সাথে গ্লাইকোসিডিক বন্ধন দ্বারা সংযুক্ত থাকে।[১] গ্লাইকোলিপিড কোষের ঝিল্লি তে গুরুত্বপূর্ণ ভূমিকা পালন করে। গ্লাইকোলিপিড কোষের ঝিল্লির কাঠামোগত স্থিতিশীলতা বজায় রাখতে সাহায্য করে।[২] গ্লাইকোলিপিড কোষের পৃষ্ঠে অ্যান্টিজেন হিসেবে কাজ করে। কোষ-থেকে-কোষে যোগাযোগ, টিস্যু গঠন এবং প্রতিরোধ ব্যবস্থার জন্য কোষীয় সনাক্তকরণ অপরিহার্য। কিছু গ্লাইকোলিপিড কোষ সংকেতের প্রক্রিয়ায় জড়িত। গ্লাইকোলিপিড রোগ প্রতিরোধ ব্যবস্থার জন্য গুরুত্বপূর্ণ। এগুলো অ্যান্টিবডি এবং অন্যান্য প্রতিরোধ ব্যবস্থার কোষগুলোকে বাইরের আক্রমণকারীদের সনাক্ত করতে সাহায্য করে।[৩] গ্লাইকোলিপিড সকল ইউক্যারিওটিক কোষের ঝিল্লির বাইরের পৃষ্ঠে (প্লাজমা ঝিল্লি) অবস্থিত থাকে।[৪]
কাঠামো[সম্পাদনা]
গ্লাইকোলিপিড হলো একধরনের চর্বি যার সাথে শর্করা যুক্ত থাকে। এই শর্করা একক অণু (মনোস্যাকারাইড) অথবা একাধিক অণুর (অলিগোস্যাকারাইড) সমন্বয়ে গঠিত হতে পারে। এটি গ্লাইকোলিপিডকে অনন্য করে তোলে।
কোষের ঝিল্লিতে দুই ধরনের প্রধান চর্বি পাওয়া যায়: গ্লিসারোলিপিড এবং স্ফিঙ্গোলিপিড।
- গ্লিসারোলিপিড: এই চর্বির মূল কাঠামোটি গ্লিসারল নামক একটি অণু দিয়ে তৈরি।
- স্ফিঙ্গোলিপিড: এই চর্বির মূল কাঠামোটি স্ফিঙ্গোসিন নামক একটি অণু দিয়ে তৈরি।
এই মূল কাঠামোর সাথে ফ্যাটি এসিড যুক্ত থাকে। ফলে, চর্বির অণুর মস্তক অংশটি মেরুকৃত (পানি-আকর্ষণকারী) এবং লেজ অংশটি অমেরুকৃত (পানি-বিকর্ষণকারী) হয়। কোষের ঝিল্লি দুই স্তর চর্বি দিয়ে তৈরি, আর এই দুই স্তরেই মাথা অংশ ঝিল্লির ভিতরে ও বাইরে থাকে এবং লেজ অংশ ঝিল্লির মাঝখানে অবস্থান করে। সুতরাং, গ্লাইকোলিপিডগুলো কোষের ঝিল্লিতে একটি বিশেষ ভূমিকা পালন করে। এগুলি ঝিল্লির কাঠামো ও কার্যকলাপে গুরুত্বপূর্ণ এবং কোষের সাথে অন্যান্য কোষ ও পরিবেশের সাথে যোগাযোগে সহায়তা করে।
কোষের ঝিল্লীর বাইরের দিকে মেরুকৃত মাথা অংশে লেগে থাকা শর্করা গ্লাইকোলিপিডের লিগ্যান্ড উপাদান হিসেবে কাজ করে। এই শর্করাগুলোও মেরুকৃত, ফলে কোষের চারপাশে থাকা জলীয় পরিবেশে দ্রবীভূত হতে পারে।[৫] চর্বি ও শর্করা একটি গ্লাইকোসাইডিক বন্ধন দ্বারা যুক্ত হয়ে একটি গ্লাইকোকনজুগেট তৈরি করে। এই বন্ধন একটি সমযোজী বন্ধন, যা খুবই শক্তিশালী। শর্করার অ্যানোমেরিক কার্বন লিপিড কাঠামোর একটি মুক্ত হাইড্রক্সিল গ্রুপের সাথে যুক্ত হয়। এই শর্করাগুলোর কাঠামো সেই অণুর কাঠামোর উপর নির্ভর করে যার সাথে এগুলো আবদ্ধ হয়। অর্থাৎ, কোষের সাথে যোগাযোগের ধরন নির্ধারণে এই শর্করাগুলোর বিভিন্ন রূপ গুরুত্বপূর্ণ ভূমিকা রাখে।
বিপাক[সম্পাদনা]
শর্করা স্থানান্তরকারী এনজাইম (গ্লাইকোসিলট্রান্সফারেজ)[সম্পাদনা]
গ্লাইকোসিলট্রান্সফারেজ নামক এনজাইমগুলো শর্করা (স্যাকারাইড) অণুগুলোকে লিপিড অণুগুলোর সাথে যুক্ত করে। এছাড়াও, তারা সঠিক অলিগোস্যাকারাইড গঠনে গুরুত্বপূর্ণ ভূমিকা পালন করে, যাতে কোষের পৃষ্ঠে থাকা গ্লাইকোলিপিডের উপস্থিতি অনুভব করে কোষটি সঠিক রিসেপ্টর সক্রিয় করতে পারে এবং প্রতিক্রিয়া দেখাতে পারে। গ্লাইকোলিপিডগুলো গলজি বস্তুতে গঠিত হয় এবং একটি ভেসিকলের পৃষ্ঠে স্থাপন করা হয়, যা পরে কোষের ঝিল্লিতে পরিবহন করা হয়। ভেসিকেলটি কোষের ঝিল্লির সাথে মিশে যায়, যাতে গ্লাইকোলিপিডটি কোষের বাইরের পৃষ্ঠে উপস্থাপিত হতে পারে।[৬]
গ্লাইকোসাইড হাইড্রোলেজ এনজাইম[সম্পাদনা]
গ্লাইকোসাইড হাইড্রোলেজ হলো একধরনের এনজাইম যা গ্লাইকোসাইডিক বন্ধন ভেঙে দেয়। এই বন্ধনগুলো শর্করা অণুগুলোকে একে অপরের সাথে যুক্ত করে রাখে। গ্লাইকোলিপিড তৈরির পরে, এই এনজাইমগুলো গ্লাইক্যান নামক শর্করা অংশের কাঠামো পরিবর্তন করতে সাহায্য করে। এই পরিবর্তনগুলো কোষের সাথে যোগাযোগের মতো বিভিন্ন গুরুত্বপূর্ণ কাজে গ্লাইকোলিপিডকে সাহায্য করে। গ্লাইকোসাইড হাইড্রোলেজ এনজাইমগুলো গ্লাইকানগুলোকে সম্পূর্ণভাবে অপসারণ করতে পারে, যার ফলে গ্লাইকোলিপিডগুলো সাধারণ চর্বির মতো হয়ে যায়। এটি গ্লাইকোলিপিডের পরিমাণ নিয়ন্ত্রণে গুরুত্বপূর্ণ ভূমিকা পালন করে।[৭]
বিপাক-ত্রুটি[সম্পাদনা]
স্ফিঙ্গোলিপিডোজেস হলো এমন একধরনের রোগ যা সঠিকভাবে ভাঙা না যাওয়া স্ফিঙ্গোলিপিডের জমাট বাঁধার সাথে সম্পর্কিত। সাধারণত এটি গ্লাইকোসাইড হাইড্রোলেজ এনজাইমের ত্রুটির কারণে ঘটে। এই রোগগুলো সাধারণত বংশগত হয়। কোন এনজাইম ক্ষতিগ্রস্ত হয়েছে এবং কতটা ক্ষতিগ্রস্ত হয়েছে তার উপর নির্ভর করে এর প্রভাব ভিন্ন ভিন্ন হয়। এর একটি উল্লেখযোগ্য উদাহরণ হলো নিমান-পিক রোগ, যা ব্যথা সৃষ্টি ও স্নায়ুতন্ত্রের ক্ষতি করতে পারে।[৮]
কার্যক্রিয়া[সম্পাদনা]
কোষ-কোষ মিথস্ক্রিয়া[সম্পাদনা]
মানবদেহে গ্লাইকোলিপিডের প্রধান কাজ হল কোষ-কোষ মিথস্ক্রিয়ার জন্য স্বীকৃতি স্থান হিসেবে কাজ করা। একটি গ্লাইকোলিপিডের স্যাকারাইড প্রতিবেশী কোষের একটি নির্দিষ্ট পরিপূরক কার্বোহাইড্রেট বা লেকটিন (কার্বোহাইড্রেট-বাঁধনকারী প্রোটিন) এর সাথে আবদ্ধ হবে। এই কোষের পৃষ্ঠের চিহ্নিতকারীদের মিথস্ক্রিয়া কোষের স্বীকৃতির ভিত্তি এবং সেলুলার প্রতিক্রিয়া শুরু করে যা নিয়ন্ত্রণ, বৃদ্ধি এবং কোষপতনের মতো কার্যকলাপে অবদান রাখে।[৯]
রোগপ্রতিরোধ প্রতিক্রিয়া[সম্পাদনা]
গ্লাইকোলিপিড শরীরে কিভাবে কাজ করে তার একটি উদাহরণ হোল প্রদাহের সময় শ্বেতকণিকা এবং এন্ডোথেলিয়াল কোষের মধ্যকার মিথস্ক্রিয়া। লিউকোসাইট (শ্বেতকণিকা) এবং এন্ডোথেলিয়াল কোষের পৃষ্ঠে পাওয়া এক ধরনের লেকটিন, সিলেক্টিন, রোগ প্রতিরোধ ব্যবস্থা তৈরি করতে গ্লাইকোলিপিডের সাথে সংযুক্ত কার্বোহাইড্রেটের সাথে বন্ধন তৈরি করে। এই বন্ধন লিউকোসাইটকে রক্তনালী থেকে বের হয়ে প্রদাহের স্থানের কাছে জমা হতে বাধ্য করে। এটি প্রাথমিক বন্ধন প্রক্রিয়া, এর পরে ইন্টিগ্রিন নামক অণু প্রকাশিত হয়, যা শক্তিশালী বন্ধন তৈরি করে এবং লিউকোসাইটকে প্রদাহের স্থানে অভিবাসনে সহায়তা করে।[১০] গ্লাইকোলিপিডগুলো অন্যান্য প্রতিক্রিয়া, বিশেষ করে ভাইরাস দ্বারা হোস্ট কোষের সনাক্তকরণের জন্যও দায়ী।[১১]
রক্তের গ্রুপ[সম্পাদনা]
রক্তের গ্রুপ নির্ধারণ করা হয় লোহিত রক্তকণিকার পৃষ্ঠে থাকা অ্যান্টিজেন নামক কিছু জৈব অণুর উপস্থিতি বা অনুপস্থিতির উপর। এই অ্যান্টিজেনগুলো শরীরের রোগ প্রতিরোধ ব্যবস্থাকে সাহায্য করে বাহিরের কোষকে চিহ্নিত করতে।
চারটি প্রধান রক্তের গ্রুপ রয়েছে:
- A: লাল রক্তকণিকার পৃষ্ঠে A অ্যান্টিজেন থাকে।
- B: লাল রক্তকণিকার পৃষ্ঠে B অ্যান্টিজেন থাকে।
- AB: লাল রক্তকণিকার পৃষ্ঠে A এবং B উভয় অ্যান্টিজেন থাকে।
- O: লাল রক্তকণিকার পৃষ্ঠে A বা B অ্যান্টিজেন থাকে না।
অ্যান্টিবডি:
রক্তের প্লাজমাতে অ্যান্টিবডি নামক কিছু প্রোটিন থাকে যা অ্যান্টিজেনের সাথে বেঁধে যায়। যখন কোন ব্যক্তির রক্তে A অ্যান্টিজেন থাকে, তখন তার শরীরে B অ্যান্টিজেনের বিরুদ্ধে অ্যান্টিবডি তৈরি হয়। একইভাবে, যখন কোন ব্যক্তির রক্তে B অ্যান্টিজেন থাকে, তখন তার শরীরে A অ্যান্টিজেনের বিরুদ্ধে অ্যান্টিবডি তৈরি হয়।
রক্ত সঞ্চালন:
রক্ত সঞ্চালনের সময়, রক্ত দানকারী এবং গ্রহীতার রক্তের গ্রুপের মিল থাকা গুরুত্বপূর্ণ। কারণ, যদি গ্রহীতার রক্তে অ্যান্টিবডি থাকে যা দানকারীর রক্তের অ্যান্টিজেনের সাথে বেঁধে যায়, তাহলে গ্রহীতার শরীরে রক্তের কোষ ভেঙে যেতে পারে। এর ফলে জটিল স্বাস্থ্য সমস্যা, এমনকি মৃত্যুও হতে পারে।
নিচে রক্ত সঞ্চালনের জন্য একটি সারণী দেওয়া হল:
| গ্রহীতার রক্তের গ্রুপ | দানকারীর রক্তের গ্রুপ |
|---|---|
| A | A, O |
| B | B, O |
| AB | A, B, AB, O |
| O | O |
বিশ্বজনীন দানকারী এবং গ্রহণকারী:
- O রক্তের গ্রুপের ব্যক্তিরা বিশ্বজনীন দানকারী।[১২] কারণ, তাদের রক্তে A বা B অ্যান্টিজেন থাকে না, তাই A, B, AB, O যেকোনো রক্তের গ্রুপের ব্যক্তিকে রক্ত দিতে পারে।
- AB রক্তের গ্রুপের ব্যক্তিরা বিশ্বজনীন গ্রহণকারী। কারণ, তাদের রক্তে A এবং B উভয় অ্যান্টিজেন থাকে, তাই A, B, AB, O যেকোনো রক্তের গ্রুপের রক্ত গ্রহণ করতে পারে।
প্রকারভেদ[সম্পাদনা]
গ্লাইকোলিপিডকে বিভিন্ন উপদলে বিভক্ত করা যায়, প্রতিটি উপদলের নিজস্ব কাঠামো ও কাজ রয়েছে।
- গ্লাইকোগ্লিসারোলিপিড: এই উপদলে চর্বির অংশটি অ্যাসিটাইলেটেড বা নন-অ্যাসিটাইলেটেড গ্লিসারোল দিয়ে তৈরি হয় এবং কমপক্ষে একটি ফ্যাটি অ্যাসিড থাকে। এগুলো সাধারণত ফোটোসিন্থেটিক ঝিল্লিতে পাওয়া যায় এবং ফোটোসিন্থেসিসের সাথে সম্পর্কিত কাজ করে। এই উপদল আরও বিভক্ত হয় যেগুলো যুক্ত শর্করা অণুর উপর নির্ভর করে।[১৩]
- গ্যালাক্টোলিপিড: এগুলো গ্লিসারোল চর্বির অণুতে যুক্ত গ্যালাক্টোজ শর্করা দ্বারা সংজ্ঞায়িত হয়। এগুলো ক্লোরোপ্লাস্ট ঝিল্লিতে পাওয়া যায় এবং ফোটোসিন্থেসিসের সাথে সম্পর্কিত।[১৪]
- সালফোলিপিড: এগুলোর শর্করা অংশে সালফার-ধারণকারী একটি ফাংশনাল গ্রুপ থাকে। একটি গুরুত্বপূর্ণ গ্রুপ হলো "সালফোকুইনোভোসিল ডাইঅ্যাসাইলগ্লিসারোল" যা উদ্ভিদের সালফার চক্রের সাথে সম্পর্কিত।[১৫]
- গ্লাইকোস্ফিঙ্গোলিপিড: এই উপদলটি স্ফিঙ্গোলিপিড নামক চর্বির উপর ভিত্তি করে গঠিত। এগুলো প্রধানত স্নায়ুতন্ত্রে পাওয়া যায় এবং কোষের মধ্যে সংকেত আদানপ্রদানের কাজ করে।[১৬]
- সেরিব্রোসাইড: এই গ্রুপের গ্লাইকোস্ফিঙ্গোলিপিডগুলো স্নায়ু কোষের ঝিল্লিতে গুরুত্বপূর্ণ ভূমিকা পালন করে।[১৭]
- গ্যালাক্টোসেরিব্রোসাইড: সেরিব্রোসাইডের একটি প্রকার যাতে গ্যালাক্টোজ শর্করা থাকে।
- গ্লুকোসেরিব্রোসাইড: সেরিব্রোসাইডের একটি প্রকার যাতে গ্লুকোজ শর্করা থাকে; সাধারণত স্নায়ুতন্ত্রের বাইরে পাওয়া যায়।
- সালফেটাইড: এই গ্রুপের গ্লাইকোলিপিডগুলোতে একটি সালফেট গ্রুপ থাকে, যা সেরামাইড চর্বির সাথে যুক্ত থাকে। এগুলো রোগ প্রতিরোধ ব্যবস্থা থেকে স্নায়ুতন্ত্রের সংকেত আদানপ্রদান পর্যন্ত বিভিন্ন জৈবিক কাজে জড়িত।
- গ্যাংলিওসাইড: সবচেয়ে জটিল প্রাণীজ গ্লাইকোলিপিড। এগুলোতে ঋণাত্মক চার্জযুক্ত অলিগোস্যাকারাইড থাকে, যার মধ্যে এক বা একাধিক সিয়ালিক অ্যাসিড অবশিষ্টাংশ থাকে; এ পর্যন্ত ২০০টিরও বেশি[১৮] বিভিন্ন গ্যাংলিওসাইড সনাক্ত করা হয়েছে। এগুলো স্নায়ু কোষে সবচেয়ে বেশি পরিমাণে থাকে।
- গ্লোবোসাইড: গ্লাইকোস্ফিঙ্গোলিপিডে একাধিক জটিল শর্করা থাকে। এগুলোর বিভিন্ন কাজ রয়েছে; এই অণুগুলোকে ভাঙতে ব্যর্থ হলে ফ্যাব্রি রোগ দেখা দেয়।
- গ্লাইকোফোসফোস্ফিঙ্গোলিপিড: ছত্রাক, ইস্ট এবং উদ্ভিদের জটিল গ্লাইকোফোসফোলিপিড। এখানে এগুলোকে "ফাইটোগ্লাইকোলিপিড" বলা হয়। এগুলো ঋণাত্মক চার্জযুক্ত গ্যাংলিওসাইডের মতো জটিল যৌগ হতে পারে।
- গ্লাইকোফোসফাটিডিলিনোসিটল: একটি ফসফাটিডিলিনোসিটল চর্বি অংশ দ্বারা সংজ্ঞায়িত গ্লাইকোলিপিডের উপদল, যা একটি জটিল শর্করার সাথে যুক্ত থাকে। এগুলো প্রোটিনের C-টার্মিনাসের সাথে যুক্ত হতে পারে এবং বিভিন্ন প্রোটিনের সাথে যুক্ত থেকে বিভিন্ন কাজ করতে পারে।[১৯]
- সেরিব্রোসাইড: এই গ্রুপের গ্লাইকোস্ফিঙ্গোলিপিডগুলো স্নায়ু কোষের ঝিল্লিতে গুরুত্বপূর্ণ ভূমিকা পালন করে।[১৭]
- লিপোপলিস্যাকারাইড: ব্যাকটেরিয়ার কোষ প্রাচীরের একটি গুরুত্বপূর্ণ উপাদান।
- স্যাকারোলিপিড: শর্করা এবং চর্বির সাথে তৈরি জৈব অণু।
আরও দেখুন[সম্পাদনা]
তথ্যসূত্র[সম্পাদনা]
- ↑ Voet, Donald; Voet, Judith; Pratt, Charlotte (২০১৩)। Fundamentals of Biochemistry Life at the Molecular Level (Fourth সংস্করণ)। Hoboken, NJ: John Wiley & Sons, Inc.। আইএসবিএন 9781118129180। অজানা প্যারামিটার
|name-list-style=উপেক্ষা করা হয়েছে (সাহায্য) - ↑ "Glycolipids"। nature। Nature Publishing Group। সংগ্রহের তারিখ ২০১৫-১১-০১।
- ↑ "Glycolipids"। nature। Nature Publishing Group। সংগ্রহের তারিখ ২০১৫-১১-০১।
- ↑ "Glycolipids"। nature। Nature Publishing Group। সংগ্রহের তারিখ ২০১৫-১১-০১।
- ↑ Aureli M, Grassi S, Prioni S, Sonnino S, Prinetti A (আগস্ট ২০১৫)। "Lipid membrane domains in the brain"। Biochimica et Biophysica Acta (BBA) - Molecular and Cell Biology of Lipids। 1851 (8): 1006–16। ডিওআই:10.1016/j.bbalip.2015.02.001। পিএমআইডি 25677824।
- ↑ Williams GJ, Thorson JS (২০০৯)। "Natural product glycosyltransferases: properties and applications"। Advances in Enzymology। Advances in Enzymology - and Related Areas of Molecular Biology। 76। পৃষ্ঠা 55–119। আইএসবিএন 9780470392881। ডিওআই:10.1002/9780470392881.ch2। পিএমআইডি 18990828।
- ↑ Sinnott ML (নভেম্বর ১৯৯০)। "Catalytic mechanism of enzymic glycosyl transfer"। Chemical Reviews। 90 (7): 1171–1202। ডিওআই:10.1021/cr00105a006।
- ↑ Sandhoff K (১৯৭৪)। "Sphingolipidoses"। Journal of Clinical Pathology। 8 (12): 94–105। ডিওআই:10.1136/jcp.s3-8.1.94। পিএমআইডি 4157247। পিএমসি 1347206
 ।
।
- ↑ Schnaar RL (জুন ২০০৪)। "Glycolipid-mediated cell-cell recognition in inflammation and nerve regeneration"। Archives of Biochemistry and Biophysics। 426 (2): 163–72। ডিওআই:10.1016/j.abb.2004.02.019। পিএমআইডি 15158667।
- ↑ Cooper GM (২০০০)। "Cell-Cell Interactions"। The Cell: A Molecular Approach. (2nd সংস্করণ)। Sunderland (MA): Sinauer Associates।
- ↑ Wang, Binghe; Boons, Geert-Jan (২০১১-০৯-০৯)। Carbohydrate Recognition: Biological Problems, Methods, and Applications। John Wiley & Sons। পৃষ্ঠা 66। আইএসবিএন 9781118017579। অজানা প্যারামিটার
|name-list-style=উপেক্ষা করা হয়েছে (সাহায্য) - ↑ Erb IH (মে ১৯৪০)। "Blood Group Classification: A Plea for Uniformity"। Canadian Medical Association Journal। 42 (5): 418–21। পিএমআইডি 20321693। পিএমসি 537907
 ।
।
- ↑ Neufeld EF, Hall CW (জানুয়ারি ১৯৬৪)। "Formation of galactolipids by chloroplasts"। Biochemical and Biophysical Research Communications। 14 (6): 503–8। ডিওআই:10.1016/0006-291X(64)90259-1। পিএমআইডি 5836548।
- ↑ Neufeld EF, Hall CW (জানুয়ারি ১৯৬৪)। "Formation of galactolipids by chloroplasts"। Biochemical and Biophysical Research Communications। 14 (6): 503–8। ডিওআই:10.1016/0006-291X(64)90259-1। পিএমআইডি 5836548।
- ↑ Harwood JL, Nicholls RG (এপ্রিল ১৯৭৯)। "The plant sulpholipid-- a major component of the sulphur cycle"। Biochemical Society Transactions। 7 (2): 440–7। ডিওআই:10.1042/bst0070440। পিএমআইডি 428677।
- ↑ Hakomori S, Igarashi Y (ডিসেম্বর ১৯৯৫)। "Functional role of glycosphingolipids in cell recognition and signaling"। Journal of Biochemistry। 118 (6): 1091–103। ডিওআই:10.1093/oxfordjournals.jbchem.a124992
 । পিএমআইডি 8720120।
। পিএমআইডি 8720120।
- ↑ Jurevics H, Hostettler J, Muse ED, Sammond DW, Matsushima GK, Toews AD, Morell P (মে ২০০১)। "Cerebroside synthesis as a measure of the rate of remyelination following cuprizone-induced demyelination in brain"। Journal of Neurochemistry। 77 (4): 1067–76। ডিওআই:10.1046/j.1471-4159.2001.00310.x
 । পিএমআইডি 11359872।
। পিএমআইডি 11359872।
- ↑ Ariga T, McDonald MP, Yu RK (জুন ২০০৮)। "Role of ganglioside metabolism in the pathogenesis of Alzheimer's disease--a review"। Journal of Lipid Research। 49 (6): 1157–75। ডিওআই:10.1194/jlr.R800007-JLR200
 । পিএমআইডি 18334715। পিএমসি 2386904
। পিএমআইডি 18334715। পিএমসি 2386904  ।
।
- ↑ Paulick MG, Bertozzi CR (জুলাই ২০০৮)। "The glycosylphosphatidylinositol anchor: a complex membrane-anchoring structure for proteins"। Biochemistry। 47 (27): 6991–7000। ডিওআই:10.1021/bi8006324। পিএমআইডি 18557633। পিএমসি 2663890
 ।
।
বহিঃসংযোগ[সম্পাদনা]
- Glycolipids যুক্তরাষ্ট্রের জাতীয় চিকিৎসা গ্রন্থাগারে চিকিৎসা বিষয়ক শিরোনাম (MeSH)
