আইসোটোপ
| নিউক্লীয় পদার্থবিজ্ঞান |
|---|
 |
| নিউক্লিয়াস · নিউক্লিয়ন (প্রো., নি.) · পারমাণবিক বল · নিউক্লিয়াসের গঠন · পারমাণবিক বিক্রিয়া |
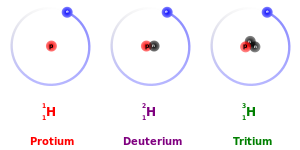
যেসব পরমাণুর নিউক্লিয়াসে প্রোটন সংখ্যা (p) সমান; কিন্তু নিউট্রন সংখ্যা (n) অসমান হওয়ায় ভর সংখ্যা (n + p) অসমান হয়, এদেরকে আইসোটোপ বলে।সমস্থানিক বা আইসোটোপ হলো একই মৌলিক পদার্থের ভিন্ন ভিন্ন পরমাণু যাদের পারমাণবিক সংখ্যা একই তবে নিউক্লিয়াসে নিউট্রনের সংখ্যা ভিন্ন। সমস্থানিকসমূহের পারমাণবিক সংখ্যা একই কিন্তু ভর সংখ্যা ভিন্ন। প্রোটনের সংখ্যা একই থাকায় সমস্থানিকসমূহের রাসায়নিক ও ভৌত ধর্মে অনেক সাদৃশ্য বিদ্যমান। যেমন- কার্বন-১২, কার্বন-১৩, কার্বন-১৪ তিনটি সমস্থানিক যারা একই পদার্থ কার্বন হতে উৎপন্ন, এদের ভর সংখ্যা যথাক্রমে ১২, ১৩ ও ১৪। কার্বনের পারমাণবিক সংখ্যা ৬, তাই এসকল সমস্থানিকে নিউট্রনের সংখ্যা হল যথাক্রমে ১২-৬=৬, ১৩-৬=৭ এবং ১৪-৬=৮। সংক্ষেপে, সমস্থানিকসমূহ ভিন্ন নিউট্রন সংখ্যা বিশিষ্ট একই পদার্থের পরমাণু। এদের প্রোটন ও ইলেকট্রন সংখ্যা একই।
প্রোটন ও নিউট্রনের সুনির্দিষ্ট বিন্যাস সংবলিত নিউক্লিয়াসকে বলা হয় নিউক্লাইড। নিউক্লাইডের ধারণা রাসায়নিক বৈশিষ্টের চেয়ে নিউক্লিয়ার বৈশিষ্টকে বেশি গুরুত্ব আরোপ করে, পক্ষান্তরে সমস্থানিক করে তার উল্টোটি। নিউট্রনের সংখ্যা পরমাণুর নিউক্লিয়ার বৈশিষ্টকে অনেক বেশি প্রভাবিত করলেও তা রাসায়নিক বৈশিষ্টকে অতটা প্রভাবিত করে না। যেহেতু সমস্থানিক ঐতিহাসিকভাবে সুপরিচিত, তাই যে ক্ষেত্রে যেখানে নিউক্লাইড ব্যবহার করা অধিকতর যুক্তিসঙ্গত কোন কোন সময় সেসব জায়গায় সমস্থানিক ব্যবহৃত হয়, যেমন- নিউক্লিয়ার প্রযুক্তিতে।
কোন সমস্থানিকের সংকেত প্রকাশের জন্য সংশ্লিষ্ট মৌলের নামের পরে একটি হাইফেন চিহ্নের পর ভর সংখ্যা উল্লেখ করতে হয় (যেমন- হিলিয়াম-৩, কার্বন-১২, আয়োডিন-১৩১, ইউরেনিয়াম-২৩৮)। কোন মৌলকে প্রকাশের ক্ষেত্রে ঐ মৌলের সংকেতের বামে উপরে ভর সংখ্যা, বাম পাশে নিচে পারমাণবিক সংখ্যা উল্লেখ করা হয়।
কিছু সমস্থানিক তেজস্ক্রিয়, এদেরকে বলে তেজস্ক্রিয় সমস্থানিক বা রেডিও নিউক্লাইড। আবার কিছু সমস্থানিক তেজস্ক্রিয় ক্ষয় প্রদর্শন করে না, এদেরকে বলে স্থায়ী সমস্থানিক। যেমন- 14
6C
একটি কার্বনের তেজস্ক্রিয় সমস্থানিক আবার 12
6C
এবং 13
6C
কার্বনের স্থায়ী সমস্থানিক। প্রাকৃতিকভাবে উৎপন্ন সমস্থানিকের সংখ্যা ৩৩৯,[১] এদের মধ্যে ২৮ টি হল প্রাইমর্ডিয়াল বা আদিম এবং ২৫৯ টি স্থায়ী সমস্থানিক।[১] প্রাইমোর্ডিয়াল সমস্থানিক হল সেসব সমস্থানিক যেগুলো পৃথিবী সৃষ্টির পূর্ব হতে বর্তমান অবস্থা পর্যন্ত একই রূপে অক্ষত রয়েছে। ধারণা করা হয় যে কিছু কিছু স্থায়ী সমস্থানিকও তেজস্ক্রিয় যাদের অর্ধায়ু বা হাফ-লাইফ অত্যন্ত দীর্ঘ। প্রাকৃতিক ও কৃত্রিমভাবে সৃষ্ট মোট সমস্থানিকের সংখ্যা হল ৩১০০ টি।[২]
সংকেত
[সম্পাদনা]কোন মৌলিক পদার্থের আইসোটোপ বা নিউক্লাইডকে মৌলিক পদার্থটির নামের পর হাইফেন বসিয়ে এর ভরসংখ্যা যোগ করে প্রকাশ করা হয় (যেমন— হিলিয়াম-3, হিলিয়াম-4, কার্বন-12, কার্বন-14, ইউরেনিয়াম-235, ইউরেনিয়ান-239 ইত্যাদি)।[৩] রাসায়নিক প্রতীক দিয়ে আইসোটোপ লেখার ক্ষেত্রে প্রতীকটির বাম পার্শ্বে উপরে ভরসংখ্যা এবং বাম পার্শ্বে নিচে পারমাণবিক সংখ্যা উল্লেখ করতে হয় (যেমন— 3
2He
, 4
2He
, 12
6C
, 14
6C
, 235
92U
, 239
92U
ইত্যাদি।).[৪] প্রতিটি মৌলের প্রতীক একটি নির্দিষ্ট পারমাণবিক সংখ্যা নির্দেশ করায় অনেক সময় শুধুমাত্র ভরসংখ্যা উল্লেখ করা হয় (যেমন— 3
He
, 4
He
, 12
C
, 14
C
, 235
U
, 239
U
ইত্যাদি)। কখনো কখনো নিউক্লিয় আইসোমার নির্দেশ করতে ভরসংখ্যার শেষে m যুক্ত করা হয় (যেমন— 180m
73Ta
(ট্যান্টালাম-180m)। উল্লেখিত সংকেত ব্যবস্থাটি হল আইসোটোপের আদর্শ সংকেত যা এখন "AZE সংকেত" নামে পরিচিত যেখানে A হল ভরসংখ্যা, Z হল পারমাণবিক সংখ্যা এবং E হল মৌলটির প্রতীক।
সাধারণত "AZE সংকেত" যেভাবে লেখা হয় সেভাবে এটি পড়া হয় না। যেমন— 4
2He
কে সাধারণত চার-দুই-হিলিয়াম এর পরিবর্তে চার-হিলিয়াম বা 4-হিলিয়াম পড়া হয়। অনুরূপভাবে 235
92U
কে ২৩৫-ইউরেনিয়াম পড়া হয়।
তেজস্ক্রিয়, আদিম ও স্থিতিশীল আইসোটোপ
[সম্পাদনা]যেসব আইসোটোপ তেজস্ক্রিয়তা প্রদর্শন করে তাদেরকে তেজস্ক্রিয় আইসোটোপ বা তেজস্ক্রিয় নিউক্লাইড বলা হয়, অপরদিকে যেসব আইসোটোপের কখনোই তেজস্ক্রিয় ক্ষয় ঘটে না তাদেরকে স্থিতিশীল আইসোটোপ বা স্থিতিশীল নিউক্লাইড বলা হয়। যেমন— 14
C
হল কার্বনের তেজস্ক্রিয় আইসোটোপ অপরদিকে 12
C
এবং 13
C
হল কার্বনের স্থিতিশীল আইসোটোপ। আবার যেসব আইসোটোপ পৃথিবী সৃষ্টির আদি (মহা বিস্ফোরণ) থেকে সৌরজগৎের গঠনের পূর্ব পর্যন্ত বিদ্যমান ছিল তাদেরকে আদিম আইসোটোপ বা কখনো কখনো আদিম নিউক্লাইড বলা হয়। বিসমাথ, থোরিয়াম, ইউরেনিয়াম এবং প্লুটোনিয়াম হল আদিম নিউক্লাইড। কারণ এদের অর্ধায়ু এমনই দীর্ঘ যে অদ্যাবধি পৃথিবীতে এদের পাওয়া যায়। এছাড়াও পটাশিয়াম-40 একটি আদিম নিউক্লাইড।[৫]
পৃথিবীতে প্রাকৃতিক ভাবে প্রায় ৩৩৯টি নিউক্লিয়াইড পাওয়া গেছে যাদের মধ্যে ২৮৬টি আদিম নিউক্লাইড।[১] এদের মধ্যে ২৬৯টি স্থিতিশীল এবং ৭০টি তেজস্ক্রিয়। এছাড়াও কণা ত্বরক যন্ত্রে ১৬৫০টি তেজস্ক্রিয় আইসোটোপ কৃত্রিমভাবে তৈরি করা হয়েছে।
সমস্থানিকের বৈশিষ্টসমূহের বিভিন্নতা
[সম্পাদনা]রাসায়নিক ও পারমাণবিক বৈশিষ্ট্য
[সম্পাদনা]একটি নিরপেক্ষ পরমাণুতে সমসংখ্যক ইলেকট্রন এবং প্রোটন থাকে। তাই, কোন মৌলের সকল সমস্থানিকে সমান সংখ্যক ইলেকট্রন ও প্রোটন থাকে, এমনকি এদের ইলেকট্রন বিন্যাসও একই, কারণ একটি পরমাণুর রাসায়নিক বৈশিষ্ট্য এর ইলেকট্রন বিন্যাসের উপর নির্ভরশীল। একারণে একই মৌলের সমস্থানিকসমূহ প্রায় অভিন্ন রাসায়নিক বৈশিষ্ট্য প্রদর্শন করে। সমস্থানিকসমূহের ইলেকট্রন ও প্রোটন সংখ্যা সমান থাকলেও নিউট্রন সংখ্যা ভিন্ন থাকে। তাই এদের ভরসংখ্যাও ভিন্ন হয়। যেমনঃ- ওজোন ও অক্সিজেন।
ব্যবহার
[সম্পাদনা]বর্তমান বিজ্ঞান জগতে তেজস্ক্রিয় আইসোটোপ এক বিস্ময়কর ভূমিকা গ্রহণ করেছে। বিজ্ঞানের অধিকাংশ ক্ষেত্রে এদের ব্যবহার হয়ে থাকে।
কৃষিবিদ্যায় ব্যবহার
[সম্পাদনা]কৃষিবিদ্যায় আইসোটোপের ব্যবহার অত্যন্ত গুরুত্বপূর্ণ। খাদ্য দ্রব্য উৎপাদনের খরচের মধ্যে জমির সার একটি প্রধান খরচ। ফসফেট জাতীয় সারের সাথে রেডিও ফসফরাস আইসোটোপ মিশ্রিত থাকে বলা যেতে পারে গাছের মধ্যে এই সার গাছের বৃদ্ধির কোন স্তরে কি কি কাজ করছে। বিজ্ঞানীরা পরীক্ষা করে দেখেছেন যে, মাটির উপর ফসফেট দেবার সাথে সাথেই গাছপালা শিকড় দিয়ে সেগুলিকে টেনে নেয়। রেডিও আইসোটোপের সাহায্যে আরো জানা গেছে যে, তামাক, ভুট্টা, তুলা, বিট প্রভৃতি গাছ কেবল চারা অবস্থাতেই ফসফেট গ্রহণ করতে সক্ষম। চারা অবস্থাতেই এই সার দেওয়া না হলে তেমন কোনো কাজে আসে না। পর্যবেক্ষক আইসোটোপ ব্যবহার করে জানা গেছে যে, জমিতে জল সেচনের পূর্বে ওই জলে ফসফরিক এসিড মিশ্রিত করে দিলেই জমিতে ফসফেট দেওয়ার আর কোনো প্রয়োজন হয় না।
তেজস্ক্রিয় সাহায্যে নতুন নতুন জাতের বীজ সৃষ্টি করাও বর্তমানে সম্ভব হয়েছে। অধিকন্তু আলু পেঁয়াজ রসুন প্রভৃতি বিভিন্ন কৃষিজাত ফসল দীর্ঘদিন সংরক্ষণ করার জন্য একটি সুনির্দিষ্ট মাত্রার তেজস্ক্রিয় বিকিরণ প্রয়োগ করা হয়। এর ফলে পোকামাকড় বা জীবাণু আক্রমণে ফসল সহজে নষ্ট হয় না; আলু পেঁয়াজের চারা গজানো এবং বিভিন্ন রকম ফলের পাকা বা পচে যাওয়া বিলম্বিত হয়।
তেজস্ক্রিয় বিকিরণের সাহায্যে বিভিন্ন দেশে ফসলের ক্ষতিকর নানা রকম কীটপতঙ্গ ধ্বংস করার পদ্ধতিও বেশ সাফল্যজনক প্রমাণিত হয়েছে। এই পদ্ধতিতে বিকিরণের সাহায্যে বিপুল সংখ্যক পুরুষ পতঙ্গের প্রজনন ক্ষমতা নষ্ট করে তাদের ছেড়ে দেওয়া হয় যেখানে ফসলে ওই পতঙ্গের আক্রমণ হওয়ার সম্ভাবনা দেখা দিয়েছে। বিভিন্ন দেশে ধ্বংস করার পদ্ধতি বিপুল সংখ্যক ফলে স্ত্রী পতঙ্গরা প্রজনন ক্ষমতাহীন পুরুষ পতঙ্গের সাথে মিলিত হলে তাদের বংশ বিস্তার ঘটে না। বলাবাহুল্য এতে কীটনাশক ব্যবহারের প্রয়োজন হয় না বলে পরিবেশ দূষিত হওয়ার সম্ভাবনা থাকে না। অথচ কীটপতঙ্গ নির্বংশ হওয়ায় ফসল রক্ষা পায়।
রেডিও আইসোটোপ ব্যবহার করে সবুজ লতা-পাতার ফটোসিন্থেসিস বা সালোকসংশ্লেষণ সম্পর্কে অনেক তথ্য জানা সম্ভব হয়েছে।
শিল্পজগতে ব্যবহার
[সম্পাদনা]তেজস্ক্রিয় আইসোটোপের সাহায্যে ধাতু দিয়ে তৈরি দেয়াল বা প্লেটের বেধ অতি সহজেই মাপা যেতে পারে। মোটর গাড়ির টায়ার, ঘরবাড়ি রং করার রং, গাঁথুনির কংক্রিট প্রভৃতি কতখানি মজবুত বা টেকসই তা নির্ধারণের সমস্ত কার্যে পর্যবেক্ষক আইসোটোপ ব্যবহার করা হয়ে থাকে। কারখানায় কার্যরত শ্রমিকদের দুর্ঘটনার হাত থেকে বাঁচানোর জন্য রেডিও আইসোটোপ ব্যবহার করা হয়ে থাকে। তেজস্ক্রিয় উপাদান দিয়ে তৈরি এক প্রকার গ্লাভস বা কব্জিবন্ধ হাতে লাগিয়ে মিস্ত্রিরা কার্যরত হয় এবং মেশিনে তেজস্ক্রিয় রশ্মি ধরা পড়ার যন্ত্র যুক্ত করা থাকে। মিস্ত্রির হাত মেশিনের খুব কাছে গেলেই তার হাতের কব্জি বন্ধ হতে নির্গত তেজস্ক্রিয় রশ্মি যন্ত্রে ধরা পরে এবং সাথে সাথেই তাকে সতর্ক করে দেওয়ার জন্য তীব্র আলোর ঝলকানি সৃষ্টি হয় অথবা মেশিনটি স্বয়ংক্রিয়ভাবে বন্ধ হয়ে যায়। এছাড়া একটি মেশিনের মধ্যে কোনখানে কি পরিমাণ ঘর্ষণ হচ্ছে এবং পিচ্ছিলকারক পদার্থসমূহ কি পরিমাণ কাজ করতে পারছে এই সমস্ত গবেষণার ক্ষেত্রেও রেডিও আইসোটোপ ব্যবহার করা হয়ে থাকে।
চিকিৎসাবিজ্ঞানে ব্যবহার
[সম্পাদনা]চিকিৎসা বিজ্ঞানে রোগ নির্ণয় ও নিরাময়ে তথা গবেষণা ও উন্নয়নে তেজস্ক্রিয় বিকিরণের বহুল প্রয়োগ বর্তমানে বিশ্বজুড়ে চালু হয়েছে। এই চিকিৎসা পদ্ধতির হাতিয়ার হচ্ছে তেজস্ক্রিয় আইসোটোপ। রোগভেদে এবং রোগাক্রান্ত অঙ্গ ভেদে ভিন্ন ভিন্ন তেজস্ক্রিয় আইসোটোপ প্রয়োগ করা হয়ে থাকে। সচরাচর গামা রশ্মি নিঃসরণকারী স্বল্প অর্ধায়ুর তেজস্ক্রিয় আইসোটোপ ব্যবহৃত হয়। আজকাল অনেক ক্ষেত্রে পজিট্রন বিচ্ছুরণকারী আইসোটোপ যথা: তামা-64, কার্বন-11 এবং অক্সিজেন-15 রোগ নির্ণয়ে ব্যবহৃত হচ্ছে। তেজস্ক্রিয় আইসোটোপের ব্যবহারে ক্ষতিকর প্রতিক্রিয়া নেই বললেই চলে। গড়ে প্রতিদিন 1000 থেকে 10,000 টি পরীক্ষার মধ্যে একটি ক্ষেত্রে ক্ষতিকর প্রভাব লক্ষ্য করা গেছে।
পরমাণু চিকিৎসায় ব্যবহৃত আইসোটোপগুলির মধ্যে সবচেয়ে যেসব বেশি ব্যবহৃত হয় সেগুলি হচ্ছে আয়োডিন-131, আয়োডিন-125, টেকনিশিয়ান-99, স্ট্রনশিয়াম-90 ইত্যাদি।
পরমাণু চিকিৎসায় রোগ নির্ণয়ে ব্যবহৃত যন্ত্রগুলি নিম্নরূপ:
- থাইরয়েড আপটেক যন্ত্র: রোগীকে তেজস্ক্রিয়-131 সেবন করানোর পর নির্ধারিত সময়ান্তে থাইরয়েড গ্রন্থিতে আয়োডিন গ্রহণের শতকরা হার এ যন্ত্র দ্বারা পরিমাপ করা হয়ে থাকে।
- লিনিয়ার স্ক্যানার: এ যন্ত্রের দ্বারা থাইরয়েড গ্রন্থির প্রতিটি অংশে সেবন কৃত আয়োডিন গ্রহণের শতকরা হার পরিমাপনের মাধ্যমে গলগ্রন্থির প্রতিচিত্র গ্রহণের পর তাতে কি ধরনের রোগ হয়েছে তা নির্ণয় করা যায়। তাছাড়া এই যন্ত্র ব্যবহার করে তেজস্ক্রিয় টেকনিশিয়ান-99 এর সাথে বিভিন্ন বিভিন্ন কীট মিশিয়ে যকৃত, কিডনি, হাড়, মস্তিষ্ক, হৃৎপিণ্ড ইত্যাদি প্রত্যঙ্গের প্রতিচিত্র গ্রহণ করে ফোঁড়া, টিউমার, ক্যান্সার ও অন্যান্য জটিল রোগের উপস্থিতি নির্ণয় করা যায়।
- টেরিজিয়াম অ্যাপ্লিকেটর: চোখের টেরিজিয়াম অপারেশনের পর পুনরাবৃত্তি রোধ করার জন্য পরপর দুদিন স্ট্রনশিয়াম-90 থেকে নিঃসৃত বিটা রশ্মি দ্বারা চিকিৎসা করা হয়ে থাকে।
- গামা ক্যামেরা: এ যন্ত্রের সাহায্যে লিনিয়ার স্ক্যানারের চেয়ে দ্রুত তেজস্ক্রিয় পরমাণু চিত্র তথা আপটেকের ধরনধারণ জানা যায়। গামা ক্যামেরায় কম্পিউটার যুক্ত করা হলে চিত্রটি বিভিন্ন ভাবে নিয়ন্ত্রণ করা সম্ভব হয় এবং নিরীক্ষিত এলাকা থেকে বিভিন্ন তথ্য সংগ্রহ করা সম্ভব হয়। পরমাণু-চিকিৎসা পদ্ধতিতে এ যন্ত্রের গুরুত্ব অপরিসীম ও সর্বাধিক।
- রেনোগ্রাম: কিডনির কার্যকারিতা পরীক্ষণে ও রোহ নির্ণয়ে রেনোগ্রাম ব্যবহার করা হয়। এর জন্য অল্পমাত্রায় তেজস্ক্রিয় আয়োডিন-131 ও একটি রাসায়নিক পদার্থের সংমিশ্রণ ইনজেকশনের মাধ্যমে রোগীর শরীরে প্রবেশ করানো হয় এবং চিত্রের মাধ্যমে রোগ নির্ণয় করা হয়। কিডনি সংযোজনের ক্ষেত্রে এই পরীক্ষাটি গুরুত্বপূর্ণ।
- উন্নত ধরনের গামা গণনা যন্ত্র: এটি এক ধরনের স্বয়ংক্রিয় গণক যন্ত্র বা কাউন্টার। পরিমাপের সকল কাজ করেনি এই সূক্ষ্ম যন্ত্রটি ব্যবহার করা হয়ে থাকে। কোন তেজস্ক্রিয় নমুনা সক্রিয়তা এটি অনেক বেশি দক্ষ।
- পজিট্রন ক্যামেরা: এই পদ্ধতিতে স্ফটিক ব্যবহার করে বিপরীতমুখী দুটি গামা রশ্মি ফটো ধারণ করা হয়। এর ফলে বিভিন্ন তল থেকে গৃহীত প্রতিচ্ছায়ার সমষ্টি একটি তীক্ষ্ণ ও বিচিত্র সৃষ্টি করতে পারে। কিন্তু পজিট্রন বিকিরণকারী আইসোটোপগুলির অর্ধায়ু খুব কম হওয়ায় তরব যন্ত্র ব্যবহার করে কৃত্রিম উপায়ে এগুলি উৎপাদন করতে হয়। ফলে পজিট্রন মাধ্যমে চিত্রায়ন খুবই ব্যয়বহুল।
রসায়নে ব্যবহার
[সম্পাদনা]রসায়নে এদের ব্যবহার প্রভূত কল্যাণ সাধন করেছে। এদের সাহায্যে বহু সাংশ্লেষিক উপাদান প্রস্তুত করা সম্ভব হয়েছে। রাসায়নিক বিক্রিয়ার হার, পদার্থের অণুর গঠন, দ্রবণীয়তা, অনুঘটন প্রভৃতি বিষয়ে গবেষণা তেজস্ক্রিয় আইসোটোপের সাহায্যে সহজলভ্য হয়েছে।
তথ্যসূত্র
[সম্পাদনা]- ↑ ক খ গ "Radioactives Missing From The Earth"।
- ↑ "NuDat 2 Description"। ২৩ ডিসেম্বর ২০১৬ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ৩০ জানুয়ারি ২০১০।
- ↑ IUPAC (Connelly, N. G.; Damhus, T.; Hartshorn, R. M.; and Hutton, A. T.), Nomenclature of Inorganic Chemistry – IUPAC Recommendations 2005, The Royal Society of Chemistry, 2005; IUPAC (McCleverty, J. A.; and Connelly, N. G.), Nomenclature of Inorganic Chemistry II. Recommendations 2000, The Royal Society of Chemistry, 2001; IUPAC (Leigh, G. J.), Nomenclature of Inorganic Chemistry (recommendations 1990), Blackwell Science, 1990; IUPAC, Nomenclature of Inorganic Chemistry, Second Edition ওয়েব্যাক মেশিনে আর্কাইভকৃত ৩ মার্চ ২০১৬ তারিখে, 1970; probably in the 1958 first edition as well
- ↑ This notation seems to have been introduced in the second half of the 1930s. Before that, various notations were used, such as Ne(22) for neon-22 (1934), Ne22 for neon-22 (1935), or even Pb210 for lead-210 (1933).
- ↑ "Primordial Radionuclides"
বহিঃসংযোগ
[সম্পাদনা]- নিউক্লিওনিকা নিউক্লিয়ার সায়েন্স পোর্টাল
- নিউক্লিওনিকা নিউক্লিয়ার সায়েন্স উইকি
- য়ান্তর্জাতিক পরমাণু শক্তি সংস্থা
- সকল সমস্থানিকের পারমাণবিক ভর
- Atomgewichte, Zerfallsenergien und Halbwertszeiten aller Isotope
- নিউক্লাইডসমূহের চার্ট ওয়েব্যাক মেশিনে আর্কাইভকৃত ৩ জুলাই ২০০৮ তারিখে $২৫
- বর্তমান সমস্থানিক বিষয়ক গবেষণা এবং তথ্য
- তেজস্ক্রিও সমস্থানিকসমূহ
- নিউক্লাইড, সমস্থানিক এবং পর্যায় সারণীর ইন্টারঅ্যাকটিভ চার্ট
 The LIVEChart of Nuclides - IAEA with isotope data, in Java or HTML
The LIVEChart of Nuclides - IAEA with isotope data, in Java or HTML
| পদার্থবিজ্ঞান-সম্পর্কিত বিষয়ক এই নিবন্ধটি অসম্পূর্ণ। আপনি চাইলে এটিকে সম্প্রসারিত করে উইকিপিডিয়াকে সাহায্য করতে পারেন। |
