সমাণু
সমাণু বা সমাবয়ব হল রসায়ন এ অণু বা বহুআণবিক আয়ন এর অভিন্ন আণবিক সংকেত যাদের প্রতিটি উপাদান এ পরমাণুর সংখ্যা একই কিন্তু পরমাণুর বিন্যাস স্বতন্ত্র হয়। [১] সমাণুর সম্ভাবণার কারণেই ঘটে সমাণুকরণ বা সমাবয়বতা এর অস্তিত্ব।
সমাণু একই রকমের বা অনুরূপ রাসায়নিক বা ভৌত ধর্ম পালন করে না। সমাণুকরণের দুটি প্রধান রূপ হ'ল কাঠামোগত বা গঠনগত সমাণুকরণ এবং স্টেরিওসমাণুকরণ বা স্থানিক সমাণুকরণ বা ত্রিমাত্রিক সমাণুকরণ। এর মধ্যে কাঠামোগত সমাণুকরণে পরমাণুগুলির মধ্যে বন্ধন ভিন্ন হয় এবং স্টেরিওসমাণুকরণের ক্ষেত্রে বন্ধনগুলি একই হয় কিন্তু পরমাণুগুলির আপেক্ষিক অবস্থান পৃথক হয়।
সমাণুক সম্পর্কগুলি একটি শ্রেণিবিন্যাস গঠন করে। দুটি রাসায়নিক একই কাঠামোগত সমাণু হতে পারে কিন্তু গভীর বিশ্লেষণের পরে দেখা যেতে পারে তারা একে অপরের স্টেরিওসমাণু। দুটি অণু যারা পরস্পরে একই স্টেরিওসমাণু তারা বিভিন্ন রূপগত আকারের হতে পারে অথবা হতে পারে ভিন্ন আইসোটোপোলগ যা বিশ্লেষণের গভীরতা অধ্যয়নের ক্ষেত্রের উপর নির্ভর করে অথবা আগ্রহের রাসায়নিক এবং ভৌত ধর্মের উপর নির্ভর করে।
ইংরেজি শব্দ "(isomer) আইসোমার" (/ˈaɪsəmər/) হ'ল "(isomeric) আইসোমেরিক" এর একটি ফিরতি গঠন [২] যা সুইডিশ শব্দ (isomerisk) আইসোমরিস্ক থেকে জার্মান (isomerisch) আইসোমরিচ এর মাধ্যমে ধার করে এসেছে।[৩] যার ফলে গ্রীক ἰσόμερoς ('isómeros যার মূল isos = "সমান" এবং méros = "অংশ") থেকে তৈরি হয়েছিল।

সমাণুর গঠন
[সম্পাদনা]গাঠনিক সমাণু
[সম্পাদনা]কাঠামোগত সমাণু এর প্রতিটি উপাদানে একই সংখ্যক অণু (তাই একই আণবিক সংকেত) থাকে। তবে পরমাণুগুলি যুক্তিযুক্তভাবে পৃথক উপায়ে সংযুক্ত থাকে।[৪]
গাঠনিক সমাণুর প্রকারভেদ হলো:[৫]
- শিকল সমাণু
- অবস্থান সমাণু
- কার্যকরী মূলক সমাণু
- মেটামারিজম
- টটোমার
উদাহরণ: C
3H
8O
[সম্পাদনা]উদাহরণ, তিনটি স্বতন্ত্র যৌগ রয়েছে যাদের আণবিক সংকেত C
3H
8O:
3H
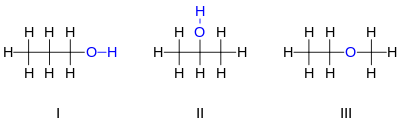
8O: I 1-propanol, II 2-propanol, III ethyl-methyl-ether.
C
3H
8O এর দুটি সমাণু হল প্রপানল অর্থাৎ প্রপেন থেকে প্রাপ্ত অ্যালকোহল। উভয়ের তিনটি কার্বন পরমাণুর একটি শৃঙ্খলা রয়েছে যা এক বন্ধন দ্বারা সংযুক্ত রয়েছে। অবশিষ্ট কার্বন যোজ্যতা সাতটি হাইড্রোজেন পরমাণু দ্বারা এবং একটি হাইড্রোক্সিল মূলক –OH (একটি হাইড্রোজেন পরমাণুর সাথে আবদ্ধ অক্সিজেন পরমাণু ) দ্বারা পরিপূর্ণ হয়। এই দুই সমাণুর কার্বনের সাথে আবদ্ধ হাইড্রোক্সিলের বন্ধনের পার্থক্য: কার্বন শৃঙ্খলের এক প্রান্তে প্রোপান-১-অল (১-প্রোপান, n-প্রোপাইল অ্যালকোহল, n-প্রপানল; I) বা মাঝের কার্বনে প্রোপান-২-অল (২-প্রপানল, আইসোপ্রোপাইল অ্যালকোহল, আইসোপ্রোপানল; II)। এগুলিকে ঘনীভূত কাঠামোগত সংকেত দ্বারা বর্ণনা করা যেতে পারে H
3C–CH
2–CH
2OH এবং H
3C–CH(OH)–CH
3
C
3H
8O এর তৃতীয় সমাণু হল ইথার মিথোক্সিইথেন (ইথাইল-মিথাইল-ইথার)। অন্য দুটির থেকে এটি পৃথক। এতে অক্সিজেন পরমাণু দুটি কার্বনের সাথে সংযুক্ত এবং আটটি হাইড্রোজেনই সরাসরি কার্বনের সাথে বন্ধন দ্বারা যুক্ত। এর ঘনীভূত কাঠামোগত সংকেত H
3C–O–CH
2–CH
3
অ্যালকোহল "৩-প্রোপানল" অন্য আর একটি সমাণু নয়। কারণ এটির সাথে ১-প্রোপানলের পার্থক্য প্রকৃত নয়। এটি কেবল শৃঙ্খল বরাবর কার্বনগুলির ক্রম অনুসারে একটি স্বেচ্ছাসেবী পছন্দের ফলাফল। একই কারণে "এথোক্সিমিথেন" অন্য সমাণু নয়।.
১-প্রোপানল এবং ২-প্রোপানল হ'ল অবস্থানগত সমাণু যা তার অবস্থানের দ্বারা কিছু কিছু বৈশিষ্টের ক্ষেত্রে পৃথক হয়। যেমন দ্বি বন্ধন বা কার্যকরী মূলক এর মতো কিছু বৈশিষ্ট্য "পিতৃ" অণুতে ঘটে (এ ক্ষেত্রে প্রোপেন এ)।
উদাহরণ: C
3H
4
[সম্পাদনা]এছাড়াও হাইড্রোকার্বন এরও তিনটি কাঠামোগত সমাণু রয়েছে C
3H
4:

|
|

|
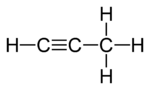
| I প্রোপাডিন | III প্রোপাইন | II সাইক্লোপ্রোপিন |
সমাণুর দুটিতে তিনটি কার্বন পরমাণু একটি মুক্ত শৃঙ্খলে সংযুক্ত। তবে এর মধ্যে একটিতে (প্রোপাডিন, অ্যালিন; I) কার্বন দুটি দ্বি বন্ধন এর দ্বারা সংযুক্ত। অপর দিকে (প্রোপাইন, III) এ তারা এক বন্ধন এবং ত্রি বন্ধন দ্বারা সংযুক্ত থাকে। তৃতীয় সমাণুতে (সাইক্লোপ্রোপিন; II)) তিনটি কার্বন দুটি এক বন্ধন এবং একটি দ্বি বন্ধন দ্বারা একটি বলয়ে সংযুক্ত থাকে। তিনটিরই কার্বন পরমাণুর অবশিষ্ট যোজ্যতা চারটি হাইড্রোজেন দ্বারা তুষ্ট হয়।
আবারও দ্রষ্টব্য যে ত্রি বন্ধনের সাথে কেবলমাত্র একটি কাঠামোগত সমাণু রয়েছে। কারণ সেই বন্ধনের অন্যান্য সম্ভাব্য স্থান নির্ধারণের ফলে কেবল তিনটি কার্বনকে একটি আলাদা ক্রমে বিন্যস্ত করা হচ্ছে। একই কারণে কেবল তিনটি নয় একটিই সাইক্লোপ্রোপিন রয়েছে।
টটোমার
[সম্পাদনা]টটোমার হলো গাঠনিক সমাণু। এতে সহজেই আন্তঃরূপান্তর ঘটে যাতে দুই বা ততোধিক প্রজাতি H–X–Y=Z ![]() X=Y–Z–H. এর মতো ভারসাম্যে সহাবস্থান করে। [৬] গুরুত্বপূর্ণ উদাহরণ হ'ল কিটো-ইনোল টটোমারিজম এবং নিরপেক্ষর ও একটি অ্যামাইনো অ্যাসিড এর জুইটেরিয়নিক আকারের মধ্যে ভারসাম্য রক্ষা করে।
X=Y–Z–H. এর মতো ভারসাম্যে সহাবস্থান করে। [৬] গুরুত্বপূর্ণ উদাহরণ হ'ল কিটো-ইনোল টটোমারিজম এবং নিরপেক্ষর ও একটি অ্যামাইনো অ্যাসিড এর জুইটেরিয়নিক আকারের মধ্যে ভারসাম্য রক্ষা করে।
অনুরণন ফর্ম
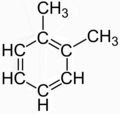
[সম্পাদনা]কিছু অণুর কাঠামোকে মাঝে মাঝে বেশ কয়েকটি দৃশ্যত বিভিন্ন কাঠামোগত সমাণুর মধ্যে অনুরণন হিসাবে বর্ণনা করা হয়। এর আদর্শ উদাহরণ হ'ল ১,২-মিথাইলবেনজিন (o-জাইলিন) যা প্রায়ই দুটি আপাত স্বতন্ত্র কাঠামোগত সমাণুর মিশ্রণ হিসাবে বর্ণনা করা হয়:

|
|
অবশ্য এই দুই কাঠামোর কোনওটিই কোনও বাস্তব যৌগের বর্ণনা দেয় না। এগুলি (তাদের "গড়" বা "অনুরণন" দ্বারা) বর্ণনা করার উপায় হিসাবে রচিত হয়েছে। এ গুলি o-জাইলিন এর প্রকৃত ডিলোকালাইজড বন্ধন যা একটি বেনজিন কোর এর সাথে সংশ্লিষ্ট অবস্থানে দুটি মিথাইল মূলকের C
8H
10 একক সমাণু হয়।
ত্রিমাত্রিক সমাণু
[সম্পাদনা]ত্রিমাত্রিক সমাণু বা স্টেরিও সমাণু যে সব যৌগের আণবিক ও গাঠনিক সংকেত একই কিন্তু বিভিন্ন পরমাণু ও মূলকের ত্রিমাত্রিক অবস্থান বিন্যাসের কারণে তাদের ভৌত ও রাসায়নিক ধর্মের পার্থক্য দেখা যায় সে সব যৌগকে ত্রিমাত্রিক সমাণু এবং তাদের এই ধর্মকে ত্রিমাত্রিক বা স্টেরিও সমাণুতা বলা হয়।
জ্যামিতিক সমাণুগুলি একই ধরনের বন্ধন দ্বারা সংযুক্ত একই পরমাণু বা আইসোটোপ থাকে। কিন্তু আবর্তন এবং ট্রাশ্লেশন বা অনুবাদ ছাড়াও মহাশূণ্যে ঐ সব পরমাণুর আপেক্ষিক অবস্থানে তাদের আকারের ভিন্নতা দেখা যায়।
তত্ত্ব অনুসারে অণু বা আয়নে পরমাণুর বিশেষ বিন্যাস ধীরে ধীরে অসীমভাবে বিভিন্ন উপায়ে উপযুক্ত পথ বরাবর পরিবর্তন করে যাওয়ার কল্পনা করা যেতে পারে। তবে পরমাণুর অবস্থানের পরিবর্তনগুলি সাধারণত একটি অণুর আভ্যন্তরীণ শক্তির পরিবর্তন করবে যা প্রতিটি পরমাণুর বন্ধনের মধ্যবর্তী কোণগুলির সাথে এবং পরমাণুর মধ্যের দূরত্ব দ্বারা নির্ধারিত হয় (তারা বন্ধনযুক্ত হক বা হক)।
জ্যামিতিক সমাণুর প্রকারভেদ হলো:[৫]
- জ্যামিতিক সমাণু বা সিস-ট্রান্স সমাণু
- আলোক সমাণু
তথ্যসূত্র
[সম্পাদনা]- ↑ Petrucci, Ralph H.; Harwood, William S.; Herring, F. Geoffrey (২০০২)। General chemistry: principles and modern applications
 (8th সংস্করণ)। Upper Saddle River, N.J: Prentice Hall। পৃষ্ঠা 91]। আইএসবিএন 978-0-13-014329-7। এলসিসিএন 2001032331। ওসিএলসি 46872308।
(8th সংস্করণ)। Upper Saddle River, N.J: Prentice Hall। পৃষ্ঠা 91]। আইএসবিএন 978-0-13-014329-7। এলসিসিএন 2001032331। ওসিএলসি 46872308।
- ↑ Merriam-Webster: "isomer" online dictionary entry. Accessed on 2020-08-26
- ↑ Merriam-Webster: "isomeric" online dictionary entry. Accessed on 2020-08-26
- ↑ Smith, Janice Gorzynski (২০১০)। General, Organic and Biological Chemistry (1st সংস্করণ)। McGraw-Hill। পৃষ্ঠা 450। আইএসবিএন 978-0-07-302657-2।
- ↑ ক খ "জৈব রসায়নের সূচনা" (পিডিএফ)।
- ↑ "tautomerism"। IUPAC Gold Book। IUPAC। সংগ্রহের তারিখ ২১ এপ্রিল ২০১৯।
