হাইপারভ্যালেন্ট অনু
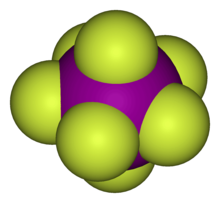
রসায়নে, হাইপারভ্যালেন্ট অণু (ঘটনাটি অষ্টক সম্প্রসারণ নামেও পরিচিত) হল একটি অণু যা এক বা একাধিক প্রধান শ্রেণী উপাদান ধারণ করে যা স্পষ্টতই তাদের শেষ কক্ষপথে আটটিরও বেশি ইলেকট্রন বহন করে। যেমন:ফসফরাস পেন্টাক্লোরাইড (PCl5), সালফার হেক্সাফ্লোরাইড (SF6), ক্লোরিন ট্রাইফ্লুরাইড (ClF3), ক্লোরিট (ClO–2) আয়ন, এবং ট্রাইওডাইড (I–3) আয়ন হাইপারভ্যালেন্ট অণুর উদাহরণ।
সংজ্ঞা এবং নামকরণ
[সম্পাদনা]হাইপারভ্যালেন্ট অণুগুলিকে প্রথম আনুষ্ঠানিকভাবে ১৯৬৯ সালে জেরেমি আই. মুশার দ্বারা সংজ্ঞায়িত করেন যে গ্রুপ ১৫-১৮ এর কেন্দ্রীয় পরমাণু সর্বনিম্ন যোজনী ব্যাতিত অন্য কোনো যোজনীতে (যেমন:১৫, ১৬, ১৭, ১৮ গ্রুপ এর ৩, ২, ১, ০ যোজনীবিশিষ্ট মৌলগুলো , অষ্টক নিয়ম মেনেচলে)[১]
হাইপারভ্যালেন্ট অণুর বেশ কয়েকটি নির্দিষ্ট শ্রেণী বিদ্যমান:
- জৈব রসায়নে হাইপারভ্যালেন্ট আয়োডিন যৌগগুলি কার্যকরী বিকারক (e.g. ডেস-মার্টিন পিরিওডিনেন)
- টেট্রা-, পেন্টা- এবং হেক্সাভ্যালেন্ট ফসফরাস, সিলিকন এবং সালফার যৌগ (যেমন: PCl5, PF5, SF6, সালফিরানস এবং পারসালফুরানস)
- নিষ্ক্রিয় গ্যাস যৌগ (যেমন জেনন টেট্রাফ্লোরাইড, XeF4)
- হ্যালোজেন পলিফ্লোরাইড (যেমন ক্লোরিন পেন্টাফ্লোরাইড, ClF5)
N-X-L স্বরলিপি
[সম্পাদনা]N-X-L নামকরণ, ১৯৮০ সালে মার্টিন, আরডুয়েঙ্গো এবং কোচির গবেষণা শ্রেণী দ্বারা যৌথভাবে প্রবর্তিত,[২] প্রায়শই প্রধান গ্রুপ উপাদানগুলির হাইপারভ্যালেন্ট যৌগগুলিকে শ্রেণীবদ্ধ করতে ব্যবহৃত হয়, যেখানে:
- N যোজনী ইলেকট্রনের সংখ্যা উপস্থাপন করে
- X কেন্দ্রীয় পরমাণুর রাসায়নিক প্রতীক নির্দেশ করে
- L কেন্দ্রীয় পরমাণুতে লিগ্যান্ডের সংখ্যা
N-X-L নামকরণের উদাহরণগুলির মধ্যে রয়েছে:
- XeF 2, 10-Xe-2
- PCl 5, 10-P-5
- SF 6, 12-S-6
- IF 7, 14-I-7
তথ্যসূত্র
[সম্পাদনা]- ↑ Musher, J.I. (১৯৬৯)। "The Chemistry of Hypervalent Molecules": 54–68। ডিওআই:10.1002/anie.196900541।
- ↑ Perkins, C. W.; Martin, J. C. (১৯৮০)। "An Electrically Neutral σ-Sulfuranyl Radical from the Homolysis of a Perester with Neighboring Sulfenyl Sulfur: 9-S-3 species": 7753–7759। ডিওআই:10.1021/ja00546a019।
