ফেরিক ক্লোরাইড: সংশোধিত সংস্করণের মধ্যে পার্থক্য
Firuz Ahmmed (আলোচনা | অবদান) |
Firuz Ahmmed (আলোচনা | অবদান) |
||
| ১৭৩ নং লাইন: | ১৭৩ নং লাইন: | ||
===ক্ষার ধাতু অ্যালকক্সাইডের সহিত=== |
===ক্ষার ধাতু অ্যালকক্সাইডের সহিত=== |
||
ক্ষারীয় ধাতু অ্যালকক্সাইড বিভিন্ন ধরণের জটিলের সাথে বিক্রিয়া করে ধাতব অ্যালকক্সাইড জটির গঠন করে।<ref>{{Cite book|url=https://books.google.com/books?id=rPzaMRjK8pQC|title=The Chemistry of Metal Alkoxides|last=|first=|publisher=Springer Science|year=2002|isbn=0306476576|veditors=Turova NY, Turevskaya EP, Kessler VG, Yanovskaya MI|location=|pages=481|chapter=12.22.1 Synthesis|display-editors=3}}</ref> যৌগসমূহ ডাইমারিক বা ট্রাইমারিক হতে পারে।<ref>{{Cite book|title=Alkoxo and aryloxo derivatives of metals|vauthors=Bradley DC, Mehrotra RC, Rothwell I, Singh A|publisher=Academic Press|year=2001|isbn=9780121241407|location=San Diego|pages=69|chapter=3.2.10. Alkoxides of later 3d metals|oclc=162129468|display-authors=3|chapter-url=https://books.google.com/books?id=ixNEpx8aDHUC&pg=PA69}}</ref> কঠিন পর্যায়ে FeCl<sub>3</sub> এবং সোডিয়াম ইথোক্সাইডের মধ্যে নূন্যতম স্টোয়িচোমেট্রিক বিক্রিয়ার ফলে বিভিন্ন মাল্টিনিউক্লিয়ার জটিল গঠিত হয়:<ref> |
|||
{{cite journal|vauthors=Michael V, Grätz F, Huch V|year=2001|title={{Chem2|Fe9O3(OC2H5)21·C2H5OH}}—A New Structure Type of an Uncharged Iron(III) Oxide-Alkoxide Cluster|url=|journal=[[European Journal of Inorganic Chemistry|Eur. J. Inorg. Chem.]]|volume=2001|issue=2|pages=367|doi=10.1002/1099-0682(200102)2001:2<367::AID-EJIC367>3.0.CO;2-V}}</ref><ref> |
|||
{{cite journal|display-authors=3|vauthors=Seisenbaeva GA, Gohil S, Suslova EV, Rogova TV, Turova NY, Kessler VG|year=2005|title=The synthesis of iron (III) ethoxide revisited: Characterization of the metathesis products of iron (III) halides and sodium ethoxide|url=|journal=[[Inorganica Chimica Acta|Inorganica Chim. Acta]]|volume=358|issue=12|pages=3506–3512|doi=10.1016/j.ica.2005.03.048}}</ref> |
|||
:<chem>FeCl3 + 3 [C2H5O]- Na+ -> Fe(OC2H5)3 + 3 NaCl</chem> |
|||
===অর্গানোমেটালিক যৌগের সাথে=== |
===অর্গানোমেটালিক যৌগের সাথে=== |
||
১৯:৪০, ২৩ অক্টোবর ২০২০ তারিখে সংশোধিত সংস্করণ
 Iron(III) chloride (hydrate)
| |||
 Iron(III) chloride (anhydrous)
| |||
| |||
| নামসমূহ | |||
|---|---|---|---|
| ইউপ্যাক নামs
Iron(III) chloride
Iron trichloride | |||
অন্যান্য নাম
| |||
| শনাক্তকারী | |||
| |||
ত্রিমাত্রিক মডেল (জেমল)
|
|||
| সিএইচইবিআই | |||
| কেমস্পাইডার | |||
| ইসিএইচএ ইনফোকার্ড | ১০০.০২৮.৮৪৬ | ||
| ইসি-নম্বর |
| ||
পাবকেম CID
|
|||
| আরটিইসিএস নম্বর |
| ||
| ইউএনআইআই |
| ||
| ইউএন নম্বর |
| ||
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|||
| |||
| |||
| বৈশিষ্ট্য | |||
| FeCl3 | |||
| আণবিক ভর |
| ||
| বর্ণ | প্রতিফলিত আলোক মাধ্যমে কালচে-সবুজ; সঞ্চারিত আলোক মাধ্যমে বেগুনি-লাল; হেক্সাহাইড্রেট হিসাবে কঠিন হলুদ; জলীয় দ্রবনে বাদামী রঙের | ||
| গন্ধ | সামান্য HCl | ||
| ঘনত্ব |
| ||
| গলনাঙ্ক | ৩০৭.৬ °সে (৫৮৫.৭ °ফা; ৫৮০.৮ K) (অনার্দ্র) ৩৭ °সে (৯৯ °ফা; ৩১০ K) (hexahydrate)[১] | ||
| স্ফুটনাঙ্ক |
| ||
| ৯১২ গ্রাম/লিটার অনার্দ্র বা হেক্সাহাইড্রেট, ২৫ °সে)[১] | |||
| দ্রাব্যতা |
| ||
| +১৩,৪৫০·১০−৬ সেমি৩/মোল[২] | |||
| সান্দ্রতা | 12 cP (40% solution) | ||
| গঠন | |||
| স্ফটিক গঠন | Hexagonal, hR24 | ||
| Space group | R3, No. 148[৩] | ||
| Lattice constant | |||
এককের সূত্রসমূহ (Z)
|
6 | ||
| Coordination geometry |
Octahedral | ||
| ঝুঁকি প্রবণতা[৫][৬][Note ১] | |||
| নিরাপত্তা তথ্য শীট | টেমপ্লেট:ICSC-small | ||
| জিএইচএস চিত্রলিপি |  
| ||
| জিএইচএস সাংকেতিক শব্দ | বিপদজনক | ||
| জিএইচএস বিপত্তি বিবৃতি | H290, H302, H314, H318 | ||
| জিএইচএস সতর্কতামূলক বিবৃতি | P234, P260, P264, P270, P273, P280, P301+312, P301+330+331, P303+361+353, P363, P304+340, P310, P321, P305+351+338 | ||
| এনএফপিএ ৭০৪ | |||
| ফ্ল্যাশ পয়েন্ট | Non-flammable | ||
| যুক্তরাষ্ট্রের স্বাস্থ্য অনাবৃতকরণ সীমা (NIOSH): | |||
REL (সুপারিশকৃত)
|
TWA 1 mg/m3[৪] | ||
| সম্পর্কিত যৌগ | |||
অন্যান্য অ্যানায়নসমূহ
|
|||
অন্যান্য ক্যাটায়নসমূহ
|
|||
সম্পর্কিত দম্বল
|
|||
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |||
| তথ্যছক তথ্যসূত্র | |||
আয়রন(III) ক্লোরাইড একটি অজৈব যৌগ এর রাসায়নিক সংকেত (FeCl3)। একে ফেরিক ক্লোরাইডও বলা হয়, এটি +৩ জারণ মানের লোহার একটি সাধারণ যৌগ। অনাদ্র্র যৌগটি কঠিন স্ফটিকাকার এবং এর গলনাঙ্ক ৩০৭.৬ ডিগ্রি সেন্টিগ্রেড। এর রঙ দেখার কোণের উপর নির্ভর করে: প্রতিফলিত আলোক মাধ্যমে স্ফটিকের রঙ গাঢ় সবুজ দেখা যায় অপরদিকে সঞ্চারিত আলোক মাধ্যমে একে বেগুনি-লাল দেখা যায়।
গঠন এবং বৈশিষ্ট্যাবলী
অনার্দ্র
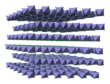
অনার্দ্র ফেরিক ক্লোরাইডের দ্বি-তুল্য ক্লোরাইড লিগ্যান্ডসমূহ পরস্পর সংযুক্ত অক্টাহেড্রাল Fe(III) কেন্দ্রের সাথে BiI3 কাঠামো রয়েছে।[৩]
ফেরিক ক্লোরাইডের গলনাঙ্ক তুলনামূলকভাবে কম এবং এর স্ফুটনাঙ্ক প্রায় ৩১৫ ডিগ্রি সেন্টিগ্রেড। বাষ্পে Fe2Cl6 (তুলনা: অ্যালুমিনিয়াম ক্লোরাইড) ডাইমার থাকে যা উচ্চ তাপমাত্রায় ক্রমবর্ধমান মনোমেরিক FeCl3 (D3h প্রতিসম গ্রুপের আণবিক প্রতিসাম্য) এ বিয়োজিত হয়ে বিপরীতমুখী বিশ্লেষণের মাধ্যমে ফেরাস ক্লোরাইড এবং ক্লোরিন গ্যাস উৎপন্ন করে।[৮]
হাইড্রেট
অনার্দ্র উপাদান ছাড়াও ফেরিক ক্লোরাইড চারটি হাইড্রেট গঠন করে। ফেরিক ক্লোরাইডের সকল গঠনের লিগ্যান্ড হিসাবে দুই বা দুয়ের অধিক ক্লোরাইড বৈশিষ্ট্যযুক্ত এবং তিনটি হাইড্রেট FeCl4− বৈশিষ্ট্যযুক্ত।[৯]
- হেক্সাহাইড্রেট: FeCl3.6H2O এর গাঠনিক সংকেত ট্রান্স-[Fe(H2O)4Cl2]Cl.2H2O
- FeCl3.2.5H2O এর গাঠনিক সংকেত সিস-[Fe(H2O)4Cl2][FeCl4].H2O.
- ডাইহাইড্রেট: FeCl3.2H2O এর গাঠনিক সংকেত ট্রান্স-[Fe(H2O)4Cl2][FeCl4].
- FeCl3.3.5H2O এর গাঠনিক সংকেত সিস-[FeCl2(H2O)4][FeCl4].3H2O.
জলীয় দ্রবণ
ফেরিক ক্লোরাইডের জলীয় দ্রবণ [Fe(H2O)6]3+ এর ম্লান গোলাপী দ্রবণের তুলনায় চরিত্রগতভাবে হলুদ বর্ণের। স্পেকট্রোস্কোপিক পরিমাপন অনুসারে ফেরিক ক্লোরাইডের জলীয় দ্রবণের প্রধান প্রজাতি হল অক্টাহেড্রাল জটিল [FeCl2(H2O)4]+ (স্টেরিওকেমিস্ট্রি অনির্ধারিত) এবং টেট্রাহেড্রাল [FeCl4]−।[৯]
প্রস্তুত প্রণালী
উপাদানসমূহের মিশ্রণ দ্বারা অনার্দ্র ফেরিক ক্লোরাইড প্রস্তুত করা যায়:[১০]
ফেরিক ক্লোরাইডের দ্রবণসমূহ ক্লোজড-লুপ প্রক্রিয়াতে লোহা এবং আকরিক উভয় থেকে শিল্পৎপাদন করা হয়।
- হাইড্রোক্লোরিক অ্যাসিডে লোহার আকরিক দ্রবীভূত করে
- ক্লোরিনের সাথে ফেরাস ক্লোরাইডের জারণ ঘটিয়ে
- অক্সিজেনের সাথে ফেরাস ক্লোরাইডের জারণ ঘটিয়ে
প্রথমে হাইড্রোক্লোরিক অ্যাসিডের সাথে আয়রনের বিক্রিয়া ঘটিয়ে তারপর হাইড্রোজেন পারক্সাইডের বিক্রিয়ার মাধ্যমে অল্প পরিমাণে উৎপাদন করা যায়। ফেরাস ক্লোরাইডকে ফেরিক ক্লোরাইডে পরিণত করতে হাইড্রোজেন পারক্সাইড হল জারক।
হাইড্রেটকে উত্তপ্ত করে অনার্দ্র ফেরিক ক্লোরাইড পাওয়া যায় না। বরং বিশ্লিষ্ট হয়ে HCl এবং আয়রন অক্সিক্লোরাইডে বিভক্ত হয়। থায়োনিল ক্লোরাইড দিয়ে রূপান্তরটি সম্পাদন করা যায়।[১১] একইভাবে ট্রাইমেথিলসিলাইল ক্লোরাইড দ্বারা নিরুদন প্রভাবিত হয়:[১২]
বিক্রিয়া

ফেরিক ক্লোরাইড হাইড্রোলাইসিস এর দ্বারা একটি শক্তিশারী অম্লীয় দ্রবণ উৎপন্ন করে।[১৩][৯]
৩৫০ °সে এ ফেরিক অক্সাইড দিয়ে উত্তপ্ত করা হলে তখন ফেরিক ক্লোরাইড কঠিন স্তরযুক্ত আয়রন অক্সিক্লোরাইড উৎপন্ন করে।[১৪]
অ্যানহাইড্রস লবণ একটি মাঝারি শক্তিশালী লুইস অ্যাসিড, যা ট্রাইফিনাইলফসফিন অক্সাইডের মতো লুইস ক্ষারক উৎপাদন করে; উদাহরণস্বরূপ, FeCl3(OPPh3)2 এখানে Ph হচ্ছে ফিনাইল। এটি অন্যান্য ক্লোরাইড লবণের সাথেও বিক্রিয়া করে হলুদ বর্ণের টেট্রাহেড্রাল [FeCl4]− আয়ন উৎপন্ন করে। হাইড্রোক্লোরিক অ্যাসিডে [FeCl4]− এর লবণ ডাইইথাইল ইথারের মাধ্যমে নিষ্কাশিত করা যায়।
জারণ-বিজারণ বিক্রিয়া
আয়রন(III) ক্লোরাইড একটি হালকা অক্সিডাইজিং এজেন্ট উদাহরণস্বরূপ, এটি কপার(I) ক্লোরাইডকে জারিত করে কপার(II) ক্লোরাইড উৎপাদন করতে সক্ষম।
এটি আয়রনের সাথেও বিক্রিয়া করে ফেরাস ক্লোরাইড গঠন করে:
অনার্দ্র ফেরাস ক্লোরাইডের একটি ঐতিহ্যবাহী সংশ্লেষণ হল ক্লোরোবেঞ্জিনের সাথে FeCl3 এর বিজারণ:[১৫]
কার্বক্সিলেট অ্যানায়নের সহিত
অক্সালেট জলীয় ফেরিক ক্লোরাইডের সাথে দ্রুত বিক্রিয়া করে [Fe(C2O4)3]3- উৎপাদন করে। অন্যান্য কার্বক্সিলেট লবণ জটিল গঠন করে; যেমন সাইট্রেট এবং টার্ট্রেট।
ক্ষার ধাতু অ্যালকক্সাইডের সহিত
ক্ষারীয় ধাতু অ্যালকক্সাইড বিভিন্ন ধরণের জটিলের সাথে বিক্রিয়া করে ধাতব অ্যালকক্সাইড জটির গঠন করে।[১৬] যৌগসমূহ ডাইমারিক বা ট্রাইমারিক হতে পারে।[১৭] কঠিন পর্যায়ে FeCl3 এবং সোডিয়াম ইথোক্সাইডের মধ্যে নূন্যতম স্টোয়িচোমেট্রিক বিক্রিয়ার ফলে বিভিন্ন মাল্টিনিউক্লিয়ার জটিল গঠিত হয়:[১৮][১৯]
অর্গানোমেটালিক যৌগের সাথে
ব্যবহার
শিল্পকারখানায়
পরীক্ষাগারে ব্যবহার
অন্যান্য ব্যবহার
নিরাপত্তা
ফেরিক ক্লোরাইড ক্ষতিকারক, অত্যন্ত ক্ষয়কারক এবং অম্লীয়। অনার্দ্র ফেরিক ক্লোরাইড একটি শক্তিশালী ডিহাইড্রেটিং এজেন্ট।
যদিও মানুষের মধ্যে এর বিষক্রিয়ার তথ্য খুব কমই জানা যায় তবে ফেরিক ক্লোরাইড গ্রহণের ফল মারাত্মক অসুস্থতা এবং মৃত্যুর কারণ হতে পারে। অযথাযথ লেবেল আঁটা এবং সংরক্ষণের কারণে দুর্ঘটনাক্রমে খেয়ে ফেলে বা ভুল রোগ নির্ণয়ের দিকে পরিচালিত করে। প্রাথমিকভাবে রোগ নির্ণয় গুরুত্বপূর্ণ বিশেষত মারাত্মকভাবে বিষাক্রান্ত রোগীদের ক্ষেত্রে।
আরও দেখুন
টীকা
তথ্যসূত্র
- ↑ ক খ গ ঘ ঙ চ হেইন্স, উইলিয়াম এম., সম্পাদক (২০১১)। সিআরসি হ্যান্ডবুক অব কেমিস্ট্রি এন্ড ফিজিক্স [রসায়ন ও পদার্থ বিজ্ঞানের সিআরসি হস্তপুস্তিকা] (ইংরেজি ভাষায়) (৯২তম সংস্করণ)। বোকা রটন, ফ্লোরিডা: সিআরসি প্রেস। পৃষ্ঠা 4.69। আইএসবিএন 1439855110।
- ↑ হেইন্স, উইলিয়াম এম., সম্পাদক (২০১১)। সিআরসি হ্যান্ডবুক অব কেমিস্ট্রি এন্ড ফিজিক্স [রসায়ন ও পদার্থ বিজ্ঞানের সিআরসি হস্তপুস্তিকা] (ইংরেজি ভাষায়) (৯২তম সংস্করণ)। বোকা রটন, ফ্লোরিডা: সিআরসি প্রেস। পৃষ্ঠা 4.133। আইএসবিএন 1439855110।
- ↑ ক খ Hashimoto S, Forster K, Moss SC (১৯৮৯)। "Structure refinement of an FeCl3 crystal using a thin plate sample"। J. Appl. Crystallogr.। 22 (2): 173। ডিওআই:10.1107/S0021889888013913। templatestyles stripmarker in
|title=at position 28 (সাহায্য) - ↑ "NIOSH Pocket Guide to Chemical Hazards #0346" (ইংরেজি ভাষায়)। ন্যাশনাল ইনস্টিটিউট ফর অকুপেশনাল সেফটি অ্যান্ড হেলথ (NIOSH)।
- ↑ টেমপ্লেট:GHS class NZ
- ↑ Various suppliers, collated by the Baylor College of Dentistry, Texas A&M University. (accessed 2010-09-19)
- ↑ টেমপ্লেট:GHS class JP
- ↑ Holleman AF, Wiberg E (২০০১)। Wiberg N, সম্পাদক। Inorganic Chemistry। San Diego: Academic Press। আইএসবিএন 978-0-12-352651-9।
- ↑ ক খ গ Simon A. Cotton (২০১৮)। "Iron(III) chloride and its coordination chemistry"। Journal of Coordination Chemistry। 71 (21): 3415–3443। এসটুসিআইডি 105925459। ডিওআই:10.1080/00958972.2018.1519188।
- ↑ Tarr BR, Booth HS, Dolance A (১৯৫০)। "Anhydrous Iron(III) Chloride"। Audrieth LF। Inorganic Syntheses। 3। McGraw-Hill Book Company, Inc.। পৃষ্ঠা 191–194। আইএসবিএন 9780470132340। ডিওআই:10.1002/9780470132340.ch51।
- ↑ Pray AR, Heitmiller RF, Strycker S, ও অন্যান্য (১৯৯০)। "Anhydrous Metal Chlorides"। Angelici RJ। Inorganic Syntheses। 28। পৃষ্ঠা 321–323। আইএসবিএন 9780470132593। ডিওআই:10.1002/9780470132593.ch80।
- ↑ Boudjouk P, So JH, Ackermann MN, ও অন্যান্য (১৯৯২)। "Solvated and Unsolvated Anhydrous Metal Chlorides from Metal Chloride Hydrates"। Grimes RN। Inorganic Syntheses। 29। পৃষ্ঠা 108–111। আইএসবিএন 9780470132609। ডিওআই:10.1002/9780470132609.ch26।
- ↑ Housecroft, C. E.; Sharpe, A. G. (২০১২)। Inorganic Chemistry (4th সংস্করণ)। Prentice Hall। পৃষ্ঠা 747। আইএসবিএন 978-0-273-74275-3।
- ↑ Kikkawa S, Kanamaru F, Koizumi M, ও অন্যান্য (১৯৮৪)। "Layered Intercalation Compounds"। Holt SL Jr। Inorganic Syntheses। John Wiley & Sons, Inc.। পৃষ্ঠা 86–89। আইএসবিএন 9780470132531। ডিওআই:10.1002/9780470132531.ch17।
- ↑ P. Kovacic and N. O. Brace (১৯৬০)। "Iron(II) Chloride"। Inorganic Syntheses। Inorg. Synth.। Inorganic Syntheses। 6। পৃষ্ঠা 172–173। আইএসবিএন 9780470132371। ডিওআই:10.1002/9780470132371.ch54।
- ↑ Turova NY, Turevskaya EP, Kessler VG, ও অন্যান্য, সম্পাদকগণ (২০০২)। "12.22.1 Synthesis"। The Chemistry of Metal Alkoxides। Springer Science। পৃষ্ঠা 481। আইএসবিএন 0306476576।
- ↑ Bradley DC, Mehrotra RC, Rothwell I, ও অন্যান্য (২০০১)। "3.2.10. Alkoxides of later 3d metals"। Alkoxo and aryloxo derivatives of metals। San Diego: Academic Press। পৃষ্ঠা 69। আইএসবিএন 9780121241407। ওসিএলসি 162129468।
- ↑
Michael V, Grätz F, Huch V (২০০১)। "Fe9O3(OC2H5)21·C2H5OH—A New Structure Type of an Uncharged Iron(III) Oxide-Alkoxide Cluster"। Eur. J. Inorg. Chem.। 2001 (2): 367। ডিওআই:10.1002/1099-0682(200102)2001:2<367::AID-EJIC367>3.0.CO;2-V। templatestyles stripmarker in
|title=at position 1 (সাহায্য) - ↑ Seisenbaeva GA, Gohil S, Suslova EV, ও অন্যান্য (২০০৫)। "The synthesis of iron (III) ethoxide revisited: Characterization of the metathesis products of iron (III) halides and sodium ethoxide"। Inorganica Chim. Acta। 358 (12): 3506–3512। ডিওআই:10.1016/j.ica.2005.03.048।
আরও পড়ুন
- Lide DR, সম্পাদক (১৯৯০)। CRC Handbook of Chemistry and Physics (71st সংস্করণ)। Ann Arbor, MI, USA: CRC Press। আইএসবিএন 9780849304712।
- Stecher PG, Finkel MJ, Siegmund OH, সম্পাদকগণ (১৯৬০)। The Merck Index of Chemicals and Drugs (7th সংস্করণ)। Rahway, NJ, USA: Merck & Co।
- Nicholls D (১৯৭৪)। Complexes and First-Row Transition Elements, Macmillan Press, London, 1973.। A Macmillan chemistry text। London: Macmillan Press। আইএসবিএন 9780333170885।
- Wells AF (১৯৮৪)। Structural Inorganic Chemistry। Oxford science publications (5th সংস্করণ)। Oxford, UK: Oxford University Press। আইএসবিএন 9780198553700।
- March J (১৯৯২)। Advanced Organic Chemistry (4th সংস্করণ)। New York: John Wiley & Sons, Inc.। পৃষ্ঠা 723। আইএসবিএন 9780471581482।
- Reich HJ, Rigby HJ, সম্পাদকগণ (১৯৯৯)। Acidic and Basic Reagents। Handbook of Reagents for Organic Synthesis। New York: John Wiley & Sons, Inc.। আইএসবিএন 9780471979258।












![{\displaystyle {\ce {FeCl3 + 3 [C2H5O]- Na+ -> Fe(OC2H5)3 + 3 NaCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/ddc3c55642250edf274b916c6006e34934890549)
