আয়ন: সংশোধিত সংস্করণের মধ্যে পার্থক্য
ট্যাগ: মোবাইল সম্পাদনা মোবাইল ওয়েব সম্পাদনা |
|||
| ১০৭ নং লাইন: | ১০৭ নং লাইন: | ||
|Chloride (ক্লোরাইড)||Cl<sup>−</sup>|| |
|Chloride (ক্লোরাইড)||Cl<sup>−</sup>|| |
||
|- |
|- |
||
|Fluoride (ফ্লোরাইড)||F<sup>−</sup>|| |
|Fluoride ([[ফ্লোরাইড]])||F<sup>−</sup>|| |
||
|- |
|- |
||
|Hydride (হাইড্রেড)||H<sup>−</sup>|| |
|Hydride (হাইড্রেড)||H<sup>−</sup>|| |
||
১৭:৫৩, ১৬ ফেব্রুয়ারি ২০২০ তারিখে সংশোধিত সংস্করণ
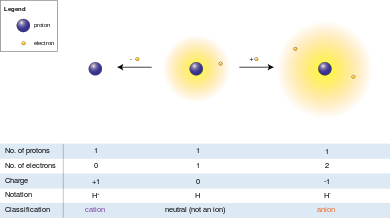
আয়ন (/ˈaɪɒn,
ধণাত্মক(+) বা ঋণাত্মক(–) আধান যুক্ত পরমাণু বা যৌগমূলক কে আয়ন বলা হয়।
সাধারণত সব পরমাণুই আধান নিরপেক্ষ। কারণ তাদের মধ্যে যতটি ধনাত্মক চার্জ যুক্ত প্রোটন থাকে ঠিক ততটিই ঋণাত্মক চার্জ যুক্ত ইলেকট্রন থাকে। তাই সামগ্রিক ভাবে তারা আধান নিরপেক্ষ। তবে প্রতিটি পরমাণুই তাদের নিকটস্থ নিষ্ক্রিয় গ্যাসের স্থিতিশীল ইলেকট্রন বিন্যাস অর্জন করতে চায়। তাই যৌগ গঠন কালে তারা ইলেকট্রন গ্রহণ বা অপসারণ করে।
ইলেকট্রন গ্রহণ বা অপসারণ করার ফলে ইলেকট্রন এবং প্রোটনের সাম্য অবস্থা নষ্ট হয়। ফলে তারা ধনাত্মক(+) বা ঋণাত্মক(–) চার্জ যুক্ত হয়। এই অবস্থাই হল আয়ন।
ক্যাটায়ন
ধাতু সমূহ তাদের সর্বশেষ শক্তিস্তরের এক বা একাধিক ইলেকট্রন অপসারণ করে যে আয়নে পরিণত হয় তাকে ক্যাটায়ন বলে। ক্যাটায়নে প্রোটনের তুলানায় ইলেকট্রন কম থাকায় এর আধান (চার্জ) ধনাত্মক(+)।
ব্যাখ্যা
যেহেতু ধাতু সমূহের সর্বশেষ শক্তিস্তরে ১টি, ২টি বা ৩টি ইলেকট্রন থাকে তাই এদের প্রতি নিউক্লিয়াসের প্রোটনের আকর্ষণ কম থাকে। ফলে, তারা সহজেই ওই ইলেকট্রন গুলো ত্যাগ করতে পারে। সর্বশেষ শক্তিস্তরের ওই ইলেকট্রন গুলো ত্যাগ করলে ধাতব পরমাণু গুলো আর আধান নিরপেক্ষ থাকে না। এগুলো আয়নে পরিণত হয়। এই আয়নই হল ক্যাটায়ন[২]
কিছু ক্যাটায়ন
| সাধারণ নাম | Formula | প্রচলিত নাম |
|---|---|---|
| মৌলের ক্যাটায়ন | ||
| Aluminium (অ্যালুমিনিয়াম) | Al3+ | |
| Barium (বেরিয়াম) | Ba2+ | |
| Beryllium (বেরিলিয়াম) | Be2+ | |
| Calcium (ক্যালসিয়াম) | Ca2+ | |
| Chromium(III) (ক্রোমিয়াম III) | Cr3+ | |
| Copper(I) (কপার I) | Cu+ | cuprous (কিউপ্রাস) |
| Copper(II) (কপার II) | Cu2+ | cupric (কিউপ্রিক) |
| Hydrogen (হাইড্রোজেন) | H+ | |
| Iron(II) (আয়রন II) | Fe2+ | ferrous (ফেরাস) |
| Iron(III) (আয়রন III) | Fe3+ | ferric (ফেরিক) |
| Lead(II) (লেড II) | Pb2+ | plumbous (প্লামবাস) |
| Lead(IV) (লেড IV) | Pb4+ | plumbic (প্লামবিক) |
| Lithium (লিথিয়াম) | Li+ | |
| Magnesium (ম্যাগনেসিয়াম) | Mg2+ | |
| Manganese(II) (ম্যাঙ্গানিজ II) | Mn2+ | manganous (ম্যাঙ্গানাস) |
| Manganese(III) (ম্যাঙ্গানিজ III) | Mn3+ | manganic (ম্যাঙ্গানিক) |
| Manganese(IV) (ম্যাঙ্গানিজ IV) | Mn4+ | |
| Mercury(I) (মার্কারি I) | Hg2+ 2 |
mercurous (মারকিউরাস) |
| Mercury(II) (মার্কারি II) | Hg2+ | mercuric (মারকিউরিক) |
| Potassium (পটাসিয়া) | K+ | kalium (ক্যালিয়াম) |
| Silver (সিলভার) | Ag+ | argentous (আর্জেন্টাস) |
| Sodium (সোডিয়াম) | Na+ | natric (ন্যাট্রিক) |
| Strontium (স্ট্রনসিয়া) | Sr2+ | |
| Tin(II) (টিন II) | Sn2+ | stannous (স্ট্যানাস) |
| Tin(IV) (টিন IV) | Sn4+ | stannic (স্ট্যানিক) |
| Zinc (জিঙ্ক) | Zn2+ | |
| যৌগমূলক ক্যাটায়ন | ||
| Ammonium (অ্যামোনিয়াম) | NH+ 4 |
|
| Hydronium (হাইড্রোনিয়াম) | H3O+ | |
অ্যানায়ন
অধাতু সমূহ তাদের সর্বশেষ শক্তিস্তরে এক বা একাধিক ইলেকট্রন অপসারণ করে যে আয়নে পরিণত হয় তাকে অ্যানায়ন বলে। অ্যানায়নে প্রোটনের তুলানায় ইলেকট্রন বেশি থাকায় এর আধান (চার্জ) ঋণাত্মক (–)।
ব্যাখ্যা
অধাতু সমূহের সর্বশেষ শক্তিস্তরে ৫টি, ৬টি বা ৭টি ইলেকট্রন থাকে তাই এদের প্রতি নিউক্লিয়াসের প্রোটনের আকর্ষণ অনেক বেশি থাকে। অর্থাৎ, এদের আয়নিকরণ শক্তির মান অনেক বেশি হয়। ফলে, ওই ইলেকট্রন গুলো ত্যাগ করতে অনেক বেশি শক্তি প্রয়োজন হয়, যা সাধারণ অবস্থায় কোন রাসায়নিক বিক্রিয়া থেকে সহজে পাওয়া যায় না। ফলে অধাতু সমুহ ইলেকট্রন ত্যাগ করেনা। তাই তারা অন্য পরমাণু (সাধারণত ধাতব পরমাণু) থেকে ১টি, ২টি বা ৩টি ইলেকট্রন গ্রহণ করে।
সর্বশেষ শক্তিস্তরের ওই ইলেকট্রন গুলো গ্রহণ করলে অধাতব পরমাণু গুলো আর আধান নিরপেক্ষ থাকে না। এগুলো আয়নে পরিণত হয়। এই আয়নই হল অ্যানায়ন।[২]
কিছু অ্যানায়ন
| সাধারণ নাম | Formula | প্রচলিত নাম |
|---|---|---|
| মৌলের অ্যানায়ন | ||
| Azide (অ্যাজাইড) | N− 3 |
|
| Bromide (ব্রোমাইড) | Br− | |
| Chloride (ক্লোরাইড) | Cl− | |
| Fluoride (ফ্লোরাইড) | F− | |
| Hydride (হাইড্রেড) | H− | |
| Iodide (আয়োডাইড) | I− | |
| Nitride (নাইট্রাইড) | N3− | |
| Phosphide (ফসফাইড) | P3− | |
| Oxide (অক্সাইড) | O2− | |
| Sulfide (সালফাইড) | S2− | |
| selenide (সেলেনাইড) | Se2− | |
| অক্সো-অ্যানায়ন (যৌগ মূলকের অ্যানায়ন)[৩] | ||
| Carbonate (কার্বনেট) | CO2− 3 |
|
| Chlorate (ক্লোরেট) | ClO− 3 |
|
| Chromate (ক্রোমেট) | CrO2− 4 |
|
| Dichromate (ডাই ক্রোমেট) | Cr 2O2− 7 |
|
| Dihydrogen phosphate (ডাই হাইড্রোজেন ফসফেট) | H 2PO− 4 |
|
| Hydrogen carbonate (হাইড্রোজেন কার্বনেট) | HCO− 3 |
bicarbonate (বাইকার্বনেট) |
| Hydrogen sulfate (হাইড্রোজেন সালফেট) | HSO− 4 |
bisulfate (বাইসালফেট) |
| Hydrogen sulfite (হাইড্রোজেন সালফাইট) | HSO− 3 |
bisulfite (বাইসালফাইট) |
| Hydroxide (হাইড্রোক্সাইড) | OH− | |
| Hypochlorite (হাইপোক্লোরাইট) | ClO− | |
| Monohydrogen phosphate (মনোহাইড্রোজেন ফসফেট) | HPO2− 4 |
|
| Nitrate (নাইট্রেট) | NO− 3 |
|
| Nitrite (নাইট্রাইট) | NO− 2 |
|
| Perchlorate (পার ক্লোরেট) | ClO− 4 |
|
| Permanganate (পার ম্যাঙ্গানেট) | MnO− 4 |
|
| Peroxide (পার অক্সাইড) | O2− 2 |
|
| Phosphate (ফসফেট) | PO3− 4 |
|
| Sulfate (সালফেট) | SO2− 4 |
|
| Sulfite (সালফাইট) | SO2− 3 |
|
| Superoxide (সুপার অক্সাইড) | O− 2 |
|
| Thiosulfate (থিও সালফেট) | S 2O2− 3 |
|
| Silicate (সিলিকেট) | SiO4− 4 |
|
| Metasilicate (মেটাসিলিকেট) | SiO2− 3 |
|
| Aluminium silicate (অ্যালুমিনিয়াম সিলিকেট) | AlSiO− 4 |
|
| জৈব এসিডের অ্যানায়ন | ||
| Acetate (এসিটেড) | CH 3COO− |
ethanoate (ইথানয়েট) |
| Formate (ফরমেট) | HCOO− |
methanoate (মিথানয়েট) |
| Oxalate (অক্সালেট) | C 2O2− 4 |
|
| Cyanide (সায়ানাইড) | CN− | |
আরো দেখুন
তথ্যসূত্র
- ↑ "Ion" entry in Collins English Dictionary.
- ↑ ক খ রসায়ন ৯ম-১০ম। NCTB। ২০১৮। পৃষ্ঠা 92-94।
- ↑ ক খ গ "Common Ions and Their Charges" (পিডিএফ)। Science Geek।
