জুল-থমসন প্রভাব
এই নিবন্ধটি ইংরেজি থেকে আনাড়িভাবে অনুবাদ করা হয়েছে। এটি কোনও কম্পিউটার কর্তৃক অথবা দ্বিভাষিক দক্ষতাহীন কোনো অনুবাদক কর্তৃক অনূদিত হয়ে থাকতে পারে। |
তাপগতিবিদ্যায়, জুল–থমসন প্রভাব (জুল – কেলভিন প্রভাব বা কেলভিন – জুল প্রভাব হিসাবেও পরিচিত) যখন একটি বাস্তব গ্যাস বা তরল মাধ্যমে জোর করা হয় তখন একটি আসল গ্যাস বা তরল (একটি আদর্শ গ্যাস থেকে পৃথক হিসাবে) এর তাপমাত্রা পরিবর্তনের বর্ণনা দেয় ইনসুলেটেড রাখার সময় এটি প্লাগ করুন যাতে কোনও তাপই পরিবেশের সাথে বিনিময় হয় না। এই পদ্ধতিটিকে থ্রোটলিং প্রক্রিয়া বা জোল – থমসন প্রক্রিয়া বলা হয়। ঘরের তাপমাত্রায় হাইড্রোজেন, হিলিয়াম এবং নিয়ন ব্যতীত সমস্ত গ্যাস জুল – থমসন প্রক্রিয়া দ্বারা প্রসারিত হওয়ার পরে শীতল হয়ে যাওয়ার সময় শীতল হয়; এই তিনটি গ্যাস একই প্রভাব ফেলে তবে কেবলমাত্র কম তাপমাত্রায় হাইড্রোলিক অয়েলের মতো বেশিরভাগ তরলগুলি জোল – থমসন থ্রোটলিং প্রক্রিয়া দ্বারা উষ্ণ করা হবে।
গ্যাস-কুলিং থ্রোটলিং প্রক্রিয়া সাধারণত এয়ার কন্ডিশনার, হিট পাম্প এবং লিকুইফায়ারগুলির মতো ফ্রিজে প্রক্রিয়াগুলিতে ব্যবহার করা হয়। হাইড্রোলিক্সে, জুল–থমসন থ্রোটলিংয়ের উষ্ণতর প্রভাবটি অভ্যন্তরীণভাবে ভালভগুলি খুঁজে পাওয়ার জন্য ব্যবহার করা যেতে পারে কারণ এগুলি তাপ উৎপাদন করে যা থার্মোকল বা থার্মাল-ইমেজিং ক্যামেরা দ্বারা শনাক্ত করা যায়। থ্রোটলিং একটি মৌলিকভাবে অপরিবর্তনীয় প্রক্রিয়া। সরবরাহের লাইন, হিট এক্সচেঞ্জার্স, রিজেনারেটর এবং (তাপ) মেশিনের অন্যান্য উপাদানগুলিতে প্রবাহ প্রতিরোধের কারণে থ্রোটলিং হল ক্ষতির একটি উৎস যা কার্য সম্পাদনকে সীমাবদ্ধ করে।[১][২][৩] [৪] [৫][৬]
ইতিহাস[সম্পাদনা]
জেমস প্রেসকট জুল এবং উইলিয়াম থমসন, ১ম ব্যারন কেলভিনের নামানুসারে এই প্রভাবটির নামকরণ করা হয়েছিল, যিনি এটি ১৮৫২ সালে আবিষ্কার করেছিলেন। এটি জুল দ্বারা সম্প্রসারণ সম্পর্কে জুলের প্রথম কাজ অনুসরণ করেছিল, যেখানে একটি শূন্যে কোনও গ্যাস নিখরচায় বৃদ্ধি পায় এবং তাপমাত্রা অপরিবর্তিত থাকে, যদি আদর্শ গ্যাস হয়।
বিবরণ[সম্পাদনা]
গ্যাসের রুদ্ধতাপীয়(কোনও তাপের বিনিময় হয় না) বিস্তৃতি বিভিন্ন উপায়ে করা যেতে পারে। সম্প্রসারণের সময় গ্যাসের দ্বারা তাপমাত্রার পরিবর্তন কেবলমাত্র প্রাথমিক এবং চূড়ান্ত চাপের উপর নির্ভর করে না, পাশাপাশি যেভাবে সম্প্রসারণ করা হয় তার উপরও নির্ভর করে।
- যদি প্রসারণ প্রক্রিয়াটি বিপরীতমুখী হয়, যার অর্থ গ্যাসটি সর্বদা তাপবিদ্যায়িত ভারসাম্যহীন অবস্থায় থাকে তবে একে আইসেন্ট্রোপিক সম্প্রসারণ বলা হয়। এই দৃশ্যে, গ্যাস সম্প্রসারণের সময় ইতিবাচক কাজ করে এবং এর তাপমাত্রা হ্রাস পায়।
- অন্যদিকে, একটি মুক্ত সম্প্রসারণে, গ্যাস কোনও কাজ করে না এবং কোনও তাপ শোষণ করে না, তাই অভ্যন্তরীণ শক্তি সংরক্ষণ করা হয়। এই পদ্ধতিতে প্রসারিত, একটি আদর্শ গ্যাসের তাপমাত্রা স্থির থাকবে তবে খুব উচ্চ তাপমাত্রা ব্যতীত সত্যিকারের গ্যাসের তাপমাত্রা হ্রাস পেয়েছে|
- এই নিবন্ধে আলোচিত সম্প্রসারণের পদ্ধতিটি, যেখানে গতিবেগ শক্তিতে উল্লেখযোগ্য পরিবর্তন ছাড়াই চাপ P1 এ অবস্থিত একটি গ্যাস বা তরল নিম্নচাপের P2 অঞ্চলে প্রবাহিত হয়, তাকে জুল – থমসন সম্প্রসারণ বলা হয়। প্রসারণ সহজাতভাবে অপরিবর্তনীয়। এই সম্প্রসারণের সময়, এনথালপির অপরিবর্তিত রয়েছে (নীচে প্রমাণ দেখুন)। একটি নিখরচায় সম্প্রসারণের বিপরীতে, কাজটি করা হয়, যার ফলে অভ্যন্তরীণ শক্তির পরিবর্তন ঘটে। অভ্যন্তরীণ শক্তি বৃদ্ধি বা হ্রাস কিনা তা নির্ধারিত হয় ত্বকের উপর দিয়ে বা কাজটি করা হচ্ছে কিনা; এটি প্রসারণের প্রাথমিক এবং চূড়ান্ত অবস্থা এবং তরলের বৈশিষ্ট্য দ্বারা নির্ধারিত হয়।
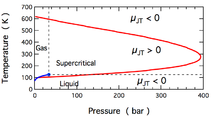
জুল–থমসন সম্প্রসারণের সময় উৎপাদিত তাপমাত্রা পরিবর্তনটি জোল-
থমসন সহগ এই সহগটি হয় ধনাত্মক (শীতল করার সাথে সম্পর্কিত) বা নেতিবাচক (গরম) হতে পারে; প্রতিটি আণবিক নাইট্রোজেন,N2এর জন্য যে অঞ্চলগুলি ঘটে সেগুলি চিত্রটিতে দেখানো হয়েছে। নোট করুন যে চিত্রটির বেশিরভাগ শর্ত N2 একটি সুপারক্রিটিকাল তরল হিসাবে সম্পর্কিত, যেখানে এটিতে গ্যাসের কিছু বৈশিষ্ট্য রয়েছে এবং কিছু তরল রয়েছে, তবে বাস্তবে এটি কোনওরূপে বর্ণিত হতে পারে না। সহগ খুব উচ্চ এবং খুব কম তাপমাত্রায় উভয় নেতিবাচক; খুব উচ্চ চাপে এটি সমস্ত তাপমাত্রায় নেতিবাচক।শূন্য চাপের কাছাকাছি আসার সাথে সাথে সর্বাধিক বিপরীত তাপমাত্রা (N2[১০] এর জন্য ৬২১ কেলভিন) ঘটে।N2 নিম্ন চাপে গ্যাসের জন্য,()উচ্চ তাপমাত্রায় নেতিবাচক এবং কম তাপমাত্রায় ইতিবাচক। গ্যাস-তরল সহাবস্থান বক্ররেখার নীচে তাপমাত্রায২, এন 2 ঘন তরল গঠন করে এবং সহগ আবার নেতিবাচক হয়।সুতরাং, ৬২১ কেলভিন নীচের গ্যাসের জন্য,N2 একটি জুল – থমসন প্রসারণ তরল N2 গঠন না হওয়া পর্যন্ত গ্যাসকে শীতল করতে ব্যবহার করা যেতে পারে।
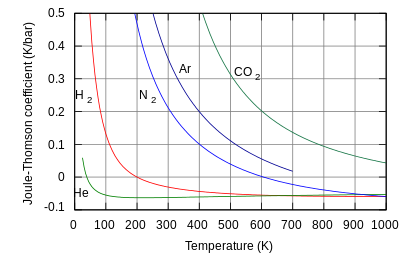
জুল – থমসন (কেলভিন) সহগ[সম্পাদনা]
তথ্যসূত্র[সম্পাদনা]
- ↑
R. H. Perry and D. W. Green (১৯৮৪)। Perry's Chemical Engineers' Handbook
 । McGraw-Hill। আইএসবিএন 978-0-07-049479-4।
। McGraw-Hill। আইএসবিএন 978-0-07-049479-4।
- ↑ B. N. Roy (২০০২)। Fundamentals of Classical and Statistical Thermodynamics। John Wiley & Sons। আইএসবিএন 978-0-470-84313-0। বিবকোড:2002fcst.book.....N।
- ↑ W. C. Edmister, B. I. Lee (১৯৮৪)। Applied Hydrocarbon Thermodynamics। Vol. 1 (2nd সংস্করণ)। Gulf Publishing। আইএসবিএন 978-0-87201-855-6।
- ↑ F. Reif (১৯৬৫)। "Chapter 5 – Simple applications of macroscopic thermodynamics"। Fundamentals of Statistical and Thermal Physics। McGraw-Hill। আইএসবিএন 978-0-07-051800-1।
- ↑ A. W. Adamson (১৯৭৩)। "Chapter 4 – Chemical thermodynamics. The First Law of Thermodynamics"। A Textbook of Physical Chemistry (1st সংস্করণ)। Academic Press। এলসিসিএন 72088328।
- ↑
G. W. Castellan (১৯৭১)। "Chapter 7 – Energy and the First Law of Thermodynamics; Thermochemistry"। Physical Chemistry
 (2nd সংস্করণ)। Addison-Wesley। আইএসবিএন 978-0-201-00912-5।
(2nd সংস্করণ)। Addison-Wesley। আইএসবিএন 978-0-201-00912-5।

