রুদ্ধতাপীয় প্রক্রিয়া
| তাপগতিবিজ্ঞান |
|---|
 |
| পুস্তক:তাপগতিবিদ্যা |

রুদ্ধতাপীয় প্রক্রিয়া হলো একটি তাপগতীয় প্রক্রিয়া যেখানে বাইরের পরিবেশের সাথে কোনো তাপগতীয় ব্যাবস্থার (সিস্টেমের) কোনো রকম তাপ বা ভরের আদান-প্রদান ঘটে না। এই প্রক্রিয়ায় শুধুমাত্র কাজের মাধ্যমে শক্তির আদান-প্রদান ঘটে ও সিস্টেমের তাপগতীয় পরিবর্তন সংঘটিত হয়।[১][২][৩]
বর্ণনা[সম্পাদনা]

যদি, কোনো গ্যাসকে কুপরিবাহী পাত্রে রেখে খুব দ্রুত চাপের পরিবর্তন ঘটানো যায় তাহলে তাপ সিস্টেম থেকে বেরও হতে পারবে না এবং ভেতরে প্রবেশও করতে পারবে না। (যদিও কোনো প্রক্রিয়াই সম্পূর্ণ ভাবে রুদ্ধতাপীয় নয় যেহেতু কিছু তাপ সবসময়ই আদান-প্রদান হয়। কিন্তু কিছু ক্ষেত্রে এই তাপের আদান-প্রদান এতই কম হয় যে সেইসব প্রক্রিয়াকে রুদ্ধতাপীয় প্রক্রিয়া হিসেবেই ধরা হয়)
তাপগতিবিদ্যার প্রথম সূত্র হতে আমরা জানি[৪],
যেখানে, অভ্যন্তরীণ শক্তির পরিবর্তন; হলো তাপের পরিবর্তন ও হলো কাজের পরিবর্তন।
যেহেতু, রুদ্ধতাপীয় প্রক্রিয়ায় কোনো তাপের আদান-প্রদান ঘটে না তাই, এক্ষেত্রে, হয়। ফলে সূত্রটি দাঁড়ায়,
বা,
এখন, যেহেতু : (; ; ; তাই, ) কাজেই,
যেখানে, হলো আয়তন, হলো বল, হলো ক্ষেত্রফল, হলো সরণ ও হলো চাপ।
সুতরাং, আয়তনের পরিবর্তন অর্থাৎ কাজ করলেই সিস্টেমের অভ্যন্তরীণ শক্তির পরিবর্তন হয় ও সিস্টেমের তাপগতীয় পরিবর্তন সংঘটিত হয়।
এই প্রক্রিয়ায় আয়তনের পরিবর্তন ঘটালে চাপেরও পরিবর্তন ঘটে। চাপ ও আয়তনের পরিবর্তন হলে (আদর্শ গ্যাসের জন্য চার্লস ও বয়েলের সূত্রানুযায়ী) সিস্টেমের তাপমাত্রারও পরিবর্তন ঘটে। আয়তন বাড়লে, অভ্যন্তরীণ শক্তি হ্রাস পায় ও আয়তন কমলে অভ্যন্তরীণ শক্তি বৃদ্ধি পায়।
আদর্শ গ্যাসের ক্ষেত্রে রুদ্ধতাপীয় প্রক্রিয়া (প্রত্যাবর্তি রুদ্ধতাপীয় প্রক্রিয়ার ক্ষেত্রে)[সম্পাদনা]
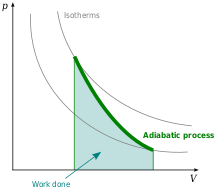
রুদ্ধতাপীয় প্রক্রিয়ায় (সূত্রের জন্য উপরের অংশ দেখুন),
আবার, স্থির আয়তনে এক মোল গ্যাসের আপেক্ষিক তাপ,
এখানে, হলো তাপমাত্রায় পার্থক্য ও হলো তাপমাত্রা।
কিন্তু, স্থির আয়তনে,
সুতরাং,
প্রথম সমীকরণ হতে,
আবার, আদর্শ গ্যাসের সূত্র অনুযায়ী, এক মোল গ্যাসের জন্য,
এখানে, হলো গ্যাস ধ্রুবক।
শেষোক্ত সমীকরণের অন্তরীকরণ (ডিফারেন্সিয়েশন) করে পাই,
বা,
এর মান (2) এ বসিয়ে পাই,
এখন এক মোল গ্যাসের জন্য, (মেয়ারের অন্বয়) হলে,
এখানে, হলো স্থির চাপে গ্যাসের আপেক্ষিক তাপ।
(3) এর সরল করে পাই,
- হলে,
(4) এর উভয় পক্ষকে দ্বারা ভাগ করে পাই,
(5) নং সমীকরণের সমাকলন করে পাই (সমাকলন করলে একটি ধ্রুবক উৎপন্ন হয়),
এখন,
- ধরলে,
(6) এর সরলীকরণ করে পাই,
আদর্শ গ্যাসের ক্ষেত্রে এটিই রুদ্ধতাপীয় প্রক্রিয়ায় চাপ ও আয়তনের মাঝে সম্পর্ক।
আরো দেখুন[সম্পাদনা]
সম্পর্কিত পদার্থবিদ্যা বিষয়[সম্পাদনা]
সম্পর্কিত তাপগতিবিদ্যা প্রক্রিয়া[সম্পাদনা]
তথ্যসূত্র[সম্পাদনা]
- ↑ "Adiabatic process"। Encyclopedia Britannica। Oct 04, 2010। এখানে তারিখের মান পরীক্ষা করুন:
|তারিখ=(সাহায্য) - ↑ Carathéodory, C. (১৯০৯)। "Untersuchungen über die Grundlagen der Thermodynamik"। Mathematische Annalen। 67 (3): 355–386। এসটুসিআইডি 118230148। ডিওআই:10.1007/BF01450409।. A translation may be found here ওয়েব্যাক মেশিনে আর্কাইভকৃত ২০১৯-১০-১২ তারিখে. Also a mostly reliable translation is to be found in Kestin, J. (১৯৭৬)। The Second Law of Thermodynamics। Stroudsburg, PA: Dowden, Hutchinson & Ross।
- ↑ Bailyn, M. (১৯৯৪)। A Survey of Thermodynamics। New York, NY: American Institute of Physics Press। পৃষ্ঠা 21। আইএসবিএন 0-88318-797-3।
- ↑ Franz, Mandl। Statistical Physics (2nd ed.)। John Wiley & sons। আইএসবিএন 978-0471915331।
বহিঃসংযোগ[সম্পাদনা]
![]() উইকিমিডিয়া কমন্সে রুদ্ধতাপীয় প্রক্রিয়া সম্পর্কিত মিডিয়া দেখুন।
উইকিমিডিয়া কমন্সে রুদ্ধতাপীয় প্রক্রিয়া সম্পর্কিত মিডিয়া দেখুন।













































