ইথানল: সংশোধিত সংস্করণের মধ্যে পার্থক্য
42.110.249.8 (আলাপ)-এর সম্পাদিত 4375685 নম্বর সংশোধনটি বাতিল করা হয়েছে (পূর্বাবস্থায় ফেরত) ট্যাগ: পূর্বাবস্থায় ফেরত মোবাইল সম্পাদনা মোবাইল ওয়েব সম্পাদনা উচ্চতর মোবাইল সম্পাদনা |
পরিভাষা ও বানান সংশোধন |
||
| ৭ নং লাইন: | ৭ নং লাইন: | ||
| ImageFileR2 = Ethanol-3D-balls.png |
| ImageFileR2 = Ethanol-3D-balls.png |
||
| IUPACName = ইথানল |
| IUPACName = ইথানল |
||
| OtherNames = ইথাইল অ্যালকোহল; গ্রেইন অ্যালকোহল; বিশুদ্ধ অ্যালকোহল; হাইড্রক্সিইথেন; পানীয় অ্যালকোহল; ইথাইল হাইড্রেট; অ্যাবসোলুট অ্যালকোহল; |
| OtherNames = ইথাইল অ্যালকোহল; গ্রেইন অ্যালকোহল; বিশুদ্ধ অ্যালকোহল; হাইড্রক্সিইথেন; পানীয় অ্যালকোহল; ইথাইল হাইড্রেট; অ্যাবসোলুট অ্যালকোহল; অনার্দ্র অ্যালকোহল |
||
| Section1 = {{Chembox Identifiers |
| Section1 = {{Chembox Identifiers |
||
| SMILES = CCO |
| SMILES = CCO |
||
| ৪৫ নং লাইন: | ৪৫ নং লাইন: | ||
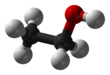
'''ইথানল''', যা '''ইথাইল অ্যালকোহল''' নামেও পরিচিত, এক প্রকারের [[অ্যালকোহল]]। এটি দাহ্য, স্বাদবিহীন, বর্ণহীন, সামান্য বিষাক্ত ও বিশিষ্ট গন্ধযুক্ত, এবং অধিকাংশ মদ এর প্রধান উপাদান। এতে ৯৯% বিশুদ্ধ অ্যালকোহল থাকে। এটি জৈব সংশ্লেষণে ব্যবহৃত হয়। এর রাসায়নিক সংকেত হল CH<sub>3</sub>-CH<sub>2</sub>-OH, বা [[কার্বন|C]]<sub>2</sub>[[হাইড্রোজেন|H]]<sub>6</sub>[[অক্সিজেন|O]], বা EtOH, C<sub>2</sub>H<sub>5</sub>OH বা C<sub>2</sub>H<sub>6</sub>O। |
'''ইথানল''', যা '''ইথাইল অ্যালকোহল''' নামেও পরিচিত, এক প্রকারের [[অ্যালকোহল]]। এটি দাহ্য, স্বাদবিহীন, বর্ণহীন, সামান্য বিষাক্ত ও বিশিষ্ট গন্ধযুক্ত, এবং অধিকাংশ মদ এর প্রধান উপাদান। এতে ৯৯% বিশুদ্ধ অ্যালকোহল থাকে। এটি জৈব সংশ্লেষণে ব্যবহৃত হয়। এর রাসায়নিক সংকেত হল CH<sub>3</sub>-CH<sub>2</sub>-OH, বা [[কার্বন|C]]<sub>2</sub>[[হাইড্রোজেন|H]]<sub>6</sub>[[অক্সিজেন|O]], বা EtOH, C<sub>2</sub>H<sub>5</sub>OH বা C<sub>2</sub>H<sub>6</sub>O। |
||
==রাসায়নিক সংকেত== |
==রাসায়নিক সংকেত== |
||
| ⚫ | ইথানল দুই কার্বন বিশিষ্ট অ্যালকোহল। এর রাসায়নিক সংকেত হচ্ছে: CH<sub>3</sub>CH<sub>2</sub>OH । CH<sub>3</sub>–CH<sub>2</sub>–OH দ্বারা বোঝায় একটি [[মিথাইল মূলক]] (CH<sub>3</sub>–) একটি [[মিথিলিন মূলক]] (–CH<sub>2</sub>–) এর সাথে যুক্ত হয়ে হাইড্রোক্সিল মূলকের অক্সিজেন অণুর সাথে একক বন্ধন দ্বারা যুক্ত। এটা ডাইমিথাইল ইথারের একটি সমানু। রসায়ন শাস্ত্রে অনেক সময় ইথানলকে সংক্ষেপে '''EtOH''' লেখা হয়। '''Et''' দ্বারা ইথাইল মূলককে বোঝানো হয়। |
||
ইথানল দুই কার্বন বিশিষ্ট এলকোহল। এর রাসায়নিক সংকেত হচ্ছে: |
|||
| ⚫ | CH<sub>3</sub>CH<sub>2</sub>OH । CH<sub>3</sub>–CH<sub>2</sub>–OH দ্বারা বোঝায় একটি [[মিথাইল মূলক]] (CH<sub>3</sub>–) একটি [[মিথিলিন মূলক]] (–CH<sub>2</sub>–) এর সাথে যুক্ত হয়ে হাইড্রোক্সিল মূলকের অক্সিজেন অণুর সাথে একক বন্ধন দ্বারা যুক্ত। এটা ডাইমিথাইল ইথারের একটি সমানু। রসায়ন শাস্ত্রে অনেক সময় ইথানলকে সংক্ষেপে '''EtOH''' লেখা হয়। '''Et''' দ্বারা ইথাইল |
||
==ইথানল নামকরণ== |
==ইথানল নামকরণ== |
||
রসায়নের নামকরণের আন্তর্জাতিক সংস্থা IUPAC এর নিয়ম অনুসারে ইথানলের নামকরণ করা হয়েছে। ইথানলের অণুতে দুটি কার্বন থাকায় পুর্বপদে ইথ এবং হাইড্রোক্সিল মূলকের উপস্থিতির কারণে পরপদে অল ব্যবহার করা হয়েছে | |
রসায়নের নামকরণের আন্তর্জাতিক সংস্থা IUPAC এর নিয়ম অনুসারে ইথানলের নামকরণ করা হয়েছে। ইথানলের অণুতে দুটি কার্বন থাকায় পুর্বপদে ইথ এবং হাইড্রোক্সিল মূলকের উপস্থিতির কারণে পরপদে অল ব্যবহার করা হয়েছে | |
||
| ⚫ | ১৮৩৪ সালে জার্মান রসায়নবিদ জাস্টাস ফন লিয়েবেগ প্রথম ইথাইল শব্দটি ব্যবহার করেন।<ref>Liebig, Justus (1834) [http://babel.hathitrust.org/cgi/pt?id=uva.x002457887;view=1up;seq=13 "Ueber die Constitution des Aethers und seiner Verbindungen"] (On the constitution of ether and its compounds), ''Annalen der Pharmacie'', '''9''' : 1–39. From page 18: "''Bezeichnen wir die Kohlenwasserstoffverbindung 4C + 10H als das Radikal des Aethers mit E<sub>2</sub> und nennen es Ethyl'', …" (Let us designate the hydrocarbon compound 4C + 10H as the radical of ether with E<sub>2</sub> and name it ethyl …).</ref> |
||
১৮৩৪ সালে জার্মান রসায়নবিদ |
|||
| ⚫ | জাস্টাস ফন লিয়েবেগ প্রথম ইথাইল শব্দটি ব্যবহার করেন।<ref>Liebig, Justus (1834) [http://babel.hathitrust.org/cgi/pt?id=uva.x002457887;view=1up;seq=13 "Ueber die Constitution des Aethers und seiner Verbindungen"] (On the constitution of ether and its compounds), ''Annalen der Pharmacie'', '''9''' : 1–39. From page 18: "''Bezeichnen wir die Kohlenwasserstoffverbindung 4C + 10H als das Radikal des Aethers mit E<sub>2</sub> und nennen es Ethyl'', …" (Let us designate the hydrocarbon compound 4C + 10H as the radical of ether with E<sub>2</sub> and name it ethyl …).</ref> |
||
ইথাইল শব্দটি ফরাসি শব্দ ইথার এবং গ্রিক শব্দ হাইল সমন্বয়ে গঠিত। ফরাসি ভাষায় ইথার বলতে সেই পদার্থকে বোঝায় যা |
ইথাইল শব্দটি ফরাসি শব্দ ইথার এবং গ্রিক শব্দ হাইল সমন্বয়ে গঠিত। ফরাসি ভাষায় ইথার বলতে সেই পদার্থকে বোঝায় যা সাধারণ তাপমাত্রায় বাষ্পীভূত হয় এবং গ্রিক ভাষায় হাইল শব্দের অর্থ বস্তু বা পদার্থ।<ref>{{OEtymD|ethyl}}</ref> |
||
১৮৯২ সালে |
১৮৯২ সালে সুইজারল্যান্ডের জেনেভায় অনুষ্ঠিত রাসায়নিক নামকরনের আন্তর্জাতিক সম্মেলনে ইথানল নামটি সর্বসম্মতিক্রমে গৃহীত হয়।<ref>For a report on the 1892 International Conference on Chemical Nomenclature, see: |
||
* {{সাময়িকী উদ্ধৃতি|লেখক=Armstrong, Henry |বছর=1892|ইউআরএল=http://books.google.com/books?id=LHkCAAAAIAAJ&pg=PA56 |শিরোনাম=The International Conference on Chemical Nomenclature|সাময়িকী=Nature|খণ্ড=46|পাতাসমূহ=56–59|ডিওআই=10.1038/046056c0|সংখ্যা নং=1177}} |
* {{সাময়িকী উদ্ধৃতি|লেখক=Armstrong, Henry |বছর=1892|ইউআরএল=http://books.google.com/books?id=LHkCAAAAIAAJ&pg=PA56 |শিরোনাম=The International Conference on Chemical Nomenclature|সাময়িকী=Nature|খণ্ড=46|পাতাসমূহ=56–59|ডিওআই=10.1038/046056c0|সংখ্যা নং=1177}} |
||
* Armstrong's report is reprinted with the resolutions in English in: {{সাময়িকী উদ্ধৃতি|লেখক= Armstrong, Henry |বছর=1892|ইউআরএল=http://books.google.com/books?id=RogMAQAAIAAJ&pg=PA398|শিরোনাম=The International Conference on Chemical Nomenclature|সাময়িকী=The Journal of Analytical and Applied Chemistry|খণ্ড=6|পাতাসমূহ= 390–400 (398)|উক্তি= The alcohols and the phenols will be called after the name of the hydrocarbon from which they are derived, terminated with the suffix ''ol'' (ex. pentanol, pentenol, etc.).}}</ref> |
* Armstrong's report is reprinted with the resolutions in English in: {{সাময়িকী উদ্ধৃতি|লেখক= Armstrong, Henry |বছর=1892|ইউআরএল=http://books.google.com/books?id=RogMAQAAIAAJ&pg=PA398|শিরোনাম=The International Conference on Chemical Nomenclature|সাময়িকী=The Journal of Analytical and Applied Chemistry|খণ্ড=6|পাতাসমূহ= 390–400 (398)|উক্তি= The alcohols and the phenols will be called after the name of the hydrocarbon from which they are derived, terminated with the suffix ''ol'' (ex. pentanol, pentenol, etc.).}}</ref> |
||
রসায়নের পরিভাষায় |
রসায়নের পরিভাষায় অ্যালকোহল বলতে একটি রাসায়নিক পদার্থের গ্রুপকে বোঝালেও প্রচলিত অর্থে সাধারণ মানুষ অ্যালকোহল বলতে ইথানলকে বোঝায়। আলকোরআনে সুরা বলতে এই ইথানলকে বোঝানো হয়েছে।<ref>[[OED]]; [[etymonline.com]] |
||
<!--[[WP:UNDUE]]: |
<!--[[WP:UNDUE]]: |
||
According to a note by "H.A. Hajar, MD" in an article by Qatar cardiologist Rachel Hajar, [http://site.hmc.org.qa/heartviews/vol1No9/PDF/IN_CONTEXT.pdf Alcohol: Friend or Foe? A Historical Perspective], Heart Views 1.9 (2000), 341-344, |
According to a note by "H.A. Hajar, MD" in an article by Qatar cardiologist Rachel Hajar, [http://site.hmc.org.qa/heartviews/vol1No9/PDF/IN_CONTEXT.pdf Alcohol: Friend or Foe? A Historical Perspective], Heart Views 1.9 (2000), 341-344, |
||
| ৮৭ নং লাইন: | ৮৫ নং লাইন: | ||
==বিক্রিয়া== |
==বিক্রিয়া== |
||
অ্যালকোহলকে তিনভাগে ভাগ করা হয় । ইথানল [[প্রাইমারী এলকোহল|প্রাইমারী অ্যালকোহল]]। প্রাইমারী অ্যালকোহল তাদের বলা হয় যাদের [[হাইড্রোক্সিল মূলক]] যুক্ত কার্বনের সাথে কমপক্ষে দুইটি [[হাইড্রোজেন]] যুক্ত থাকে। অধিকাংশ ইথানলের হাইড্রোক্সিল মূলক অংশে প্রধান [[বিক্রিয়া]] ঘটে। |
|||
অধিকাংশ ইথানলের হাইড্রোক্সিল মূলক অংশে প্রধান [[বিক্রিয়া]] ঘটে। |
|||
===এস্টার ফরমেশান=== |
===এস্টার ফরমেশান=== |
||
অম্ল প্রভাবকের উপস্থিতিতে ইথানল কার্বক্সিলিক এসিডের সাথে বিক্রিয়া করে [[ইথাইল এস্টার]] এবং [[পানি]] তৈরী করে: |
|||
:[[কার্বক্সিলিক এসিড|RCOOH]] + HOCH<sub>2</sub>CH<sub>3</sub> {{Unicode|→}} [[এস্টার|RCOOCH<sub>2</sub>CH<sub>3</sub>]] + H<sub>2</sub>O |
:[[কার্বক্সিলিক এসিড|RCOOH]] + HOCH<sub>2</sub>CH<sub>3</sub> {{Unicode|→}} [[এস্টার|RCOOCH<sub>2</sub>CH<sub>3</sub>]] + H<sub>2</sub>O |
||
শিল্প কারখানায় প্রস্তুত এস্টার থেকে পানি অপসারণ করা হয়। [[এস্টার]] |
শিল্প কারখানায় প্রস্তুত এস্টার থেকে পানি অপসারণ করা হয়। [[এস্টার]] অম্ল অথবা ক্ষারের উপস্থিতিতে বিক্রিয়া করে পূণরায় অ্যালকোহল ও লবণ উৎপন্ন করে।এই বিক্রিয়াটি স্যাপোনিফিকেশান বা সাবানিকরণ বিক্রিয়া নামে পরিচিত। কারণ এই বিক্রিয়ার মাধ্যমে সাবান প্রস্তুত করা হয়। <ref>এস্টার ও ফ্যাটি এসিড সমূহের রসায়ন। উচ্চ মাধ্যমিক রসায়ন। দ্বিতীয় পত্র। সরোজ কান্তি সিংহ ও নাগ।</ref> অজৈব এসিডের সাথে ইথানল বিক্রিয়া করে এস্টার গঠন করে। সালফার ট্রাই অক্সাইড এবং [[ফসফরাস]] পেন্টাঅক্সাইডের সাথে ইথানলের বিক্রিয়ায় পর্যায়ক্রমে [[ডাই ইথাইল সালফেট]] এবং [[ট্রাই ইথাইল ফসফেট]] তৈরি হয়। অজৈব সংশ্লেষনে [[ডাই ইথাইল সালফেট]] উপকারী ইথাইলেটিং এজেন্ট হিসেবে কাজ করে। [[সোডিয়াম নাইট্রাইট]] এবং সালফিউরিক এসিডের সাথে ইথানলের বিক্রিয়ায় [[ইথাইল নাইট্রাইট]] উৎপন্ন হয় যা ডাই ইউরেটিক হিসেবে ব্যবহৃত হয়। |
||
===পানি বিয়োজন=== |
===পানি বিয়োজন=== |
||
শক্তিশালী |
শক্তিশালী অম্লের উপস্থিতিতে ইথানলের ডিহাইড্রেশান বা [[পানি]] বিয়োজন ঘটে। পানি বিয়োজিত হয়ে ইথানল [[ডাই ইথাইল ইথার]] এবং অন্যান্য [[উপজাত]] তৈরী করে। প্রতিবছর [[সালফিউরিক এসিড]] [[প্রভাবক]] হিসেবে ব্যবহার করে লক্ষ লক্ষ কেজি ডাই ইথাইল ইথার প্রস্তুত করা হয়: |
||
:2 CH<sub>3</sub>CH<sub>2</sub>OH {{Unicode|→}} CH<sub>3</sub>CH<sub>2</sub>OCH<sub>2</sub>CH<sub>3</sub> + H<sub>2</sub>O (120 °C তাপমাত্রায়) |
:2 CH<sub>3</sub>CH<sub>2</sub>OH {{Unicode|→}} CH<sub>3</sub>CH<sub>2</sub>OCH<sub>2</sub>CH<sub>3</sub> + H<sub>2</sub>O (120 °C তাপমাত্রায়) |
||
===দহন=== |
===দহন=== |
||
| ১০৬ নং লাইন: | ১০৩ নং লাইন: | ||
===মেথিলেটেড স্পিরিট=== |
===মেথিলেটেড স্পিরিট=== |
||
[[মদ]], [[বিয়ার]], [[হুইস্কি]], [[ব্রান্ডি]] প্রভৃতি পানীয় ইথাইল এলকোহল হতে প্রস্তুত করা হয়। এ পানীয়সমহূল প্রকৃতপক্ষে ইথাইল |
[[মদ]], [[বিয়ার]], [[হুইস্কি]], [[ব্রান্ডি]] প্রভৃতি পানীয় ইথাইল এলকোহল হতে প্রস্তুত করা হয়। এ পানীয়সমহূল প্রকৃতপক্ষে ইথাইল অ্যালকোহলের বিভিন্ন ঘনমাত্রার [[জলীয় দ্রবণ]] বিশেষ। এসকল পানীয়ের উপর প্রচুর [[আবগারী শুল্ক]] দিতে হয়। তাই এগুলো অত্যন্ত মহার্ঘ। অনেক সময় মাদকাসক্ত ব্যক্তিরা বাজার হতে সস্তা দামের ইথাইল অ্যালকোহল কিনে এর সঙ্গে প্রয়োজন মত পানি মিশ্রিত করে দামী বাণিজ্যিক মদের বিকল্প হিসেবে পান করে। পানের কাজে এরূপ যথেচ্ছ ব্যবহারের ফলে ইথাইল অ্যালকোহলের ঘাটতি পড়তে পারে। কারণ দ্রাবক এবং শিল্পজাত দ্রব্য উৎপাদনকাজে [[ইথাইল]] অ্যালকোহল ব্যাপকভাবে ব্যবহৃত হয়। তাই পানীয় হিসেবে ইথাইলে অ্যালকোহলের অনঅনুমোদিত ব্যবহার বন্ধে এর সাথে মিথানল, পিরিডিন, ন্যাপথা প্রভৃতি বিষাক্ত পদার্থ মিশিয়ে বাজারজাত করা হয়। বাণিজ্যিকভাবে এরূপ অ্যালকোহলকে মেথিলেটেড স্পিরিট, ডি ন্যাচারড অ্যালকোহল বা অসেবনীয় অ্যালকোহল নামে পরিচিত। এটি বিশেষভাবে রং-বার্ণিশের কাজে দ্রাবক হিসেবে ব্যবহার করা হয়।<ref>উচ্চ মাধ্যমিক রসায়ন, দ্বিতীয় পত্র। অধ্যায়ঃ২৪, এলকোহল, ফেনল ও ইথারসমহুহ। ৩০৭ পৃষ্ঠা। লেখকঃ ড. রবিউল ইসলাম, ড. গাজী মোঃ আহসানুল কবীর, ডঃ মনিমুল হক। ৬ষ্ঠ সংস্করণ, জুন ২০০৪ । প্রথম প্রকাশ মার্চ ১৯৯৯।</ref> মেথিলেটেড স্পিরিটকে ইথানলের প্রকারভেদ হিসেবে গণ্য করা হয়। |
||
==বিবিধ== |
==বিবিধ== |
||
===বৈশিষ্ট্য=== |
===বৈশিষ্ট্য=== |
||
মানুষের দেহ থেকে |
মানুষের দেহ থেকে অ্যালকোহল ডিহাইড্রোজিনেজ পদ্ধতিতে জারণের মাধ্যমে সীমিত ইথানল অপসারণ করা যায়। জিরো অর্ডার কাইনেটিকস বা শুন্যক্রমের মাধ্যমে রক্ত থেকে বড় আকারের অ্যালকোহল সরিয়ে নেয়া সম্ভব।এর মানে একটি নির্দিষ্ট হারে শরীর থেকে অ্যালকোহল বেরিয়ে যায়।<ref>{{সাময়িকী উদ্ধৃতি|শিরোনাম=The Clinical Pharmacology of Alcohol |প্রকাশক=Ncbi.nlm.nih.gov |তারিখ=2013-08-12|pmc=1501558|শেষাংশ১=Becker|প্রথমাংশ১=CE|খণ্ড=113|সংখ্যা নং=3|পাতাসমূহ=37–45|সাময়িকী=California Medicine|pmid=5457514}}</ref> বিশুদ্ধ বিশুদ্ধ ইথানল চামড়া ও চোখে জ্বালাপড়া সৃষ্টি করে।<ref>[http://www.nfpa.org/Assets/files/AboutTheCodes/704/CLA-AAA_ROPminutes_01-10.pdf Minutes of Meeting]. Technical Committee on Classification and Properties of Hazardous Chemical Data (January 12–13, 2010).</ref> ইথানল সেবনে মাথা ঘোরা, বমি এবং বিষক্রিয়ার সৃষ্টি হয়। দীর্ঘকাল ধরে ইথানল সেবনে লিভারের মারাত্মক ক্ষতি হতে পারে। <ref name="msdset">{{ওয়েব উদ্ধৃতি |ইউআরএল=http://msds.chem.ox.ac.uk/ET/ethyl_alcohol.html |শিরোনাম=Safety data for ethyl alcohol |প্রকাশক=Msds.chem.ox.ac.uk |তারিখ=2008-05-09 |সংগ্রহের-তারিখ=2011-01-03 |আর্কাইভের-ইউআরএল=https://web.archive.org/web/20110714040451/http://msds.chem.ox.ac.uk/ET/ethyl_alcohol.html |আর্কাইভের-তারিখ=২০১১-০৭-১৪ |অকার্যকর-ইউআরএল=হ্যাঁ }}</ref> |
||
বিশুদ্ধ বিশুদ্ধ ইথানল চামড়া ও চোখে জ্বালাপড়া সৃষ্টি করে।<ref>[http://www.nfpa.org/Assets/files/AboutTheCodes/704/CLA-AAA_ROPminutes_01-10.pdf Minutes of Meeting]. Technical Committee on Classification and Properties of Hazardous Chemical Data (January 12–13, 2010).</ref> ইথানল সেবনে মাথা ঘোরা, বমি এবং বিষক্রিয়ার সৃষ্টি হয়। দীর্ঘকাল ধরে ইথানল সেবনে মারাত্বক লিভার ড্যামেজ হতে পারে। <ref name="msdset">{{ওয়েব উদ্ধৃতি |ইউআরএল=http://msds.chem.ox.ac.uk/ET/ethyl_alcohol.html |শিরোনাম=Safety data for ethyl alcohol |প্রকাশক=Msds.chem.ox.ac.uk |তারিখ=2008-05-09 |সংগ্রহের-তারিখ=2011-01-03 |আর্কাইভের-ইউআরএল=https://web.archive.org/web/20110714040451/http://msds.chem.ox.ac.uk/ET/ethyl_alcohol.html |আর্কাইভের-তারিখ=২০১১-০৭-১৪ |অকার্যকর-ইউআরএল=হ্যাঁ }}</ref> |
|||
==তথ্য সূত্র== |
==তথ্য সূত্র== |
||
১৪:৩১, ১৬ নভেম্বর ২০২০ তারিখে সংশোধিত সংস্করণ
| |||
| |||
| নামসমূহ | |||
|---|---|---|---|
| ইউপ্যাক নাম
ইথানল
| |||
| অন্যান্য নাম
ইথাইল অ্যালকোহল; গ্রেইন অ্যালকোহল; বিশুদ্ধ অ্যালকোহল; হাইড্রক্সিইথেন; পানীয় অ্যালকোহল; ইথাইল হাইড্রেট; অ্যাবসোলুট অ্যালকোহল; অনার্দ্র অ্যালকোহল
| |||
| শনাক্তকারী | |||
ত্রিমাত্রিক মডেল (জেমল)
|
|||
| কেমস্পাইডার | |||
| ইসিএইচএ ইনফোকার্ড | ১০০.০০০.৫২৬ | ||
| ইসি-নম্বর | |||
পাবকেম CID
|
|||
| আরটিইসিএস নম্বর |
| ||
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|||
| |||
| |||
| বৈশিষ্ট্য | |||
| C2H6O | |||
| আণবিক ভর | ৪৬.০৭ g·mol−১ | ||
| বর্ণ | colorless liquid | ||
| ঘনত্ব | 0.789 g/cm3 | ||
| গলনাঙ্ক | −১১৪.৩ °সে (−১৭৩.৭ °ফা; ১৫৮.৮ K) | ||
| স্ফুটনাঙ্ক | ৭৮.৪ °সে (১৭৩.১ °ফা; ৩৫১.৫ K) | ||
| miscible | |||
| অম্লতা (pKa) | 15.9 | ||
| প্রতিসরাঙ্ক (nD) | 1.36 (25 °C) | ||
| সান্দ্রতা | 1.200 cP (1.200 mPa·s) (20 °C) | ||
| ডায়াপল মুহূর্ত | 1.69 D (gas) | ||
| ঝুঁকি প্রবণতা | |||
ইইউ শ্রেণীবিভাগ (ডিএসডি)
|
Flammable (F) | ||
| আর-বাক্যাংশ | আর১১ | ||
| এস-বাক্যাংশ | (এস২) এস৭ এস১৬ | ||
| এনএফপিএ ৭০৪ | |||
| ফ্ল্যাশ পয়েন্ট | 13 °C (55.4 °F) | ||
| সম্পর্কিত যৌগ | |||
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |||
| তথ্যছক তথ্যসূত্র | |||
ইথানল, যা ইথাইল অ্যালকোহল নামেও পরিচিত, এক প্রকারের অ্যালকোহল। এটি দাহ্য, স্বাদবিহীন, বর্ণহীন, সামান্য বিষাক্ত ও বিশিষ্ট গন্ধযুক্ত, এবং অধিকাংশ মদ এর প্রধান উপাদান। এতে ৯৯% বিশুদ্ধ অ্যালকোহল থাকে। এটি জৈব সংশ্লেষণে ব্যবহৃত হয়। এর রাসায়নিক সংকেত হল CH3-CH2-OH, বা C2H6O, বা EtOH, C2H5OH বা C2H6O।
রাসায়নিক সংকেত
ইথানল দুই কার্বন বিশিষ্ট অ্যালকোহল। এর রাসায়নিক সংকেত হচ্ছে: CH3CH2OH । CH3–CH2–OH দ্বারা বোঝায় একটি মিথাইল মূলক (CH3–) একটি মিথিলিন মূলক (–CH2–) এর সাথে যুক্ত হয়ে হাইড্রোক্সিল মূলকের অক্সিজেন অণুর সাথে একক বন্ধন দ্বারা যুক্ত। এটা ডাইমিথাইল ইথারের একটি সমানু। রসায়ন শাস্ত্রে অনেক সময় ইথানলকে সংক্ষেপে EtOH লেখা হয়। Et দ্বারা ইথাইল মূলককে বোঝানো হয়।
ইথানল নামকরণ
রসায়নের নামকরণের আন্তর্জাতিক সংস্থা IUPAC এর নিয়ম অনুসারে ইথানলের নামকরণ করা হয়েছে। ইথানলের অণুতে দুটি কার্বন থাকায় পুর্বপদে ইথ এবং হাইড্রোক্সিল মূলকের উপস্থিতির কারণে পরপদে অল ব্যবহার করা হয়েছে |
১৮৩৪ সালে জার্মান রসায়নবিদ জাস্টাস ফন লিয়েবেগ প্রথম ইথাইল শব্দটি ব্যবহার করেন।[১]
ইথাইল শব্দটি ফরাসি শব্দ ইথার এবং গ্রিক শব্দ হাইল সমন্বয়ে গঠিত। ফরাসি ভাষায় ইথার বলতে সেই পদার্থকে বোঝায় যা সাধারণ তাপমাত্রায় বাষ্পীভূত হয় এবং গ্রিক ভাষায় হাইল শব্দের অর্থ বস্তু বা পদার্থ।[২]
১৮৯২ সালে সুইজারল্যান্ডের জেনেভায় অনুষ্ঠিত রাসায়নিক নামকরনের আন্তর্জাতিক সম্মেলনে ইথানল নামটি সর্বসম্মতিক্রমে গৃহীত হয়।[৩]
রসায়নের পরিভাষায় অ্যালকোহল বলতে একটি রাসায়নিক পদার্থের গ্রুপকে বোঝালেও প্রচলিত অর্থে সাধারণ মানুষ অ্যালকোহল বলতে ইথানলকে বোঝায়। আলকোরআনে সুরা বলতে এই ইথানলকে বোঝানো হয়েছে।[৪]
প্রাকৃতিক উৎস
ঈস্টের মেটাবলিক প্রোসেসে উপজাত হিসেবে ইথানল পাওয়া যায়। তাই যেখানে ঈস্ট পাওয়া যাবে সেখানে ইথানল অবশ্যই পাওয়া যাবে। সাধারনত অতিরিক্ত পাকা ফলে ইথানল পাওয়া যায়।[৫] বারটাম পাম ফুলে সিমবায়োটিক ঈস্ট ইথানল উৎপাদন করে। কিছু কিছু পতঙ্গ যেমন পেনটেইলড ট্রিশ্রিউ ইথানলের উৎস খোঁজার প্রবণতা প্রদর্শন করে। তবে অধিকাংশ পতঙ্গ খাবারের উৎস হিসেবে ইথানল যুক্ত উৎস এড়িয়ে চলে।[৬] প্রাকৃতিক এনারোবায়োসিসের ফলাফল হিসেবে অনেক উদ্ভিদ ইথানল উৎপন্ন করে।[৭] মহাশূন্যেও ইথানলের অস্তিত্ব পাওয়া গেছে।[৮]
মানবদেহে ইথানল
এক গবেষণায় দেখা গেছে প্রতিজন সুস্থ মানুষের প্রশ্বাসে ২৪৪ ppb ইথানল এবং এসিটালডিহাইড উপস্থিত থাকে।[৯] একই রকম আরেকটি গবেষণায় সুস্থ সবল একজন স্বেচ্ছাসেবকের প্রশ্বাসে ৪৫০ ppb ইথানল পাওয়া গেছে।[১০] এই গবেষণায় মদ বা মদজাতীয় পানীয় পান করার পরের হিসাব ধরা হয়নি।
ফার্মাকোলজি
ইথানলের নিচের ফার্মাকোলজিক্যাল কাজ করার ক্ষমতা রয়েছে।:[১১]
- GABAA receptor [GABAA receptor) (primarily δ subunit-containing receptors) positive allosteric modulator
- NMDA receptor negative allosteric modulator
- Glycine receptor positive and negative allosteric modulator
- 5-HT3 receptor (5-HT3 receptor) positive allosteric modulator
- Nicotinic acetylcholine receptor (nACh receptor) positive and negative allosteric modulator
- Dihydropyridine-sensitive L-type calcium channel|L-type Ca2+ channel blocker
- GIRK channel opener [১১]
প্রস্তুত প্রণালী
ইতিহাস
বিক্রিয়া
অ্যালকোহলকে তিনভাগে ভাগ করা হয় । ইথানল প্রাইমারী অ্যালকোহল। প্রাইমারী অ্যালকোহল তাদের বলা হয় যাদের হাইড্রোক্সিল মূলক যুক্ত কার্বনের সাথে কমপক্ষে দুইটি হাইড্রোজেন যুক্ত থাকে। অধিকাংশ ইথানলের হাইড্রোক্সিল মূলক অংশে প্রধান বিক্রিয়া ঘটে।
এস্টার ফরমেশান
অম্ল প্রভাবকের উপস্থিতিতে ইথানল কার্বক্সিলিক এসিডের সাথে বিক্রিয়া করে ইথাইল এস্টার এবং পানি তৈরী করে:
- RCOOH + HOCH2CH3 → RCOOCH2CH3 + H2O
শিল্প কারখানায় প্রস্তুত এস্টার থেকে পানি অপসারণ করা হয়। এস্টার অম্ল অথবা ক্ষারের উপস্থিতিতে বিক্রিয়া করে পূণরায় অ্যালকোহল ও লবণ উৎপন্ন করে।এই বিক্রিয়াটি স্যাপোনিফিকেশান বা সাবানিকরণ বিক্রিয়া নামে পরিচিত। কারণ এই বিক্রিয়ার মাধ্যমে সাবান প্রস্তুত করা হয়। [১২] অজৈব এসিডের সাথে ইথানল বিক্রিয়া করে এস্টার গঠন করে। সালফার ট্রাই অক্সাইড এবং ফসফরাস পেন্টাঅক্সাইডের সাথে ইথানলের বিক্রিয়ায় পর্যায়ক্রমে ডাই ইথাইল সালফেট এবং ট্রাই ইথাইল ফসফেট তৈরি হয়। অজৈব সংশ্লেষনে ডাই ইথাইল সালফেট উপকারী ইথাইলেটিং এজেন্ট হিসেবে কাজ করে। সোডিয়াম নাইট্রাইট এবং সালফিউরিক এসিডের সাথে ইথানলের বিক্রিয়ায় ইথাইল নাইট্রাইট উৎপন্ন হয় যা ডাই ইউরেটিক হিসেবে ব্যবহৃত হয়।
পানি বিয়োজন
শক্তিশালী অম্লের উপস্থিতিতে ইথানলের ডিহাইড্রেশান বা পানি বিয়োজন ঘটে। পানি বিয়োজিত হয়ে ইথানল ডাই ইথাইল ইথার এবং অন্যান্য উপজাত তৈরী করে। প্রতিবছর সালফিউরিক এসিড প্রভাবক হিসেবে ব্যবহার করে লক্ষ লক্ষ কেজি ডাই ইথাইল ইথার প্রস্তুত করা হয়:
- 2 CH3CH2OH → CH3CH2OCH2CH3 + H2O (120 °C তাপমাত্রায়)
দহন
ইথানলের পূর্ণ দহনে কার্বন ডাই অক্সাইড এবং পানি উৎপন্ন হয়:
- C2H5OH (l) + 3 O2 (g) → 2 CO2 (g) + 3 H2O (liq); −ΔHc = 1371 kJ/mol[১৩]
বিভিন্ন রকমের ইথানল
রেক্টিফায়েড স্পিরিট
রেক্টিফায়েড স্পিরিট মূলত পাতন প্রকৃয়ায় পৃথকিকৃত ইথানল যা ৯৫.৪% ইথানল ও ৪.৬% পানির মিশ্রণ (দেশ ভেদে ভিন্নতা রেয়েছে)।
মেথিলেটেড স্পিরিট
মদ, বিয়ার, হুইস্কি, ব্রান্ডি প্রভৃতি পানীয় ইথাইল এলকোহল হতে প্রস্তুত করা হয়। এ পানীয়সমহূল প্রকৃতপক্ষে ইথাইল অ্যালকোহলের বিভিন্ন ঘনমাত্রার জলীয় দ্রবণ বিশেষ। এসকল পানীয়ের উপর প্রচুর আবগারী শুল্ক দিতে হয়। তাই এগুলো অত্যন্ত মহার্ঘ। অনেক সময় মাদকাসক্ত ব্যক্তিরা বাজার হতে সস্তা দামের ইথাইল অ্যালকোহল কিনে এর সঙ্গে প্রয়োজন মত পানি মিশ্রিত করে দামী বাণিজ্যিক মদের বিকল্প হিসেবে পান করে। পানের কাজে এরূপ যথেচ্ছ ব্যবহারের ফলে ইথাইল অ্যালকোহলের ঘাটতি পড়তে পারে। কারণ দ্রাবক এবং শিল্পজাত দ্রব্য উৎপাদনকাজে ইথাইল অ্যালকোহল ব্যাপকভাবে ব্যবহৃত হয়। তাই পানীয় হিসেবে ইথাইলে অ্যালকোহলের অনঅনুমোদিত ব্যবহার বন্ধে এর সাথে মিথানল, পিরিডিন, ন্যাপথা প্রভৃতি বিষাক্ত পদার্থ মিশিয়ে বাজারজাত করা হয়। বাণিজ্যিকভাবে এরূপ অ্যালকোহলকে মেথিলেটেড স্পিরিট, ডি ন্যাচারড অ্যালকোহল বা অসেবনীয় অ্যালকোহল নামে পরিচিত। এটি বিশেষভাবে রং-বার্ণিশের কাজে দ্রাবক হিসেবে ব্যবহার করা হয়।[১৪] মেথিলেটেড স্পিরিটকে ইথানলের প্রকারভেদ হিসেবে গণ্য করা হয়।
বিবিধ
বৈশিষ্ট্য
মানুষের দেহ থেকে অ্যালকোহল ডিহাইড্রোজিনেজ পদ্ধতিতে জারণের মাধ্যমে সীমিত ইথানল অপসারণ করা যায়। জিরো অর্ডার কাইনেটিকস বা শুন্যক্রমের মাধ্যমে রক্ত থেকে বড় আকারের অ্যালকোহল সরিয়ে নেয়া সম্ভব।এর মানে একটি নির্দিষ্ট হারে শরীর থেকে অ্যালকোহল বেরিয়ে যায়।[১৫] বিশুদ্ধ বিশুদ্ধ ইথানল চামড়া ও চোখে জ্বালাপড়া সৃষ্টি করে।[১৬] ইথানল সেবনে মাথা ঘোরা, বমি এবং বিষক্রিয়ার সৃষ্টি হয়। দীর্ঘকাল ধরে ইথানল সেবনে লিভারের মারাত্মক ক্ষতি হতে পারে। [১৭]
তথ্য সূত্র
- ↑ Liebig, Justus (1834) "Ueber die Constitution des Aethers und seiner Verbindungen" (On the constitution of ether and its compounds), Annalen der Pharmacie, 9 : 1–39. From page 18: "Bezeichnen wir die Kohlenwasserstoffverbindung 4C + 10H als das Radikal des Aethers mit E2 und nennen es Ethyl, …" (Let us designate the hydrocarbon compound 4C + 10H as the radical of ether with E2 and name it ethyl …).
- ↑ Harper, Douglas। "ethyl"। Online Etymology Dictionary।
- ↑ For a report on the 1892 International Conference on Chemical Nomenclature, see:
- Armstrong, Henry (১৮৯২)। "The International Conference on Chemical Nomenclature"। Nature। 46 (1177): 56–59। ডিওআই:10.1038/046056c0।
- Armstrong's report is reprinted with the resolutions in English in: Armstrong, Henry (১৮৯২)। "The International Conference on Chemical Nomenclature"। The Journal of Analytical and Applied Chemistry। 6: 390–400 (398)।
The alcohols and the phenols will be called after the name of the hydrocarbon from which they are derived, terminated with the suffix ol (ex. pentanol, pentenol, etc.).
- ↑ OED; etymonline.com
- ↑ Dudley, Robert (২০০৪)। "Ethanol, Fruit Ripening, and the Historical Origins of Human Alcoholism in Primate Frugivory"। Integrative Comparative Biology। 44 (4): 315–323। ডিওআই:10.1093/icb/44.4.315। পিএমআইডি 21676715।
- ↑ Graber, Cynthia (২০০৮)। "Fact or Fiction?: Animals Like to Get Drunk"। Scientific American। সংগ্রহের তারিখ ২০১০-০৭-২৩।
- ↑ Leblová, Sylva; Sinecká, Eva and Vaníčková, Věra (১৯৭৪)। "Pyruvate metabolism in germinating seeds during natural anaerobiosis"। Biologia Plantarum। 16 (6): 406–411। ডিওআই:10.1007/BF02922229।
- ↑ Schriver, A.; Schriver-Mazzuoli, L.; Ehrenfreund, P. and d’Hendecourt, L. (২০০৭)। "One possible origin of ethanol in interstellar medium: Photochemistry of mixed CO2–C2H6 films at 11 K. A FTIR study"। Chemical Physics। 334 (1–3): 128–137। ডিওআই:10.1016/j.chemphys.2007.02.018। বিবকোড:2007CP....334..128S।
- ↑ http://www.ncbi.nlm.nih.gov/pubmed/16312013
- ↑ http://www.ncbi.nlm.nih.gov/pubmed/16705261
- ↑ ক খ Spanagel R (২০০৯)। "Alcoholism: a systems approach from molecular physiology to addictive behavior"। Physiol. Rev.। 89 (2): 649–705। ডিওআই:10.1152/physrev.00013.2008। পিএমআইডি 19342616। অজানা প্যারামিটার
|month=উপেক্ষা করা হয়েছে (সাহায্য) - ↑ এস্টার ও ফ্যাটি এসিড সমূহের রসায়ন। উচ্চ মাধ্যমিক রসায়ন। দ্বিতীয় পত্র। সরোজ কান্তি সিংহ ও নাগ।
- ↑ Rossini, Frederick D. (১৯৩৭)। "Heats of Formation of Simple Organic Molecules"। Ind. Eng. Chem.। অজানা প্যারামিটার
|1=উপেক্ষা করা হয়েছে (সাহায্য) - ↑ উচ্চ মাধ্যমিক রসায়ন, দ্বিতীয় পত্র। অধ্যায়ঃ২৪, এলকোহল, ফেনল ও ইথারসমহুহ। ৩০৭ পৃষ্ঠা। লেখকঃ ড. রবিউল ইসলাম, ড. গাজী মোঃ আহসানুল কবীর, ডঃ মনিমুল হক। ৬ষ্ঠ সংস্করণ, জুন ২০০৪ । প্রথম প্রকাশ মার্চ ১৯৯৯।
- ↑ Becker, CE (২০১৩-০৮-১২)। "The Clinical Pharmacology of Alcohol"। California Medicine। Ncbi.nlm.nih.gov। 113 (3): 37–45। পিএমআইডি 5457514। পিএমসি 1501558
 ।
।
- ↑ Minutes of Meeting. Technical Committee on Classification and Properties of Hazardous Chemical Data (January 12–13, 2010).
- ↑ "Safety data for ethyl alcohol"। Msds.chem.ox.ac.uk। ২০০৮-০৫-০৯। ২০১১-০৭-১৪ তারিখে মূল থেকে আর্কাইভ করা। সংগ্রহের তারিখ ২০১১-০১-০৩।