আন্তঃআণবিক বল: সংশোধিত সংস্করণের মধ্যে পার্থক্য
সম্পাদনা সারাংশ নেই ট্যাগ: দৃশ্যমান সম্পাদনা মোবাইল সম্পাদনা মোবাইল ওয়েব সম্পাদনা |
সম্পাদনা সারাংশ নেই ট্যাগ: দৃশ্যমান সম্পাদনা মোবাইল সম্পাদনা মোবাইল ওয়েব সম্পাদনা |
||
| ২০ নং লাইন: | ২০ নং লাইন: | ||
== হাইড্রোজেন বন্ধন == |
== হাইড্রোজেন বন্ধন == |
||
হাইড্রোজেন বন্ধন হচ্ছে নিঃসঙ্গ ইলেকট্রন যুগলধারী [[তড়িৎ ঋণাত্মকতা|তড়িৎ ঋণাত্বক]] পরমাণুর সাথে হাইড্রোজেন পরমানুর মধ্যকার আকর্ষন বল। সাধারণত [[হাইড্রোজেন]]-র সাথে [[নাইট্রোজেন]], [[অক্সিজেন]], [[ফ্লোরিন]] যুক্ত হয়ে এই বন্ধন গঠিত হয়<ref>{{সাময়িকী উদ্ধৃতি|ইউআরএল=https://en.wikipedia.org/wiki/Intermolecular_force#cite_note-GoldBook-H02899-2|শিরোনাম=IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997)|শেষাংশ=|প্রথমাংশ=|তারিখ=2020-09-23|সাময়িকী=Wikipedia|ভাষা=en|সংগ্রহের-তারিখ=}}</ref>। হাইড্রোজেন বন্ধনকে প্রায়ই শক্তিশালী তড়িৎ(ইলেকট্রিক) মেরু-মেরু(ডাইপোল-ডাইপোল) |
হাইড্রোজেন বন্ধন হচ্ছে নিঃসঙ্গ ইলেকট্রন যুগলধারী [[তড়িৎ ঋণাত্মকতা|তড়িৎ ঋণাত্বক]] পরমাণুর সাথে হাইড্রোজেন পরমানুর মধ্যকার আকর্ষন বল। সাধারণত [[হাইড্রোজেন]]-র সাথে [[নাইট্রোজেন]], [[অক্সিজেন]], [[ফ্লোরিন]] যুক্ত হয়ে এই বন্ধন গঠিত হয়<ref>{{সাময়িকী উদ্ধৃতি|ইউআরএল=https://en.wikipedia.org/wiki/Intermolecular_force#cite_note-GoldBook-H02899-2|শিরোনাম=IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997)|শেষাংশ=|প্রথমাংশ=|তারিখ=2020-09-23|সাময়িকী=Wikipedia|ভাষা=en|সংগ্রহের-তারিখ=}}</ref>। হাইড্রোজেন বন্ধনকে প্রায়ই শক্তিশালী তড়িৎ (ইলেকট্রিক) মেরু-মেরু (ডাইপোল-ডাইপোল) ক্রিয়া হিশেবে বর্ণনা করা হয়। সমযোজী বন্ধনের মত এতেও কিছু বৈশিষ্ট্য আছে: এটা দিকমুখী, ভ্যানডার ওয়ালস বল থেকে শক্তিশালী, আন্তঃআণবিক দূরত্ব ভ্যানডার ওয়ালস বলে মৌলদ্বয়ের ব্যাসার্ধের যোগফল অপেক্ষা কম এবং যোজ্যতানুসারে সীমিত-সংখ্যক মৌলের সাথেও যুক্ত হয়। মৌলদ্বয় দ্বারা গঠিত হাইড্রোজেন বন্ধনের সংখ্যা তাদের সক্রিয় ইলেকট্রন যুগলের সমান। যে মৌল ইলেকট্রন দান করে([[হাইড্রোজেন]]) তাকে দাতা, আর ইলেকট্রন গ্রহণকারী নিঃসঙ্গ ইলেকট্রন যুগলধারী [[তড়িৎ ঋণাত্মকতা|তড়িৎ ঋণাত্বক]] পরমাণুকে গ্রহীতা বলে। সক্রিয় যুগলের মান বন্ধনে [[হাইড্রোজেন]] পরমাণুর ইলেকট্রন দান এবং [[তড়িৎ ঋণাত্মকতা|তড়িৎ ঋণাত্বক]] পরমাণুর ইলেকট্রন গ্রহণ সংখ্যার সমান।[[File:Hydrogen-bonding-in-water-2D.png|)|alt=]] |
||
যদিও চিত্রে ঠিকভাবে বর্নণা করা যাচ্ছে না, পানির অণুতে ২টি সক্রিয় যুগল থাকে, [[অক্সিজেন]] পরমাণু ২টি [[হাইড্রোজেন]] পরমাণুর এর সাথে ২টি হাইড্রোজেন বন্ধন গঠন করে। আন্তঃআণবিক হাইড্রোজেন বন্ধনই পানির উচ্চ গলনাঙ্কের(১০০ °C) জন্য দায়ী। অন্তঃআণবিক হাইড্রোজেন বন্ধন প্রোটিন এবং নিউক্লিক এসিডসমূহের সেকেন্ডারি(২), টার্শিয়ারি(৩) এবং কোয়াটার্নারি(৪) গঠনের জন্য দায়ী। এছাড়াও পলিমারের প্রাকৃতিক এবং কৃত্রিম উভয় গঠনেই অন্তঃআণবিক হাইড্রোজেন বন্ধন গুরুত্বপূর্ণ ভূমিকা রাখে।<ref>{{সাময়িকী উদ্ধৃতি|ইউআরএল=https://en.wikipedia.org/wiki/Intermolecular_force#cite_note-3|শিরোনাম=Lindh, Ulf (2013), "Biological functions of the elements", in Selinus, Olle (ed.), Essentials of Medical Geology (Revised ed.), Dordrecht: Springer, pp. 129–177, doi:10.1007/978-94-007-4375-5_7, ISBN 978-94-007-4374-8|শেষাংশ=|প্রথমাংশ=|তারিখ=2020-09-23|সাময়িকী=Wikipedia|ভাষা=en|সংগ্রহের-তারিখ=}}</ref> |
যদিও চিত্রে ঠিকভাবে বর্নণা করা যাচ্ছে না, পানির অণুতে ২টি সক্রিয় যুগল থাকে, [[অক্সিজেন]] পরমাণু ২টি [[হাইড্রোজেন]] পরমাণুর এর সাথে ২টি হাইড্রোজেন বন্ধন গঠন করে। আন্তঃআণবিক হাইড্রোজেন বন্ধনই পানির উচ্চ গলনাঙ্কের(১০০ °C) জন্য দায়ী। অন্তঃআণবিক হাইড্রোজেন বন্ধন প্রোটিন এবং নিউক্লিক এসিডসমূহের সেকেন্ডারি(২), টার্শিয়ারি(৩) এবং কোয়াটার্নারি(৪) গঠনের জন্য দায়ী। এছাড়াও পলিমারের প্রাকৃতিক এবং কৃত্রিম উভয় গঠনেই অন্তঃআণবিক হাইড্রোজেন বন্ধন গুরুত্বপূর্ণ ভূমিকা রাখে।<ref>{{সাময়িকী উদ্ধৃতি|ইউআরএল=https://en.wikipedia.org/wiki/Intermolecular_force#cite_note-3|শিরোনাম=Lindh, Ulf (2013), "Biological functions of the elements", in Selinus, Olle (ed.), Essentials of Medical Geology (Revised ed.), Dordrecht: Springer, pp. 129–177, doi:10.1007/978-94-007-4375-5_7, ISBN 978-94-007-4374-8|শেষাংশ=|প্রথমাংশ=|তারিখ=2020-09-23|সাময়িকী=Wikipedia|ভাষা=en|সংগ্রহের-তারিখ=}}</ref> |
||
১৩:৫৭, ১০ অক্টোবর ২০২০ তারিখে সংশোধিত সংস্করণ
এই নিবন্ধ বা অনুচ্ছেদটি পরিবর্ধন বা বড় কোনো পুনর্গঠনের মধ্যে রয়েছে। এটির উন্নয়নের জন্য আপনার যে কোনো প্রকার সহায়তাকে স্বাগত জানানো হচ্ছে। যদি এই নিবন্ধ বা অনুচ্ছেদটি কয়েকদিনের জন্য সম্পাদনা করা না হয়, তাহলে অনুগ্রহপূর্বক এই টেমপ্লেটটি সরিয়ে ফেলুন। ৩ বছর আগে Khalid Hasan Shohag (আলাপ | অবদান) এই নিবন্ধটি সর্বশেষ সম্পাদনা করেছেন। (হালনাগাদ) |
অবদানকারীর মন্তব্য: নতুন নিবন্ধ |
আন্তঃআণবিক বল হচ্ছে দুটি পরমাণুর মধকার আকর্ষণ বা বিকর্ষণ বল, যা পরমাণুর মত অন্য কণার(আয়ন) মধ্যেও বিরাজ করে। আন্তঃআণবিক বল, অন্তঃআণবিক বল(যে বল মৌলের পরমাণুগুলোকে একত্রে ধরে রাখে) অপেক্ষা দুর্বল প্রকৃতির। যেমনঃ সমযোজী বন্ধন, যেখানে দুটি পরমাণু ইলেকট্রন যুগল শেয়ার করে তা আন্তঃআণবিক বল অপেক্ষা বেশি শক্তিশালী। উভয় প্রকার বলই বল ক্ষেত্রের প্রয়োজনীয় অংশ যা আণবিক গতিবিদ্যায় প্রায়ই ব্যবহৃত হয়।
আন্তঃআণবিক বলের অনুসন্ধান শুরু হয় সূক্ষ্ম পর্যবেক্ষণের ফলে যখন আণবিক পর্যায়ে বলের উপস্থিতি এবং ক্রিয়া সম্পর্কে ধারণা পাওয়া যায়। এসব পর্যবেক্ষণের মধ্যে বাস্তব গ্যাসের তাপগতিবিজ্ঞান এর আচরণ যেমন- ভাইরাল সহগ(Virial coefficient), বাষ্প চাপ, সান্দ্রতা, পৃষ্ঠটান, শোষণ উল্লেখযোগ্য।
আণবিক বল সম্পর্কে প্রথম ধারণা পাওয়া যায় আলেক্সিস ক্লেইরটের কাজ Theorie de la Figure de la Terre[১] এ। অন্যান্য বিজ্ঞানী যারা একাজে অবদান রেখেছেন তারা হলেন: পিয়ের সিমোঁ লাপ্লাস, কার্ল ফ্রিডরিশ গাউস, জেমস ক্লার্ক ম্যাক্সওয়েল, এবং লুডভিগ বোলৎসমান।
আন্তঃআণবিক আকর্ষন বলকে নিমোক্তভাগে ভাগ করা যায়:
•হাইড্রোজেন বন্ধন /H-বন্ধন
•আয়ন-সংঘটিত/আবেশিত ডাইপোল বল
•আয়ন-ডাইপোল বল
হাইড্রোজেন বন্ধন
হাইড্রোজেন বন্ধন হচ্ছে নিঃসঙ্গ ইলেকট্রন যুগলধারী তড়িৎ ঋণাত্বক পরমাণুর সাথে হাইড্রোজেন পরমানুর মধ্যকার আকর্ষন বল। সাধারণত হাইড্রোজেন-র সাথে নাইট্রোজেন, অক্সিজেন, ফ্লোরিন যুক্ত হয়ে এই বন্ধন গঠিত হয়[২]। হাইড্রোজেন বন্ধনকে প্রায়ই শক্তিশালী তড়িৎ (ইলেকট্রিক) মেরু-মেরু (ডাইপোল-ডাইপোল) ক্রিয়া হিশেবে বর্ণনা করা হয়। সমযোজী বন্ধনের মত এতেও কিছু বৈশিষ্ট্য আছে: এটা দিকমুখী, ভ্যানডার ওয়ালস বল থেকে শক্তিশালী, আন্তঃআণবিক দূরত্ব ভ্যানডার ওয়ালস বলে মৌলদ্বয়ের ব্যাসার্ধের যোগফল অপেক্ষা কম এবং যোজ্যতানুসারে সীমিত-সংখ্যক মৌলের সাথেও যুক্ত হয়। মৌলদ্বয় দ্বারা গঠিত হাইড্রোজেন বন্ধনের সংখ্যা তাদের সক্রিয় ইলেকট্রন যুগলের সমান। যে মৌল ইলেকট্রন দান করে(হাইড্রোজেন) তাকে দাতা, আর ইলেকট্রন গ্রহণকারী নিঃসঙ্গ ইলেকট্রন যুগলধারী তড়িৎ ঋণাত্বক পরমাণুকে গ্রহীতা বলে। সক্রিয় যুগলের মান বন্ধনে হাইড্রোজেন পরমাণুর ইলেকট্রন দান এবং তড়িৎ ঋণাত্বক পরমাণুর ইলেকট্রন গ্রহণ সংখ্যার সমান।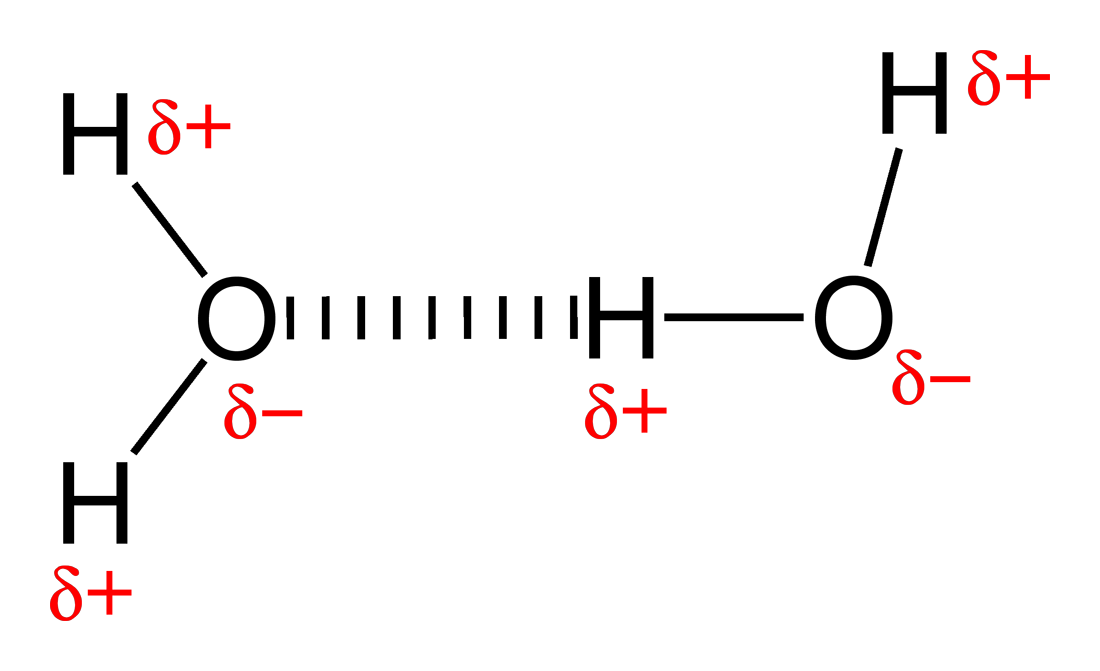
যদিও চিত্রে ঠিকভাবে বর্নণা করা যাচ্ছে না, পানির অণুতে ২টি সক্রিয় যুগল থাকে, অক্সিজেন পরমাণু ২টি হাইড্রোজেন পরমাণুর এর সাথে ২টি হাইড্রোজেন বন্ধন গঠন করে। আন্তঃআণবিক হাইড্রোজেন বন্ধনই পানির উচ্চ গলনাঙ্কের(১০০ °C) জন্য দায়ী। অন্তঃআণবিক হাইড্রোজেন বন্ধন প্রোটিন এবং নিউক্লিক এসিডসমূহের সেকেন্ডারি(২), টার্শিয়ারি(৩) এবং কোয়াটার্নারি(৪) গঠনের জন্য দায়ী। এছাড়াও পলিমারের প্রাকৃতিক এবং কৃত্রিম উভয় গঠনেই অন্তঃআণবিক হাইড্রোজেন বন্ধন গুরুত্বপূর্ণ ভূমিকা রাখে।[৩]
আয়নিক বন্ধন
প্রধান নিবন্ধ: আয়নিক বন্ধন
আয়নিক বন্ধন হচ্ছে ক্যাটায়ন এবং অ্যানায়ন এর মধ্যকার আকর্ষণ বল যেখানে কোনো ইলেকট্রনের শেয়ার হয় না, অথবা আন্তঃআণবিক ক্রিয়া যাকে আয়ন একীভূত(ক্যাটায়ন এবং অ্যানায়ন) বা লবণ সেতু বলা হয়[৪]। এর জন্য তড়িৎ বল প্রয়োজনীয়, যদিও প্রায়ই তাপহারী প্রক্রিয়া ও এনট্রপির মাধ্যমে চালিত হয়। কেলাসের বেশিরভাগ লবণের আয়নেরই আলাদা বৈশিষ্ট্য থাকে। অন্য অনেক তড়িতচুম্বক ক্রিয়ার মত লবণ সেতুসমূহ দিকবিহীন এবং কঠিন অবস্থায় তারা ভ্যানডার ওয়ালস বলের মাধ্যমে যুক্ত থাকে। একই লবণ সেতুতে জৈব আয়নের সাথে সাথে অজৈব আয়ন পানিতে আয়নিক শক্তি l প্রদর্শন করে, যেখানে ΔG এর মান ৫-৬ kJ/mol এর কাছাকাছি, (১ঃ১=ক্যাটায়নঃঅ্যানায়ন, স্বাধীন অবস্থায়)[৫] । ΔG এর মান সংযোজিত এবং বলা যায় চার্জের লিনিয়ার ফাংশন, দুই আধান বিশিষ্ট ফসফেট অ্যানায়ন একক আধান বিশিষ্ট অ্যামোনিয়াম ক্যাটায়ন যুক্ত হলে তাদের ΔG= ২x৫= ১০ kJ/mol। হাকেলের নীতি অনুসারে ΔG এর মান দ্রবণের আয়নিক শক্তির উপর নির্ভর করে, শূন্য আয়নিক শক্তিতে ΔG এর মান ৮ kJ/mol।
ডাইপোল-ডাইপোল এবং সমধর্মী মিথস্ক্রিয়া
নিয়মিত ডাইপোল
ডাইপোল-ডাইপোল বল হছে অণুসমূহের মধ্যকার তড়িৎ(স্থির) ক্রিয়া যাদের স্থায়ী ডাইপোল বিদ্যমান। এটা লন্ডন বল অপেক্ষা শক্তিশালী কিন্তু আয়নিক বন্ধন অপেক্ষা দুর্বল প্রকৃতির; কারণ এতে আংশিক আধান(ক্যাটায়ন বা অ্যানায়ন) বিদ্যমান। এটা অণুসমূহের নিজেদের মধ্যকার আকর্ষণ বৃদ্ধিতে ভূমিকা রাখে (বিভব শক্তি হ্রাস পায়)।হাইড্রোজেন বন্ধন একপ্রকার ডাইপোল-ডাইপোল আকর্ষণ বল। যেহেতু পরমাণুর মধ্যে ডাইপোলের ব্যপারটা লক্ষ্য করা যায় না, তাই দুটি ভিন্ন পরমাণুর মধ্যকার ডাইপোল-ডাইপোল আকর্ষণ বল সাধারণত শুন্য।
আয়ন-ডাইপোল এবং আয়ন-আবেশ ডাইপোল বল
আয়ন-ডাইপোল এবং আয়ন-আবেশ ডাইপোল বল, ডাইপোল-ডাইপোল এবং ডাইপোল-আবেশ ডাইপোল এর মতই কিন্তু এখানে শুধু পোলার এবং অপোলার অণুর পরিবর্তে আয়ন থাকে। আয়ন-ডাইপোল এবং আয়ন-আবেশ ডাইপোল বল, ডাইপোল-ডাইপোল বল থেকে শক্তিশালী, কারণ যেকোন আয়নের আধান ডাইপোল মোমেন্টের আধান থেকে অনেক বেশি। আয়ন-ডাইপোল বন্ধন হাইড্রোজেন বন্ধন থেকে শক্তিশালী।[৬]
একটি আয়ন এবং একটি পোলার অণু আয়ন-ডাইপোল বলের মাধ্যমে যুক্ত হয়।তারা সর্বোচ্চ আকর্ষণে এমনভাবে থাকে যাতে ধনাত্বক এবং ঋনাত্বক অংশ একে অপরের পর পর থাকে। উদাহরণ হিশেবে পানিতে আয়নের হাইড্রেশন, যা হাইড্রেশন এনথালপির মান বৃদ্ধি করে। পানির পোলার অণুসমূহ নিজেদের পানিতে আয়নের(বহিরাগত) চারপাশ ঘিরে ধরে এবং সেই সময়ে যে পরিমাণ শক্তি নির্গত করে তাকে হাইড্রেশন এনথালপি বলে। পানিতে বিভিন্ন আয়নের স্থায়িত্ব নির্ণয়ে এ প্রক্রিয়া গুরুত্বপূর্ণ।
একটি আয়ন এবং একটি অপোলার অণু আয়ন-আবেশ ডাইপোল বলের মাধ্যমে যুক্ত হয়।এক্ষেত্রে ডাইপোল-আবেশ ডাইপোল বলের মতই, আয়নের আধানের কারণে অপোলার অণুর ইলেকট্রন মেঘ বিকৃত(স্থানান্তর) হয়।[৭]
ভ্যানডার ওয়ালস বল
আধানবিহীন পরমাণু বা অণুসমূহ এর মধ্যকার মিথস্ক্রিয়া থেকে ভ্যানডার ওয়ালস বল এসেছে। এছাড়াও বিভিন্ন ঘনীভূত পর্যায়, গ্যাসের শোষণ এবং জগতের ক্ষুদ্র দেহগুলোর আকর্ষণ থেকেও এসেছে।[৮]
কেসম (স্থায়ী-স্থায়ী ডাইপোল) বল
আধানসমূহের মধ্যে স্থির তড়িৎ ক্রিয়া(অণুর আয়নে), ডাইপোলসমূহ(অপোলার অণু), কোয়াড্রপোল(সকল অণু যা কিউবিকের চেয়ে কম প্রতিসাম্য) এবং স্থায়ী মাল্টিপোল এর জন্য দায়ী কেসম বল(উইলিয়াম হেন্ড্রিক কেসমের নামে) যা ভ্যানডার ওয়ালস বলের প্রথম অবদান।[৯] স্থায়ী ডাইপোলসমূহের মধ্যকার আকর্ষণ থেকে এ বলের উৎপত্তি এবং তাপমাত্রার উপর নির্ভরশীল।[৮]
এটা ডাইপোলসমূহের মধ্যকার আকর্ষণ বল যা বিভিন্ন ঘূর্ণন কাঠামো ডাইপোলের জড়ো গড় নিয়ে গঠিত। এটা ধারণা করা হয় যে অণুসমূহ প্রতিনিয়ত ঘুরতে থাকে এবং কখনোই এক জায়গায় স্থির থাকে না। এটা যদিও ভালো ধারণা, কিন্তু কোন কোন বিন্দুতে অণুসমূহ স্থির থাকে। কেসম বলের শক্তি দূরত্বের(অণুসমূহের) ষষ্ঠ ঘাতের বিপরীত মানের উপর নির্ভর করে। কেসম বল কেবল সেইসব অণুর মধ্যে ঘটতে পারে যাদের স্থায়ী ডাইপোল বিদ্যমান। কেসম খুবই দুর্বল প্রকৃতির ভ্যানডার ওয়ালস বল এবং জলীয় দ্রবণে ঘটে না। কৌণিক গড়ের সমীকরণ:
যেখানে m = ডাইপোল মোমেন্ট, = ফাকা জায়গার অনুমতি, = ডাইলেকট্রিক ধ্রুবক, T = তাপমাত্রা, = বোলসম্যান ধ্রুবক, and r = অণুসমূহের মধ্যকার দূরত্ব।
ডিবাই (স্থায়ী-আবেশ ডাইপোল) বল
ভ্যানডার ওয়ালস বলের দ্বিতীয় অবদান। স্থায়ী ডাইপোলসমূহের ঘূর্ণন এবং পরমাণু ও অণুসমূহের (আবেশ ডাইপোল) মধ্যকার সম্পর্ক থেকে ডিবাই বল এসেছে। যখন একটি অণুর স্থায়ী ডাইপোল অপর অণুর ইলেকট্রনগুলোকে সরিয়ে দেয় তখন আবেশ ডাইপোলের সৃষ্টি হয়। স্থায়ী ডাইপোলধারী অণু নিজ ধর্মের অন্য অণুকে আবেশিত করে এবং পারস্পরিক আকর্ষণ ঘটায়। এই বল কেসম বলের মত তাপমাত্রার উপর নির্ভর করে না কারণ আবেশ ডাইপোলের স্থানান্তর ঘটতে পারে এবং পোলার অণুর চারপাশ ঘুরতে পারে। ডিবাই আবেশ প্রভাব এবং কেসম কাঠামো প্রভাবকে পোলার ক্রিয়া বলা হয়।[৮] বিজ্ঞানী পিটার জে. ডব্লিউ. ডিবাইয়ের নামানুসারে ডিবাই বলের নামকরণ করা হয়েছে।
এ বলের একটি উদাহরণ হচ্ছে HCl এবং Ar এর মধ্যকার বল। HCl এর প্রভাবে Ar এর ইলেকট্রন H এর দিকে ধাবিত হয় অথবা Cl এর কারণে দূরে সরে যায়, ফলে Ar এ আবেশ ডাইপোলের সৃষ্টি হয়।[১০] [১১] কৌণিক গড়ের সমীকরণ:
যেখানে = পোলার যোগ্যতা।
পোলার এবং অ-পোলার অণুর মধ্যে এধরণের বল দেখা যায়। এ বল ডাইপোল-ডাইপোল বল থেকে দুর্বল, কিন্তু লন্ডন বল অপেক্ষা শক্তিশালী।
লন্ডন বল
ভ্যানডার ওয়ালস বলের তৃতীয় এবং প্রধান অবদান। পরমাণু এবং অণুসমূহের ক্ষণস্থায়ী অ-শুন্য ডাইপোলের কারণে এ বল উঠে এসেছে। এধরণের পোলারাইজেশন হয় পোলার অণু দ্বারা বা অ-পোলার অণুতে ঋণাত্বক আধানবিশিষ্ট ইলেকট্রন মেঘের বিকৃতি দ্বারা।এভাবে ইলেকট্রন মেঘে ইলেকট্রন ঘনত্বের এলোমেলো অবস্থার কারণে লন্ডন বল সংঘটিত হয়। কম ইলেকট্রনবিশিষ্ট পরমাণু থেকে বেশি ইলেকট্রনবিশিষ্ট পরমাণু লন্ডন বলে বেশি সহায়ক। লন্ডন বল সবচেয়ে গুরুত্বপূর্ণ উপাদান কারণ সকল উপাদানেই পোলারাইজেশন ঘটে, অন্যদিকে কেসম এবং ডিবাই বলে স্থায়ী ডাইপোলের দরকার পড়ে। লন্ডন বল চিরন্তন এবং পরমাণু-পরমাণু(দুটি পরমাণুর মধ্যকার) বলেও উপস্থিত। বিভিন্ন কারণে, সংক্ষিপ্ত পদ্ধতিতে বৃহদাকার বস্তুসমূহের মধ্যকার ক্রিয়ায় লন্ডন বলকে প্রাসঙ্গিক ধরা হয়। ১৯৩৭ সালে হ্যামেকার বৃহদাকার বস্তুসমূহের মধ্যকার ভ্যানডার ওয়ালস বলের তত্ব বিকশিত করেন এবং দেখান যে এইসব ক্রিয়ার সংযোজন তাদেরকে(বস্তু) দীর্ঘ পরিসীমা প্রদান করে।[৮]
বলসমূহের আপেক্ষিক শক্তিমত্তা
| বন্ধনের প্রকার | পৃথকীকরণ শক্তি (kcal/mol)[১২] |
পৃথকীকরণ শক্তি
(kJ/mol) |
মন্তব্য |
|---|---|---|---|
| আয়নিক বন্ধন | ২৫০–৪০০০[১৩] | ১১০০-২০০০০ | |
| সমযোজী বন্ধন | ৩০–২৬০ | ১৩০–১১০০ | |
| হাইড্রোজেন বন্ধন | ১-১২ | ৪-৫০ | পানিতে ৫ kcal/mol (২১ kJ/mol) এর কাছাকাছি |
| ডাইপোল-ডাইপোল | .৫-২ | ২-৮ | |
| লন্ডন বল | <১-১৫ | <৪-৬৩ | হাইড্রোকার্বনের বাষ্পীভবনের এনথালপি থকে অনুমানিত[১৪] |
এই তুলনা পায় কাছাকাছি।আসলে কী ধরণের অণু অন্তর্ভূক্ত তার উপর আপেক্ষিক শক্তিমত্তা বদলায়। আয়নিক বন্ধন এবং সমযোজী বন্ধন সর্বদা যেকোন পদার্থের আন্তঃআণবিক বল অপেক্ষা শক্তিশালী।
গ্যাসের আচরণের উপর প্রভাব
আন্তঃআণবিক বল কম দূরত্বে বিকর্ষণমূলক এবং বেশি দূরত্বে আকর্ষণমূলক হয়। গ্যাসে বিকর্ষণমূলক বল প্রধানত একই আয়তনের দুটি অণুর মধ্যকার প্রভাব। এতে একই তাপমাত্রা এবং চাপে আদর্শ গ্যাস অপেক্ষা বাস্তব গ্যাসের বেশি আয়তন দখলের প্রবণতা দেখা যায়। অন্যদিকে আকর্ষণ বল অণুসমূহকে কাছাকাছি নিয়ে আসে, ফলে একই তাপমাত্রা এবং চাপে আদর্শ গ্যাস অপেক্ষা বাস্তব গ্যাসের কম আয়তন দখলের প্রবণতা দেখা যায়।
গ্যাসে অণুসমূহের মধ্যকার দূরত্ব সাধারণত বেশি থাকে, তাই আন্তঃআণবিক বলের দূরত্ব খুব কম লক্ষ্য করা যায়। আকর্ষণ বল বিকর্ষণ বলকে অতিক্রম করতে পারে না, কিন্তু তাপ শক্তি পারে। তাপমাত্রা তাপ শক্তির পরিমাপ, তাই তাপমাত্রা যত বাড়ে আকর্ষণ বলের প্রভাব তত কমে। অন্যদিকে, তাপমাত্রা বিকর্ষণ বলের কোন পরিবর্তন ঘটাতে পারে না।
যখন গ্যাসকে সঙ্কুচিত করে ঘনত্ব বৃদ্ধি করা হয়, তখন আকর্ষণ বলের প্রভাব বৃদ্ধি পায়। গ্যাসকে যদি পর্যাপ্ত ঘন করা হয়, আকর্ষণ বল এতই বৃদ্ধি পায় যে তা তাপগতিকে অতিক্রম করে অণুসমূহের বিচ্যুতি ঘটায়। তখন গ্যাস তরল বা কঠিনে রূপান্তরিত হয়। যেমনঃ ঘনীভূত পর্যায় (পানি, বরফ)। কম তাপমাত্রা ঘনীভূত পর্যায়ের আনুকূল্য। এ পর্যায়ে, আকর্ষণ ও বিকর্ষণ বলের মধ্যে প্রায় সাম্যতা বিরাজ করে।
কোয়ান্টাম মেকানিক্যাল তত্ত্ব
উপরে বর্ণিত, অণু এবং পরমাণুসমূহের মধ্যকার আন্তঃআণবিক বল ঘটনাগতভাবে স্থায়ী এবং আবেশিত ডাইপোলের মধ্যে ঘটে। অন্যদিকে, কেউ একটি মৌলিক, সমন্বয় তত্ত্ব চাইতে পারেন যা বিভিন্ন প্রকার ক্রিয়া যেমনঃ হাইড্রোজেন বন্ধন, ভ্যানডার ওয়ালস বল এবং ডাইপোল-ডাইপোল বল ব্যাখ্যা করবে। সাধারণত, অণুসমূহে কোয়ান্টাম গতিবিদ্যার ধারণা প্রয়োগ এবং রেইলি-স্রোডিঞ্জারের বিচলন তত্ত্ব ( perturbation theory) বিশেষ প্রভাব হিশেবে বিবেচনা করা হয়। যখন কোয়ান্টাম কেমিস্ট্রি প্রয়োগ করা হয়, তখন প্রায় সদৃশ পদ্ধতির কিছু বিন্যাস এই আন্তঃআণবিক ক্রিয়াকে বিশ্লেষণ করে। এই প্রকার আন্তঃআণবিক ক্রিয়া দৃশ্যমান করার সবচেয়ে উপযোগী পদ্ধতি কোয়ান্টাম কেমিস্ট্রিতে পাওয়া যায়, যাকে অ-সমযোজী মিথস্ক্রিয়া ইনডেক্স (non-covalent interaction index বলে, যা ইলেকট্রন ঘনত্বের উপর নির্ভর করে। লন্ডন বল এতে বড় ভূমিকা রাখে।
- ↑ "Margenau, H. and Kestner, N. (1969) Theory of inter-molecular forces, International Series of Monographs in Natural Philosophy, Pergamon Press, ISBN 1483119289"। Wikipedia (ইংরেজি ভাষায়)। ২০২০-০৯-২৩।
- ↑ "IUPAC, Compendium of Chemical Terminology, 2nd ed. (the "Gold Book") (1997)"। Wikipedia (ইংরেজি ভাষায়)। ২০২০-০৯-২৩।
- ↑ "Lindh, Ulf (2013), "Biological functions of the elements", in Selinus, Olle (ed.), Essentials of Medical Geology (Revised ed.), Dordrecht: Springer, pp. 129–177, doi:10.1007/978-94-007-4375-5_7, ISBN 978-94-007-4374-8"। Wikipedia (ইংরেজি ভাষায়)। ২০২০-০৯-২৩।
- ↑ Ionic interactions in natural and synthetic macromolecules। Ciferri, A., Perico, Angelo.। Hoboken, NJ: Wiley। ২০১২। আইএসবিএন 978-1-118-16586-7। ওসিএলসি 778434029।
- ↑ Biedermann, Frank; Schneider, Hans-Jörg (২০১৬-০৫-১১)। "Experimental Binding Energies in Supramolecular Complexes"। Chemical Reviews (ইংরেজি ভাষায়)। 116 (9): 5216–5300। আইএসএসএন 0009-2665। ডিওআই:10.1021/acs.chemrev.5b00583।
- ↑ Tro, Nivaldo J.। Chemistry : a molecular approach (Second edition সংস্করণ)। Upper Saddle River, NJ। আইএসবিএন 978-0-321-65178-5। ওসিএলসি 324783713।
- ↑ Zeegers-Huyskens, Th.; Huyskens, P. (১৯৯১)। Intermolecular Forces। Berlin, Heidelberg: Springer Berlin Heidelberg। পৃষ্ঠা 1–30। আইএসবিএন 978-3-642-76262-8।
- ↑ ক খ গ ঘ Leite, Fabio L.; Bueno, Carolina C.; Da Róz, Alessandra L.; Ziemath, Ervino C.; Oliveira, Osvaldo N. (২০১২-১০-০৮)। "Theoretical Models for Surface Forces and Adhesion and Their Measurement Using Atomic Force Microscopy"। International Journal of Molecular Sciences। 13 (12): 12773–12856। আইএসএসএন 1422-0067। ডিওআই:10.3390/ijms131012773।
- ↑ Saksena, M.P.; Saxena, S.C. (1965-08)। "Second virial coefficient of non-polar non-spherical molecules"। Physics Letters। 18 (2): 120–122। আইএসএসএন 0031-9163। ডিওআই:10.1016/0031-9163(65)90679-7। এখানে তারিখের মান পরীক্ষা করুন:
|তারিখ=(সাহায্য) - ↑ Blustin, Peter H. (১৯৭৮)। [http://dx.doi.org/10.1007/bf00577166 "A Floating Gaussian Orbital calculation on argon hydrochloride (Ar � HCl)"]। Theoretica Chimica Acta। 47 (3): 249–257। আইএসএসএন 0040-5744। ডিওআই:10.1007/bf00577166। replacement character in
|শিরোনাম=at position 68 (সাহায্য) - ↑ Roberts, J. K.; Orr, W. J. C. (১৯৩৮)। "Induced dipoles and the heat of adsorption of argon on ionic crystals"। Transactions of the Faraday Society। 34: 1346। আইএসএসএন 0014-7672। ডিওআই:10.1039/tf9383401346।
- ↑ Ege, Seyhan (2003) Organic Chemistry: Structure and Reactivity. Houghton Mifflin College. আইএসবিএন ০৬১৮৩১৮০৯৭. pp. 30–33, 67.
- ↑ "Lattice Energies"। সংগ্রহের তারিখ ২০১৪-০১-২১।
- ↑ Majer, V. and Svoboda, V. (1985) Enthalpies of Vaporization of Organic Compounds, Blackwell Scientific Publications, Oxford. আইএসবিএন ০৬৩২০১৫২৯২.






