ক্যালসিয়াম ব্রোমাইড
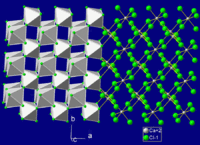
| |
| নামসমূহ | |
|---|---|
| ইউপ্যাক নাম
ক্যালসিয়াম ব্রোমাইড
| |
| অন্যান্য নাম
ক্যালসিয়াম ডাইব্রোমাইড
| |
| শনাক্তকারী | |
| |
ত্রিমাত্রিক মডেল (জেমল)
|
|
| সিএইচইবিআই | |
| কেমস্পাইডার | |
| ইসিএইচএ ইনফোকার্ড | ১০০.০২৯.২৪০ |
| ইসি-নম্বর |
|
পাবকেম CID
|
|
| আরটিইসিএস নম্বর |
|
| ইউএনআইআই | |
কম্পটক্স ড্যাশবোর্ড (EPA)
|
|
| |
| |
| বৈশিষ্ট্য | |
| CaBr2 | |
| আণবিক ভর | ১৯৯.৮৯ গ্রাম/মোল (অনার্দ্র) ২৩৫.৯৮ g/mol (ডাইহাইড্রেট) |
| বর্ণ | অনার্দ্র অবস্থায় জলগ্রাহী বর্ণহীন স্ফটিক তীক্ষ্ণ লবণাক্ত স্বাদ |
| ঘনত্ব | ৩.৩৫৩ g/cm3 |
| গলনাঙ্ক | ৭৩০ °সে (১,৩৫০ °ফা; ১,০০০ K) |
| স্ফুটনাঙ্ক | ১,৮১৫ °সে (৩,২৯৯ °ফা; ২,০৮৮ K) (অনার্দ্র) ৮১০°সে (ডাইহাইড্রেট) |
| 125 g/100 mL (0 °C) 143 g/100 mL (20 °C) 312 g/100 mL (100 °C) | |
| দ্রাব্যতা in alcohol, acetone | দ্রবণীয় |
| অম্লতা (pKa) | 9 |
| -73.8·10−6 cm3/mol | |
| গঠন | |
| স্ফটিক গঠন | রম্বয়েড |
| তাপ রসায়নবিদ্যা | |
| তাপ ধারকত্ব, C | 75 J/mol K |
| স্ট্যন্ডার্ড মোলার এন্ট্রোফি এস |
130 J/mol K |
| গঠনে প্রমান এনথ্যাল্পির পরিবর্তন ΔfH |
-647.9 kJ/mol |
গিবসের মুক্ত শক্তি (ΔfG˚)
|
-656.1 kJ/mol |
| ঝুঁকি প্রবণতা | |
| এনএফপিএ ৭০৪ | |
| প্রাণঘাতী ডোজ বা একাগ্রতা (LD, LC): | |
LD৫০ (মধ্যমা ডোজ)
|
4100 mg/kg (rat, oral) 1580 mg/kg (mouse, subcutaneous) |
| সম্পর্কিত যৌগ | |
অন্যান্য অ্যানায়নসমূহ
|
Calcium fluoride Calcium chloride Calcium iodide |
অন্যান্য ক্যাটায়নসমূহ
|
Beryllium bromide Magnesium bromide Strontium bromide Barium bromide Radium bromide |
সুনির্দিষ্টভাবে উল্লেখ করা ছাড়া, পদার্থসমূহের সকল তথ্য-উপাত্তসমূহ তাদের প্রমাণ অবস্থা (২৫ °সে (৭৭ °ফা), ১০০ kPa) অনুসারে দেওয়া হয়েছে। | |
| তথ্যছক তথ্যসূত্র | |
ক্যালসিয়াম ব্রোমাইড একটি অজৈব যৌগ যার রাসায়নিক সংকেত CaBr2। এটি ক্যালসিয়াম এবং ব্রোমিনের একটি যৌগ।
প্রস্তুতি[সম্পাদনা]
ক্যালসিয়াম কার্বনেট, ক্যালসিয়াম অক্সাইডের সাথে হাইড্রোব্রোমিক অ্যাসিডের বিক্রিয়া করে ক্যালসিয়াম ব্রোমাইড তৈরি করা হয়I এছাড়া ব্রোমিন মৌলের সাথে ক্যালসিয়াম ধাতুর বিক্রিয়া ঘটিয়েও ক্যালসিয়াম ব্রোমাইড তৈরি করা যায়I[১]
ধর্ম[সম্পাদনা]
ক্যালসিয়াম ব্রোমাইড এমনিতে বর্ণহীন কঠিন পদার্থ। এটি জলগ্রাহী পদার্থ। অনার্দ্র অবস্থায় জলের থেকে তিন গুণেরও বেশি ভারী। এর ঘনত্ব ৩.৩৫৩ গ্রাম/সিসি এবং গলনাঙ্ক ৭৩0 ডিগ্রি সেলসিয়াস।
বিক্রিয়া[সম্পাদনা]
ক্যালসিয়াম ব্রোমাইডকে বাতাসে খুব উত্তপ্ত করলে এটি বাতাসের অক্সিজেনের সাথে বিক্রিয়া করে ক্যালসিয়াম অক্সাইড এবং ব্রোমিন উৎপন্ন করে:
2 CaBr2 + O2 → 2 CaO + 2 Br2
এই বিক্রিয়াতে অক্সিজেন ব্রোমাইডকে ব্রোমিনে জারিত করে।
ব্যবহার[সম্পাদনা]
ক্যালসিয়াম ব্রোমাইডের ঘন জলীয় দ্রবণ প্রধানত ড্রিলিং এর জন্য ব্যবহৃত তরলে ব্যবহার হয়।[২] এটি স্নায়ুর ওষুধে, হিমশীতল মিশ্রণে, খাদ্য সংরক্ষণে, ফটোগ্রাফিতে এবং অগ্নি নিরোধক পদার্থ হিসাবে ব্যবহার করা হয়।[৩]
তথ্যসূত্র[সম্পাদনা]
- ↑ Michael J. Dagani, Henry J. Barda, Theodore J. Benya, David C. Sanders “Bromine Compounds” Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. ডিওআই:10.1002/14356007.a04_405
- ↑ Michael J. Dagani, Henry J. Barda, Theodore J. Benya, David C. Sanders “Bromine Compounds” Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH, Weinheim. doi:10.1002/14356007.a04_405
- ↑ "Chemical Land 21"। সংগ্রহের তারিখ ২৫ ডিসেম্বর ২০০৮।

